สื่อจะถือว่าเป็นกลางหากมีความเข้มข้นเท่ากัน (โมล/ลิตร) ของไฮโดรเนียมไอออน (H3อู๋+) และไฮดรอกไซด์ (OH-).
ตัวอย่างของตัวกลางที่เป็นกลางที่ทำหน้าที่เป็นมาตรฐานสำหรับสารละลายอื่นๆ ด้วยซ้ำคือน้ำกลั่นบริสุทธิ์ที่อุณหภูมิ 25ºC ที่อุณหภูมินี้ มันมี 1 พอดี 10-7 โมล/ลิตรของไอออนทั้งสอง ดังนั้นผลิตภัณฑ์ไอออนิกของคุณ (Kw) เท่ากับ 10-14 (นางสาว)2:
Kw = [H3อู๋+]. [โอ้-]
Kw = (1. 10-7 นางสาว). (1. 10-7 โมล/ลิตร) = 10-14 (นางสาว)2
ค่า pH และ pOH แสดงไว้ด้านล่าง:
pH= - บันทึก [H3อู๋+] pOH= -log[OH-]
pH= - บันทึก 1 10-7 pOH= - บันทึก 1 10-7
pH = 7pOH = 7
นี่แสดงให้เราเห็นว่า ในการแก้ปัญหาที่เป็นกลาง pH เท่ากับ pOH.
- กรดปานกลาง:
ในตัวกลางที่เป็นกรด ความเข้มข้นของ H ไอออน3อู๋+ มีขนาดใหญ่กว่าไอออนของ OH-.
การแก้ปัญหาดังกล่าวสามารถทำได้โดยการเพิ่มส่วนเล็ก ๆ ของไอออน H3อู๋+ตัวอย่างเช่น โดยใช้กรด
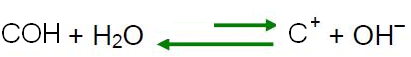
ตามหลักการของเลอ ชาเตอลิเยร์ เมื่อมีการรบกวนระบบในสภาวะสมดุล ระบบมักจะปรับตัวเองใหม่เพื่อลดผลกระทบของแรงนี้ ซึ่งหมายความว่าหากเติมกรดลงในน้ำ H ไอออน3อู๋+ พวกเขาจะเกินและความสมดุลจะเปลี่ยนในทิศทางปฏิกิริยาย้อนกลับไปทางซ้าย ดังนั้นอิออนส่วนเกินเหล่านี้จะทำปฏิกิริยากับ OH ไอออน
-. ดังนั้นความเข้มข้นของ OH ไอออน- จะลดลงและสารละลายจะกลายเป็นกรด
ผลิตภัณฑ์ไอออนิก (Kw) เท่ากับ 10. เสมอ-14แต่ความเข้มข้นของ H ไอออน3อู๋+ มากกว่าความเข้มข้นของไอออน OH-1. ดังนั้น pH จะมากกว่า pOH ในตัวกลางที่เป็นกรด แต่ผลรวมจะเท่ากับ 14 เสมอ
ยิ่งความเข้มข้นของไอออน H มากขึ้น3อู๋+, ยิ่งค่า pH สูงขึ้น ที่อุณหภูมิห้อง (25 องศาเซลเซียส) pH < 7 และ pOH> 7

- หมายถึงพื้นฐาน:
ในสื่อพื้นฐานความเข้มข้นของ OH ไอออน- มีขนาดใหญ่กว่าไอออน H3อู๋+.
ถ้าเราเติมเบสลงไปในน้ำ แสดงว่าเรากำลังเติมไอออน OH- และตามที่อธิบายไว้ในข้อที่แล้ว โดยหลักการของ Le Chatelier ความสมดุลของปฏิกิริยาของ ไอออนไนซ์ในตัวเองของน้ำจะเคลื่อนที่ไปในทิศทางตรงกันข้าม โดยมีไอออนส่วนเกินทำปฏิกิริยากับ H ไอออน3อู๋+ลดความเข้มข้นของคุณและทำให้สารละลายเป็นพื้นฐาน
ในกรณีนั้น pOH จะมากกว่า pH ที่อุณหภูมิห้อง (25 องศาเซลเซียส) pH > 7 และ pOH < 7

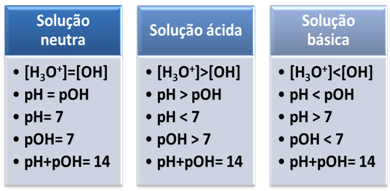
สั้น ๆ :
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
