ตารางธาตุเป็นเครื่องมือศึกษาที่สำคัญที่รวบรวมข้อมูลเกี่ยวกับองค์ประกอบทางเคมีที่รู้จักทั้งหมด
ทดสอบความรู้ของคุณด้วยรายการ .นี้ 17 คำถาม ด้วยแนวทางต่างๆ ในหัวข้อนี้และไขข้อสงสัยของคุณด้วยการลงมติที่แสดงความคิดเห็นหลังจากคำติชม
เพื่อช่วยให้เข้าใจคำถาม ให้ใช้ ตารางธาตุ สมบูรณ์และปรับปรุง
การจัดตารางธาตุ
คำถามที่ 1
(UFU) ในช่วงต้นศตวรรษที่ 19 ด้วยการค้นพบและแยกองค์ประกอบทางเคมีต่างๆ จึงจำเป็นต้องจำแนกประเภทอย่างมีเหตุผล เพื่อดำเนินการศึกษาอย่างเป็นระบบ มีการเพิ่มผลงานจำนวนมากจนกระทั่งถึงการจำแนกองค์ประกอบทางเคมีเป็นระยะในปัจจุบัน เกี่ยวกับการจำแนกตามงวดปัจจุบัน ให้ตอบ:
ก) ธาตุต่างๆ เรียงตามลำดับในตารางธาตุอย่างไร?
ตารางธาตุถูกจัดเป็นลำดับขององค์ประกอบทางเคมีในลำดับจากน้อยไปมากของ เลขอะตอม. ตัวเลขนี้สอดคล้องกับจำนวนโปรตอนในนิวเคลียสของอะตอม
วิธีการจัดระเบียบนี้เสนอโดย Henry Moseley เมื่อเขากำหนดค่าตารางที่เสนอโดย Dmitri Mendeleiev ใหม่
องค์ประกอบสามารถอยู่ในตารางโดยครอบครัวและช่วงเวลาที่แทรก การกระจายนี้เกิดขึ้นดังนี้:
| กลุ่มหรือครอบครัว | 18 ลำดับแนวตั้ง |
| กลุ่มขององค์ประกอบที่มีลักษณะคล้ายคลึงกัน |
| ประจำเดือน | 7 ลำดับแนวนอน |
| จำนวนชั้นอิเล็กทรอนิกส์ที่องค์ประกอบมี |
b) กลุ่มใดในตารางธาตุที่สามารถพบได้: ฮาโลเจน, โลหะอัลคาไล, โลหะอัลคาไลน์เอิร์ ธ, ชอล์กและก๊าซมีตระกูล?
การจำแนกองค์ประกอบออกเป็นกลุ่มทำได้ตามคุณสมบัติ องค์ประกอบที่อยู่ในกลุ่มเดียวกันมีลักษณะที่คล้ายคลึงกันและสำหรับการจัดประเภทที่กำหนดเราต้อง:
| การจำแนกประเภท | กลุ่ม | ครอบครัว | องค์ประกอบ |
| ฮาโลเจน | 17 | 7A | F, Cl, Br, I, At และ Ts |
| โลหะอัลคาไล | 1 | 1A | Li, Na, K, Rb, Cs และ Fr |
| โลหะอัลคาไลน์เอิร์ ธ | 2 | 2A | Be, Mg, Ca, Sr, Ba และ Ra |
| ชอล์ก | 16 | 6A | O, S, Se, Te, Po และ Lv |
| ก๊าซมีตระกูล | 18 | 8A | เขา, เน, อาร์, Kr, Xe, Rn และ Og |
คำถาม2
(PUC-SP) แก้ไขปัญหาตามการวิเคราะห์ข้อความด้านล่าง
I – ตารางธาตุสมัยใหม่ในปัจจุบันจัดเรียงตามมวลอะตอมจากน้อยไปมาก
II - องค์ประกอบทั้งหมดที่มี 1 อิเล็กตรอนและ 2 อิเล็กตรอนในเปลือกเวเลนซ์คือ ตามลำดับ โลหะอัลคาไลและโลหะอัลคาไลน์เอิร์ท โดยมีเงื่อนไขว่าเลขควอนตัมหลัก ของชั้นนี้ (n 1).
III – ในช่วงเวลาเดียวกัน องค์ประกอบจะแสดงจำนวนระดับ (เลเยอร์) เท่ากัน
IV – ในกลุ่มเดียวกัน (ตระกูล) องค์ประกอบมีจำนวนระดับ (เลเยอร์) เท่ากัน
สรุปได้ว่าสำหรับตารางธาตุปัจจุบันขององค์ประกอบทางเคมีนั้นถูกต้อง:
ก) ฉันและ IV (เท่านั้น)
b) I และ II (เท่านั้น)
c) II และ III (เท่านั้น)
ง) II และ IV (เท่านั้น)
จ) III และ IV (เท่านั้น)
ทางเลือกที่ถูกต้อง: c) II และ III (เท่านั้น)
การวิเคราะห์ทางเลือกแต่ละทางเราต้อง:
ฉันผิด. ธาตุต่างๆ เรียงตามลำดับจากน้อยไปมากของเลขอะตอม
II – ถูกต้อง อิเล็กตรอนในเปลือกความจุกำหนดกลุ่มที่องค์ประกอบตั้งอยู่
| โลหะอัลคาไล | 1 อิเล็กตรอนในเปลือกความจุ |
| 3อ่าน | 2-1 |
| 11ที่ | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87คุณพ่อ | 2-8-18-32-18-8-1 |
| โลหะอัลคาไลน์เอิร์ ธ | 2 อิเล็กตรอนในเปลือกความจุ |
| 4เป็น | 2-2 |
| 12มก. | 2-8-2 |
| 20ที่นี่ | 2-8-8-2 |
| 38นาย | 2-8-18-8-2 |
| 56บา | 2-8-18-18-8-2 |
| 88กบ | 2-8-18-32-18-8-2 |
หมายเลขควอนตัมหลักสอดคล้องกับเปลือกที่อิเล็กตรอนตั้งอยู่ซึ่งแตกต่างจาก 1 เพราะ โดยการกระจายทางอิเล็กทรอนิกส์เราสังเกตว่าตำแหน่งของอิเล็กตรอนนั้นมาจากเปลือกที่สองหรือ น=2.
III – ถูกต้อง ตำแหน่งขององค์ประกอบในช่วงเวลาหนึ่งเกิดจากจำนวนชั้นเมื่อทำการแจกจ่ายทางอิเล็กทรอนิกส์
| ประจำเดือน | 7 ลำดับแนวนอน |
| ช่วงที่ 1 | 1 ชั้น: K |
| ช่วงที่ 2 | 2 ชั้น: K, L |
| ช่วงที่ 3 | 3 ชั้น: K, L, M |
| ช่วงที่ 4 | 4 ชั้น: K, L, M, N |
| ช่วงที่ 5 | 5 ชั้น: K, L, M, N, O |
| ช่วงที่ 6 | 6 ชั้น: K, L, M, N, O, P |
| ช่วงที่ 7 | 7 ชั้น: K, L, M, N, O, P, Q |
ตัวอย่าง: องค์ประกอบทางเคมีตั้งอยู่ในช่วงที่สอง
IV – ผิด. องค์ประกอบที่อยู่ในกลุ่มเดียวกันมีลักษณะที่คล้ายคลึงกันและเนื่องจากข้อเท็จจริงที่ว่ามีอิเล็กตรอนจำนวนเท่ากันในเปลือกเวเลนซ์
ตัวอย่าง:
| เบริลเลียม | แมกนีเซียม |
|
2 อิเล็กตรอนใน ชั้นวาเลนซ์ |
2 อิเล็กตรอนใน ชั้นวาเลนซ์ |
ดังนั้นเบริลเลียมและแมกนีเซียมจึงเป็นส่วนหนึ่งของกลุ่มที่ 2 ของตารางธาตุ
คำถาม 3
(Unitins) เกี่ยวกับการจำแนกองค์ประกอบตามช่วงเวลาที่ทันสมัยให้ระบุข้อความที่แท้จริง:
ก) ในครอบครัว ธาตุโดยทั่วไปมีจำนวนอิเล็กตรอนเท่ากันในเปลือกสุดท้าย
b) ในตารางธาตุ องค์ประกอบทางเคมีจะเรียงตามลำดับมวลอะตอมจากมากไปน้อย
c) ในครอบครัว ธาตุมีคุณสมบัติทางเคมีที่แตกต่างกันมาก
d) ในช่วงเวลาหนึ่งองค์ประกอบมีคุณสมบัติทางเคมีที่คล้ายคลึงกัน
จ) องค์ประกอบที่เป็นตัวแทนทั้งหมดอยู่ในกลุ่ม B ของตารางธาตุ
ทางเลือกที่ถูกต้อง: ก) ในครอบครัว องค์ประกอบโดยทั่วไปมีจำนวนอิเล็กตรอนเท่ากันในเปลือกสุดท้าย
ก) ถูกต้อง องค์ประกอบทางเคมีของตระกูลเดียวกันมีจำนวนอิเล็กตรอนเท่ากันในเปลือกสุดท้ายและทำให้มีลักษณะคล้ายกัน
ข) ผิด มวลอะตอมเพิ่มขึ้นเมื่อเลขอะตอมของธาตุเพิ่มขึ้น
ค) ผิด คุณสมบัติทางเคมีของธาตุมีความคล้ายคลึงกันจึงจัดอยู่ในกลุ่มเดียวกัน
ง) ผิด ครั้งหนึ่ง ธาตุมีอิเล็กตรอนกระจายอยู่ในเปลือกจำนวนเท่ากัน
จ) ผิด องค์ประกอบที่เป็นตัวแทนอยู่ในกลุ่ม A ซึ่งสอดคล้องกับตระกูล: 1A, 2A, 3A, 4A, 5A, 6A, 7A และ 8A องค์ประกอบที่อยู่ในกลุ่ม B คือองค์ประกอบการเปลี่ยนแปลง
คำถาม 4
(Vunesp) เมื่อพิจารณาถึงคุณสมบัติขององค์ประกอบทางเคมีและตารางธาตุแล้วจะระบุไม่ถูกต้อง:
ก) โลหะคือสารที่นำกระแสไฟฟ้า มีความเหนียวและอ่อนตัวได้
ข) อโลหะ คือ สารที่ไม่นำกระแสไฟฟ้า ไม่เหนียวเหนอะหนะ
c) กึ่งโลหะมีลักษณะทางกายภาพของโลหะ แต่มีพฤติกรรมทางเคมีคล้ายกับของอโลหะ
d) องค์ประกอบทางเคมีส่วนใหญ่ประกอบด้วยอโลหะ
จ) ก๊าซมีตระกูลเป็นอะตอมเดี่ยว
ทางเลือกที่ไม่ถูกต้อง: d) องค์ประกอบทางเคมีส่วนใหญ่เป็นอโลหะ
สังเกตการจำแนกองค์ประกอบทางเคมีในตารางธาตุเป็นโลหะ อโลหะ และกึ่งโลหะ

อย่างที่เราเห็น ธาตุส่วนใหญ่เป็นโลหะ
ก) ถูกต้อง โลหะนำไฟฟ้าเนื่องจากเมฆอิเล็กตรอนที่เกิดจากอิเล็กตรอนอิสระ ซึ่งเป็นลักษณะเฉพาะของโครงสร้าง มีความเหนียวเนื่องจากสามารถเปลี่ยนเป็นลวดหรือแผ่นได้ ขึ้นอยู่กับบริเวณที่ใช้แรงกด พวกเขายังอ่อนตัวได้ เนื่องจากวัสดุประเภทนี้สามารถผลิตแผ่นบางมากได้
ข) ถูกต้อง อโลหะมีลักษณะตรงกันข้ามกับโลหะ แทนที่จะเป็นตัวนำ พวกมันเป็นฉนวนความร้อนที่ดีและเนื่องจากเปราะ พวกมันจึงไม่ถูกหล่อเป็นเส้นลวดหรือแผ่นเนื่องจากไม่มีความเหนียวและความเหนียวที่ดี
ค) ถูกต้อง เซมิเมทัลมีลักษณะเป็นสื่อกลางถึงโลหะและอโลหะ ในฐานะที่เป็นเซมิคอนดักเตอร์ของไฟฟ้า พวกมันมีเงาโลหะแต่เปราะเหมือนอโลหะ
ง) ผิด องค์ประกอบส่วนใหญ่จัดเป็นโลหะ ประเภทของโลหะที่มีอยู่ในตารางธาตุ ได้แก่ อัลคาไลน์ เอิร์ ธ การเปลี่ยนภายในและภายนอก
จ) ถูกต้อง ก๊าซมีตระกูลเป็นอะตอมเดี่ยว ดังนั้นจึงแสดงด้วยอักษรย่อเท่านั้น
ตัวอย่าง:
| ก๊าซมีตระกูล | ชอล์ก |
| ฮีเลียม (เขา) | ออกซิเจน (O2) |
| monoatomic: เกิดขึ้นจากอะตอม | ไดอะตอม: เกิดขึ้นจากสองอะตอม |
เนื่องจากความเสถียรของก๊าซมีตระกูล องค์ประกอบของตระกูลนี้มีปฏิกิริยาต่ำและเรียกอีกอย่างว่าเฉื่อย
คำถาม 5
เกี่ยวกับการจัดตารางธาตุปัจจุบัน ให้ตอบ:
ก) คอลัมน์คืออะไร?
b) เส้นคืออะไร?
ค) วิธีการที่ใช้ในการจัดองค์ประกอบทางเคมีคืออะไร?
คำตอบ:
ก) คอลัมน์คือกลุ่มของตารางธาตุซึ่งเดิมเรียกว่าครอบครัว ซึ่งรวบรวมองค์ประกอบทางเคมีที่มีคุณสมบัติคล้ายคลึงกัน
b) เส้นคือคาบของตารางธาตุและระบุจำนวนชั้นอิเล็กทรอนิกส์ของอะตอมในสถานะพื้นดิน
c) องค์ประกอบทางเคมีในตารางธาตุปัจจุบันถูกจัดเรียงจากน้อยไปหามากของเลขอะตอม ซึ่งระบุจำนวนโปรตอนในนิวเคลียสของอะตอม
ครอบครัวตารางธาตุ
คำถามที่ 1
(CESGRANRIO) การสร้างความสัมพันธ์ระหว่างคอลัมน์ด้านล่างซึ่งสอดคล้องกับตระกูลองค์ประกอบตามตารางธาตุ ลำดับตัวเลขจะเป็น:
| 1. ก๊าซมีตระกูล | • กลุ่ม 1A |
| 2. โลหะอัลคาไล | • กลุ่ม 2A |
| 3. โลหะอัลคาไลน์เอิร์ ธ | • กลุ่ม 6A |
| 4. Chalcogens | • กลุ่ม 7A |
| 5. ฮาโลเจน | • กลุ่ม 0 |
ก) 1, 2, 3, 4, 5.
ข) 2, 3, 4, 5, 1
ค) 3, 2, 5, 4, 1
ง) 3, 2, 4, 5, 1
จ) 5, 2, 4, 3, 1
ทางเลือกที่ถูกต้อง: b) 2, 3, 4, 5, 1
| กลุ่ม | การกำหนดค่าทางอิเล็กทรอนิกส์ |
| • กลุ่ม 1A: 2. โลหะอัลคาไล | เรา1 (กับ n |
| • กลุ่ม 2A: 3. โลหะอัลคาไลน์เอิร์ ธ | เรา2 (กับ n |
| • กลุ่ม 6A: 4. Chalcogens | เรา2np4 |
| • กลุ่ม 7A: 5. ฮาโลเจน | เรา2np5 |
| • กลุ่ม 0: 1. ก๊าซมีตระกูล | 1s2 (เขา) หรือ เรา2np6 (ถ้า n > 1) |
คำถาม2
(UECE) องค์ประกอบทางเคมีที่มี Z = 54 มีการกำหนดค่า 5s ในชั้นเวเลนซ์2 5p6. องค์ประกอบที่มี Z = 52 และ Z = 56 อยู่ในตระกูลของ:
ก) ชอล์กและอัลคาไลน์เอิร์ ธ
b) ฮาโลเจนและด่าง
c) ฮาโลเจนและอัลคาไลน์เอิร์ ธ
d) ชอล์กและด่าง a
ทางเลือกที่ถูกต้อง: ก) chalcogens และอัลคาไลน์เอิร์ ธ
จากเลขอะตอม เราทำการแจกแจงทางอิเล็กทรอนิกส์และพบผลลัพธ์ต่อไปนี้:
| 54X และ | 52คุณ | 56บา |
|
8 อิเล็กตรอนใน ชั้นวาเลนซ์ |
6 อิเล็กตรอนใน ชั้นวาเลนซ์ |
2 อิเล็กตรอนใน ชั้นวาเลนซ์ |
| ก๊าซมีตระกูล: ตระกูล 8A | Chalcogens: ตระกูล 6A | อัลคาไลน์เอิร์ ธ: ตระกูล 2A |
คำถาม 3
(ฟ. Ibero-Americana-SP) กลุ่มตารางธาตุที่มีลักษณะเด่นขององค์ประกอบเทียมมีดังต่อไปนี้:
ก) แลนทาไนด์
b) ก๊าซมีตระกูล
c) โลหะทรานสิชัน
d) โลหะอัลคาไลน์เอิร์ ธ
จ) แอคติไนด์
ทางเลือกที่ถูกต้อง: จ) แอคติไนด์
องค์ประกอบประดิษฐ์คือสิ่งที่ไม่มีอยู่ในธรรมชาติและได้รับการสังเคราะห์ในห้องปฏิบัติการผ่านปฏิกิริยานิวเคลียร์
พวกเขายังเรียกว่าองค์ประกอบ transuranic เนื่องจากองค์ประกอบกัมมันตภาพรังสีเหล่านี้มีเลขอะตอมมากกว่า 92 ซึ่งสอดคล้องกับยูเรเนียม
โดยทั่วไป องค์ประกอบเหล่านี้มีอายุสั้น โดยคงอยู่นานถึงเสี้ยววินาที
ตามข้อมูลนี้เราต้อง:
ธาตุที่พบในธรรมชาติ ได้แก่ แลนทาไนด์ ก๊าซมีตระกูล โลหะทรานซิชัน และโลหะอัลคาไลน์เอิร์ท ยกเว้นเทคนีเชียมและโพรมีเธียมซึ่งเป็นของเทียม
ธาตุที่เด่นกว่าคือแอกทิไนด์ ซึ่งจัดเป็นโลหะทรานซิชันภายใน และใส่ไว้ในตารางธาตุด้านล่างแลนทาไนด์ จากซีรีส์นั้น มีเพียงแอกทิเนียม ทอเรียม โพรแทกทิเนียม และยูเรเนียมเท่านั้นที่เป็นธรรมชาติ
คำถาม 4
(ยู. โบสถ์คาทอลิกแห่งซัลวาดอร์-BA) สายพันธุ์ X2- ด้วยอิเล็กตรอน 8 ตัวในเปลือกนอกสุด (เปลือกวาเลนซ์) มันสามารถมาจากองค์ประกอบ X ซึ่งในตารางธาตุเป็นของกลุ่ม:
ก) 7A
ข) 6A
ค) 2A
ง) 1A
จ) 8A
ทางเลือกที่ถูกต้อง: b) 6A
ตามกฎออกเตต สำหรับองค์ประกอบที่จะได้รับความเสถียร จะถือว่าองค์ประกอบทางอิเล็กทรอนิกส์ของก๊าซมีตระกูลซึ่งมีอิเล็กตรอน 8 ตัวในเปลือกเวเลนซ์
ชาร์จ 2- ในสายพันธุ์ X2- แสดงว่าธาตุได้รับ 2 อิเล็กตรอน
การกำหนดค่าอิเล็กตรอนของสปีชีส์ที่มี 8 อิเล็กตรอนในเปลือกนอกสุดคือns2np6.
เมื่อสูญเสียอิเล็กตรอนไป 2 ตัว ธาตุจะกลับสู่สถานะกราวด์ด้วยการกำหนดค่า ns ของอิเล็กตรอน2np4.
อิเล็กตรอน 6 ตัวในเปลือกเวเลนซ์เป็นลักษณะของคาลโคเจน ซึ่งเป็นองค์ประกอบของตระกูล 6A
ตัวอย่างเช่น:
| ธาตุ: ออกซิเจน | การกำหนดค่าทางอิเล็กทรอนิกส์ |
| 8อู๋ | 1s22s22p4 |
| สายพันธุ์ O2- | 1s22s22p6 |
ดูข้อมูลเพิ่มเติมเกี่ยวกับ ครอบครัวตารางธาตุ.
องค์ประกอบทางเคมี
คำถามที่ 1
(CESGRANRIO) จากองค์ประกอบของเลขอะตอม 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 และ 75 ตัวเลือกที่มีเฉพาะโลหะอัลคาไลคือ:
ก) 3, 11, 37 และ 55
ข) 3, 9, 37 และ 55
ค) 9, 11, 38 และ 55
ง) 12, 20, 38 และ 56
จ) 12, 37, 47 และ 75
ทางเลือกที่ถูกต้อง: ก) 3, 11, 37 และ 55
โลหะอัลคาไลสอดคล้องกับองค์ประกอบทางเคมีที่สิ้นสุดการกระจายทางอิเล็กทรอนิกส์ด้วยอิเล็กตรอนในระดับย่อย
จากการแจกแจงทางอิเล็กทรอนิกส์ของเลขอะตอมที่กำหนด เรามีโลหะอัลคาไลดังต่อไปนี้:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| ลิเธียม | โซเดียม | รูบิเดียม | ซีเซียม |
เลขอะตอมอื่น ๆ สอดคล้องกับองค์ประกอบของกลุ่มต่อไปนี้:
โลหะอัลคาไลน์เอิร์ธ: ยุติการจำหน่ายทางอิเล็กทรอนิกส์ที่ระดับย่อย s2.
| Z = 12 | Z = 38 | Z = 56 |
| แมกนีเซียม | สตรอนเทียม | แบเรียม |
โลหะทรานซิชัน: ยุติการจำหน่ายทางอิเล็กทรอนิกส์ที่ระดับย่อย ง.
| Z = 30 | Z = 47 | Z = 75 |
| สังกะสี | เงิน | รีเนียม |
ฮาโลเจน: ยุติการจำหน่ายทางอิเล็กทรอนิกส์ที่ระดับย่อย p5.
| Z = 9 |
คำถาม2
(Unirio) “หัวใจเทียมที่วางไว้ใน Eloi เริ่มมีการพัฒนาเมื่อสี่ปีที่แล้วในสหรัฐอเมริกาและมีคนใช้ไปแล้วประมาณ 500 คน ชุดที่เรียกว่าฮาร์ทเมทประกอบด้วยสามส่วนหลัก ที่สำคัญที่สุดคือกระเป๋าทรงกลมขนาด 4 ปอนด์ เส้นผ่านศูนย์กลาง 12 ซม. และหนา 3 ซม. ทำจากไททาเนียม ซึ่งเป็นโลหะสีเงิน-ขาว เบาและแข็งแรง” นิตยสาร Veja กรกฎาคม 2542
ในบรรดาโลหะด้านล่าง หนึ่งที่มีในชั้นสุดท้าย จำนวนอิเล็กตรอนเท่ากับไททาเนียมคือ:
ก) C
ข) ใน
ค) กา
ง) มก
จ) Xe
ทางเลือกที่ถูกต้อง: d) มก.
| ไทเทเนียม | การกำหนดค่าทางอิเล็กทรอนิกส์ | การกระจายชั้น |
| 22คุณ | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
จากการกระจายทางอิเล็กทรอนิกส์ของไททาเนียม เราจะเห็นว่าธาตุนี้มีอิเล็กตรอน 2 ตัวในเปลือกสุดท้าย
| ธาตุ | การกำหนดค่าทางอิเล็กทรอนิกส์ | การกระจายชั้น |
| 6ค | 1s2 2s2 2p2 | 2, 4 |
| 11ที่ | 1s2 2s2 2p6 3s1 | 2, 8, 1 |
| 31กา | 1s2 2s2 2p6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12มก. | 1s2 2s2 2p6 3s2 | 2, 8, 2 |
| 54X และ | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4 วัน10 5s2 5p6 | 2, 8, 18, 18, 8 |
ธาตุที่มีอิเลคตรอน 2 ตัวในชั้นสุดท้ายคือแมกนีเซียม
คำถาม 3
(UFPA) พิจารณาองค์ประกอบทางเคมีบางอย่างที่มีระดับย่อยที่มีพลังมากที่สุดคือ 5s2. เลขอะตอมและหมู่ที่อยู่ในตารางธาตุมีดังนี้
ก) 20; 1A
ข) 20; 2A
ค) 38; 2A
ง) 38; 1A
จ) 39; 2A
ทางเลือกที่ถูกต้อง: c) 38; 2A
โดยทำการกระจายทางอิเล็กทรอนิกส์ เราพบว่า:
- องค์ประกอบทางเคมีอยู่ในตระกูล 2Aเนื่องจากมีระดับย่อยที่มีพลังมากที่สุด s2
- มีเลขอะตอม 38ซึ่งสอดคล้องกับจำนวนอิเล็กตรอนที่กระจายไปทั้งหมด
- ตั้งอยู่ในช่วงที่ห้าเนื่องจากการกระจายทางอิเล็กทรอนิกส์ได้ดำเนินการถึงชั้นที่ห้า
การตรวจสอบข้อมูลนี้ในตารางธาตุเราสามารถยืนยันได้ว่ามันเป็นธาตุสตรอนเทียม
คำถาม 4
(UFC) อะตอม x มีโปรตอนมากกว่าอะตอม y หนึ่งตัว จากข้อมูลนี้ ให้กำหนดข้อความที่ถูกต้อง
a) ถ้า y เป็นอัลคาไลน์เอิร์ ธ x คือโลหะอัลคาไล
b) ถ้า y เป็นแก๊สมีตระกูล x คือฮาโลเจน
c) ถ้า y เป็นโลหะทรานซิชัน x เป็นแก๊สมีตระกูล
d) ถ้า y เป็นแก๊สมีตระกูล x คือโลหะอัลคาไล
จ) x อยู่ในคาบเดียวกันก่อนอะตอม y ในตารางธาตุ
ทางเลือกที่ถูกต้อง: d) ถ้า y เป็นก๊าซมีตระกูล x คือโลหะอัลคาไล
ตารางธาตุเรียงจากน้อยไปมากของเลขอะตอม
ถ้า Y มีเลขอะตอม z และ X มีโปรตอนมากกว่า 1 ตัว แสดงว่าธาตุทั้งสองนี้อยู่ในคาบเดียวกันและ X อยู่หลัง Y
ตัวอย่าง:
| ธาตุ | องค์ประกอบที่ตามมา |
| zY | z + 1X |
| 11ที่ | 12มก. |
ธาตุทั้งสองอยู่ในคาบที่ 3 และแมกนีเซียมมีโปรตอนมากกว่าโซเดียมหนึ่งตัว
ตามเหตุผลนี้เราต้อง:
ก) ผิด โลหะอัลคาไลมาก่อนโลหะอัลคาไลน์เอิร์ธในตารางธาตุ ข้อความที่ถูกต้องคือ ถ้า y เป็นโลหะอัลคาไล x คืออัลคาไลน์เอิร์ธ
ข) ผิด ฮาโลเจนมาก่อนก๊าซมีตระกูลในตารางธาตุ ข้อความที่ถูกต้องคือ ถ้า y เป็นฮาโลเจน x คือก๊าซมีตระกูล
ค) ผิด โลหะทรานซิชันและก๊าซมีตระกูลจะถูกแยกจากกันโดยองค์ประกอบทางเคมีอื่นๆ ดังนั้นจึงไม่เป็นไปตามลำดับ
ง) ถูกต้อง ก๊าซมีตระกูลเป็นกลุ่มสุดท้ายในตารางธาตุและโลหะอัลคาไลเป็นกลุ่มแรก ดังนั้นพวกมันจึงเรียงตามลำดับ
ตัวอย่าง:
| ก๊าซมีตระกูล | โลหะอัลคาไล |
| zY | z + 1X |
| 2เขา | 3อ่าน |
ลิเธียมซึ่งเป็นโลหะอัลคาไลมีโปรตอนมากกว่าฮีเลียมซึ่งเป็นก๊าซมีตระกูล
จ) ผิด X อยู่ในคาบเดียวกับ Y แต่หลังจากนั้น ไม่ใช่ช่วงก่อนหน้าของสถานะทางเลือก
คำถาม 5
จากเลขอะตอมขององค์ประกอบทางเคมี เป็นไปได้ที่จะรู้:
ก) จำนวนนิวตรอนในนิวเคลียส
b) จำนวนอิเล็กตรอนในอิเล็กโตรสเฟียร์
c) มวลแกน
คำตอบ: b) จำนวนอิเล็กตรอนในอิเล็กโตรสเฟียร์
อะตอมในสถานะพื้นดินเป็นกลางทางไฟฟ้า ดังนั้น เมื่อรู้เลขอะตอมซึ่งสอดคล้องกับจำนวนโปรตอน (อนุภาคที่มีประจุบวก) เราจึงทราบจำนวนอิเล็กตรอน (อนุภาคที่มีประจุลบ) ในอิเล็กโตรสเฟียร์
ตัวอย่างเช่น เหล็กมีเลขอะตอม 26 ดังนั้นในสถานะพื้นดินจะมีอิเล็กตรอน 26 ตัวรอบนิวเคลียส
ดูข้อมูลเพิ่มเติมเกี่ยวกับ องค์ประกอบทางเคมี มันเป็น เลขอะตอม.
คุณสมบัติเป็นระยะและเป็นระยะ
คำถามที่ 1
(UFSM) ตัดสินว่าข้อความที่เกี่ยวข้องกับคุณสมบัติเป็นระยะขององค์ประกอบเป็นจริง (T) หรือเท็จ (F)
( ) ขึ้นอยู่กับมวลอะตอมของธาตุ
( ) มีการทำซ้ำในช่วงเวลาปกติมากหรือน้อยเมื่อเทียบกับการเพิ่มขึ้นของเลขอะตอม
( ) มีความคล้ายคลึงกันในกลุ่มองค์ประกอบเดียวกัน
( ) มีความคล้ายคลึงกันในช่วงธาตุเดียวกัน
( ) ในกลุ่มเดียวกัน ค่าตัวเลขของคุณสมบัติเป็นระยะจะเพิ่มขึ้นเสมอเมื่อมีการเพิ่มจำนวนอะตอมของธาตุ
ลำดับที่ถูกต้องคือ:
ก) V - F - V - F - F
b) V - F - F - V - V
ค) F - V - V - F - F
ง) F - V - F - V - V
จ) V - F - F - V - F
ทางเลือกที่ถูกต้อง: c) F - V - V - F - F
(FALSE) ขึ้นอยู่กับมวลอะตอมของธาตุ
ตามกฎของคาบของโมสลีย์ คุณสมบัติทางกายภาพและทางเคมีหลายอย่างขององค์ประกอบทางเคมีจะแปรผันตามเลขอะตอม
(TRUE) มีการทำซ้ำในช่วงเวลาปกติมากหรือน้อยเมื่อเทียบกับการเพิ่มขึ้นของเลขอะตอม
คุณสมบัติ เช่น รัศมีอะตอม ปริมาตรอะตอม ความหนาแน่น จุดหลอมเหลว และการเดือด เป็นตัวอย่างของคุณสมบัติที่เกิดขึ้นเป็นประจำในตารางธาตุ
(TRUE) มีความคล้ายคลึงกันในกลุ่มองค์ประกอบเดียวกัน
กลุ่มตารางธาตุถูกจัดเรียงด้วยองค์ประกอบที่มีคุณสมบัติคล้ายคลึงกัน
(FALSE) มีความคล้ายคลึงกันในช่วงเวลาเดียวกันของธาตุ
คุณสมบัติมีความคล้ายคลึงกันในครอบครัวไม่ใช่ประจำเดือน ในช่วงเวลา องค์ประกอบจะกระจายตามจำนวนชั้นอิเล็กทรอนิกส์
(FALSE) ในกลุ่มเดียวกัน ค่าตัวเลขของคุณสมบัติเป็นระยะจะเพิ่มขึ้นเสมอเมื่อมีการเพิ่มจำนวนอะตอมขององค์ประกอบ
คุณสมบัติสามารถเพิ่มหรือลดได้ขึ้นอยู่กับเลขอะตอม ตัวอย่างของสิ่งนี้คืออิเล็กโตรเนกาติวีตี้ ซึ่งลดลงเมื่อเลขอะตอมเพิ่มขึ้นในกลุ่มที่กำหนด
อ่านด้วย: คุณสมบัติเป็นระยะ
คำถาม2
(FAESP) คุณสมบัติ aperiodic ขององค์ประกอบคือ:
ก) ความหนาแน่น ปริมาตรอะตอม และมวลอะตอม
b) จุดหลอมเหลว อิเล็กโตรเนกาติวีตี้ และความร้อนจำเพาะ
ค) ปริมาตรอะตอม มวลอะตอม และจุดหลอมเหลว
ง) มวลอะตอม ความร้อนจำเพาะ และจุดหลอมเหลว
จ) มวลอะตอมและความร้อนจำเพาะ
ทางเลือกที่ถูกต้อง: จ) มวลอะตอมและความร้อนจำเพาะ
คุณสมบัติ aperiodic จะทำซ้ำเป็นระยะ
มวลอะตอมคือการวัดน้ำหนักของอะตอมในหน่วยมวลอะตอมซึ่งตรงกับ ของมวลคาร์บอน-12
ความร้อนจำเพาะกำหนดปริมาณความร้อนที่จำเป็นในการเพิ่มอุณหภูมิ 1 °C ขององค์ประกอบ 1 กรัม
คุณสมบัติทั้งสองนี้ไม่เกี่ยวข้องกับตำแหน่งของธาตุในตารางธาตุ
คุณสมบัติอื่น ๆ ถูกจัดประเภทเป็นระยะ ๆ ตามที่เพิ่มขึ้นหรือลดลงด้วยเลขอะตอม ที่พวกเขา:
- ความหนาแน่น: หมายถึงผลหารระหว่างมวลและปริมาตรของธาตุ
- ปริมาตรอะตอม: แทนปริมาตรของชุดอะตอมและส่งผลต่อระยะห่างระหว่างอะตอมทั้งสอง
- จุดหลอมเหลว: อุณหภูมิที่เกิดการเปลี่ยนแปลงจากของแข็งเป็นของเหลว
- อิเล็กโตรเนกาติวีตี้: ความสามารถของอะตอมในการดึงดูดคู่อิเล็กทรอนิกส์ที่มีพันธะโควาเลนต์มาสู่ตัวเอง
อ่านด้วย: อิเล็กโตรเนกาติวีตี้ และ ความสัมพันธ์ทางอิเล็กทรอนิกส์
คำถาม 3
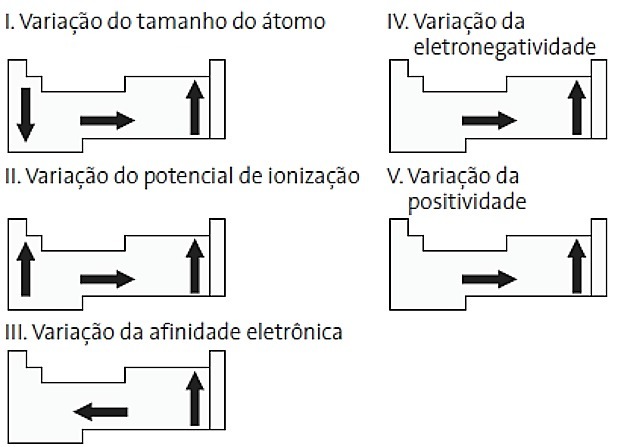
(PUC-PR) จากไดอะแกรมที่เกี่ยวข้องกับตารางธาตุต่อไปนี้ ข้อใดถูกต้อง
ก) II และ V
ข) II และ III
c) ฉันและV
ง) II และ IV
จ) III และ IV
ทางเลือกที่ถูกต้อง: d) II และ IV
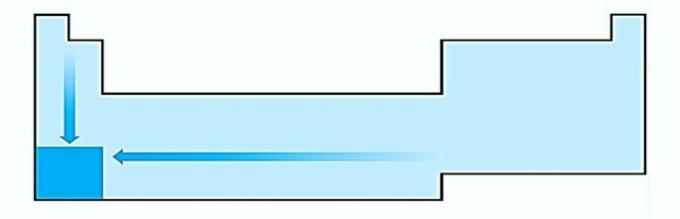
ผม. ไม่ถูกต้อง. ความแปรผันของขนาดอะตอมวัดจากระยะห่างเฉลี่ยจากนิวเคลียสถึงอิเล็กตรอนชั้นนอกสุด อะตอมที่ใหญ่ที่สุดจะอยู่ที่ด้านล่างของตาราง ดังนั้นการเพิ่มขึ้นจึงเกิดขึ้นตามเลขอะตอมและการแทนค่าที่ถูกต้องคือ:
ครั้งที่สอง แก้ไข พลังงานที่จำเป็นในการฉีกอิเล็กตรอนออกจากอะตอมที่แยกเดี่ยวในสถานะก๊าซเรียกว่าศักย์อิออไนเซชัน จะเพิ่มขึ้นตามที่แสดงในไดอะแกรมคำสั่ง
สาม. ไม่ถูกต้อง. ความสัมพันธ์ทางอิเล็กทรอนิกส์เป็นการแสดงออกถึงพลังงานที่ปล่อยออกมาเมื่ออะตอมที่เป็นกลางในสถานะก๊าซได้รับอิเล็กตรอนซึ่งเป็นคุณสมบัติที่สำคัญมากของอโลหะ พบความสัมพันธ์ทางอิเล็กทรอนิกส์สูงสุดในฮาโลเจนและออกซิเจน
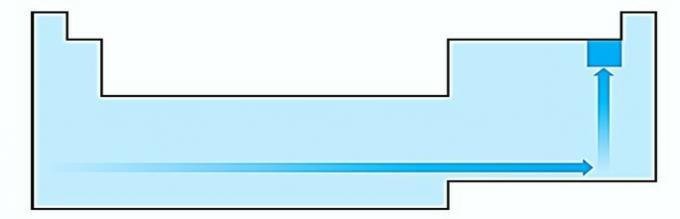
IV. แก้ไข อิเล็กโตรเนกาติวีตี้เกี่ยวข้องกับศักยภาพการแตกตัวเป็นไอออนและความสัมพันธ์ของอิเล็กตรอน ด้วยเหตุนี้ ฮาโลเจนจึงเป็นองค์ประกอบทางไฟฟ้าที่มากที่สุดในตารางธาตุ
วี ไม่ถูกต้อง. Electropositivity เกิดขึ้นในทิศทางตรงกันข้ามกับอิเล็กโตรเนกาติวีตี้ มันแสดงถึงความสามารถของอะตอมในการเลิกใช้อิเล็กตรอน
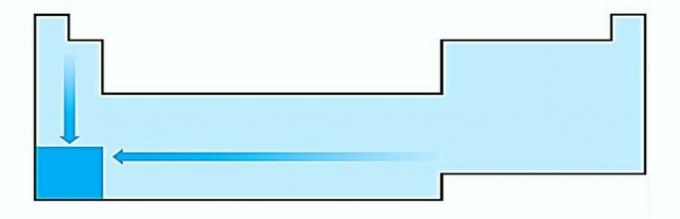
ดังนั้นโลหะอัลคาไลจึงมีอิเล็กโตรโพซิทีฟมากที่สุด
ทดสอบความรู้ของคุณด้วยรายการ:
- แบบฝึกหัดเกี่ยวกับพันธะเคมี
- แบบฝึกหัดเกี่ยวกับการกระจายทางอิเล็กทรอนิกส์
- แบบฝึกหัดเกี่ยวกับแบบจำลองอะตอม
- แบบฝึกหัดเกี่ยวกับเทอร์โมเคมี