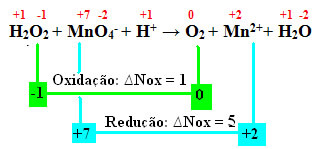
พิจารณาปฏิกิริยาผันกลับได้ทั่วไปด้านล่าง โดยที่ตัวอักษรพิมพ์เล็กสอดคล้องกับสัมประสิทธิ์ปฏิกิริยาที่สมดุล และตัวอักษรตัวพิมพ์ใหญ่คือสารตั้งต้นและผลิตภัณฑ์ทั้งหมดเป็นก๊าซ:

เมื่อพิจารณาแต่ละทิศทางปฏิกิริยาแยกกัน อัตราการพัฒนา (Td) ของพวกมันถูกกำหนดโดย:
*ปฏิกิริยาโดยตรง: aA + bB → cC + dD
ทั้งหมดโดยตรง = Kโดยตรง. [THE]ดิ. [B]บี
*ปฏิกิริยาย้อนกลับ: cC + dD → aA + bB
ทั้งหมดผกผัน = Kย้อนกลับ. [ค]ค. [ด]d
ค่าคงที่สมดุลเคมีในแง่ของความเข้มข้นในปริมาณของสสาร (Kค) และในแง่ของความดันบางส่วน (Kพี) จะได้รับโดยการหาร Kโดยตรง โดย Kย้อนกลับ.
ดังนั้นเราจึงมี:
Kโดยตรง. [THE]ดิ. [B]บี = 1 → Kโดยตรง__ = __[ค]ค. [ด]d___
Kย้อนกลับ. [ค]ค. [ด]d Kย้อนกลับ [THE]ดิ. [B]บี
เป็น, Kค =_Kโดยตรง_
Kย้อนกลับ
ดังนั้นเราจึงมี:
Kค =__[ค]ค. [ด]d___ หรือ Kพี =__(ปราซา)ค. (พีดี)d___ |
โดยที่ p คือความดันบางส่วนของสารแต่ละชนิดในสภาวะสมดุล
ด้วยวิธีนี้ ความเข้มข้นแต่ละอย่างจะเพิ่มขึ้นเป็นเลขชี้กำลังที่สอดคล้องกับสัมประสิทธิ์ของสารแต่ละตัวในปฏิกิริยา และ Kค ไม่มีหน่วย*
นอกจากนี้ สิ่งสำคัญที่ต้องเน้นคือในนิพจน์นี้
ไม่ควรแสดงส่วนประกอบที่เป็นของแข็งหรือของเหลวบริสุทธิ์เนื่องจากมีเพียงเรื่องที่สามารถรับความผันแปรเท่านั้นที่มีส่วนร่วมในนิพจน์นี้ ความเข้มข้นของปริมาณสสารในสถานะของแข็งจะคงที่และรวมอยู่ในค่าของ K เองแล้วค. เช่นเดียวกับของเหลวบริสุทธิ์เช่นน้ำ ในระยะสั้น เฉพาะสารที่อยู่ในสถานะก๊าซและในสารละลายที่เป็นน้ำเท่านั้นที่มีส่วนร่วมในการแสดงออกอย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
สังเกตตัวอย่างด้านล่าง:
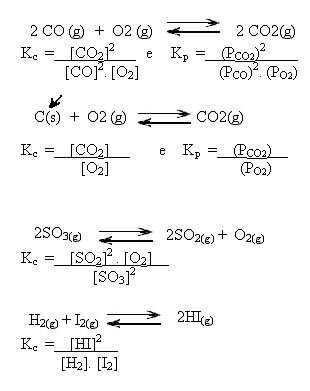
ค่า Kค สามารถแสดงให้เราเห็นว่าความเข้มข้นของสารตั้งต้นและผลิตภัณฑ์มีค่าเท่ากันหรือตัวใดตัวหนึ่งมากกว่าตัวอื่น:
- ถ้า Kค หรือ Kพี เท่ากับหนึ่ง (Kค = 1)ซึ่งหมายความว่าความเข้มข้นของสารตั้งต้นและผลิตภัณฑ์มีค่าเท่ากัน
- ถ้าค่าของ Kค หรือ Kพี สูงซึ่งหมายความว่าผลิตภัณฑ์มีความเข้มข้นมากขึ้นเพราะในการแสดงออกของKค สินค้าอยู่ในตัวเศษ
- ถ้าค่าของ Kค หรือ Kพี อยู่ในระดับต่ำซึ่งหมายความว่ารีเอเจนต์มีความเข้มข้นสูงกว่าเพราะในการแสดงออกของKค รีเอเจนต์อยู่ในตัวส่วน
*Kค และ Kพี เป็นตัวเลขไร้มิติ กล่าวคือ ตัวเลขล้วนๆ ไม่มีหน่วยที่เกี่ยวข้องกับขนาดหรือความสัมพันธ์ระหว่างขนาดใดๆ
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ค่าคงที่สมดุล Kc และ Kp"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.