หนึ่ง สารละลายบัฟเฟอร์ เป็นส่วนผสมที่ใช้ป้องกันไม่ให้ pH หรือ pOH ของตัวกลางเปลี่ยนแปลงเมื่อเติมกรดแก่หรือด่างแก่
สารละลายบัฟเฟอร์มีสองประเภท:
1. ส่วนผสมของกรดอ่อนกับเบสคอนจูเกต
2. ส่วนผสมของเบสอ่อนกับกรดคอนจูเกต
มาดูตัวอย่างกันและวิธีการทำงานเมื่อเติมกรดหรือเบสแก่ในปริมาณเล็กน้อยลงในสื่อ:
1. ส่วนผสมของกรดอ่อนกับเบสคอนจูเกต:
ในการสร้างสารละลายดังกล่าว กรดอ่อนจะผสมกับเกลือที่มีประจุลบเดียวกันกับกรด
ตัวอย่างเช่น พิจารณาสารละลายบัฟเฟอร์ที่ประกอบด้วยกรดอะซิติก (H3CCOOH(ที่นี่)) และโซเดียมอะซิเตท (H3CCOONa(ส)). เห็นว่าทั้งคู่มีประจุลบอะซิเตท: (H3CCOO-(ที่นี่)). ความเข้มข้นของไอออนเหล่านี้เกิดจากการแยกตัวของเกลือซึ่งมีขนาดใหญ่ กรดไอออไนซ์มีขนาดเล็ก

ตอนนี้ให้สังเกตว่าเกิดอะไรขึ้นในความเป็นไปได้เพิ่มเติมต่อไปนี้:
- การเติมกรดแก่จำนวนเล็กน้อย:
การเติมกรดแก่จะเพิ่มความเข้มข้นของไฮโดรเนียมไอออน H3โอ+1และเนื่องจากกรดอะซิติกเป็นกรดอ่อน แอนไอออนอะซิเตตจึงมีสัมพรรคภาพสูงสำหรับโปรตอน (H+) ไฮโดรเนียม ด้วยวิธีนี้ พวกมันจะทำปฏิกิริยาและเกิดกรดอะซิติกมากขึ้น:

เป็นผลให้ค่า pH ของตัวกลางไม่เปลี่ยนแปลง อย่างไรก็ตาม หากเติมกรดที่แรงมากขึ้นเรื่อยๆ เวลาจะมาถึงเมื่อประจุลบของอะซิเตตจะหมดลงและผลของบัฟเฟอร์จะหยุดลง
- เพิ่มฐานที่แข็งแกร่งจำนวนเล็กน้อย:
การเติมเบสแก่จะเพิ่มความเข้มข้นของไอออน OH-. แต่ไอออนเหล่านี้ถูกทำให้เป็นกลางโดยไอออน H3โอ+1 ถูกปล่อยออกมาจากการแตกตัวเป็นไอออนของกรดอะซิติก:

ด้วยปฏิกิริยานี้ความเข้มข้นของ H ไอออน3โอ+1(ที่นี่) จะลดลงและจะมีการเปลี่ยนแปลงในสมดุลในแง่ของการเพิ่มกรดไอออไนซ์ ดังนั้นความแปรผันของ pH ของสารละลายจะมีขนาดเล็กมาก ความเข้มข้นของไอออน H3โอ+1(ที่นี่) มันจะคงที่ในทางปฏิบัติ
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
ในกรณีนี้ยังมีขีดจำกัดความจุ ดังนั้น หากเราเติมเบสมากขึ้นเรื่อยๆ ความสมดุลของกรดไอออไนซ์ก็จะเปลี่ยนไปเป็นไอออไนซ์มากขึ้นเรื่อยๆ จนกว่ากรดจะหมดไป
2. ส่วนผสมของเบสอ่อนกับกรดคอนจูเกต:
สารละลายบัฟเฟอร์ประเภทนี้ประกอบด้วยเบสอ่อนและสารละลายเกลือที่มีไอออนบวกเดียวกันกับเบส
ตัวอย่างเช่น พิจารณาสารละลายบัฟเฟอร์ที่เกิดจากแมกนีเซียมไฮดรอกไซด์ MgOH2(aq) (เบสอ่อน) และแมกนีเซียมคลอไรด์ MgCl2(s) (เกลือ). ทั้งสองมีแมกนีเซียมไอออนบวก (Mg2+(ที่นี่)). ไอออนของแมกนีเซียมที่มีอยู่ในตัวกลางนั้นเกือบทั้งหมดได้มาจากการแยกตัวของเกลือ เนื่องจากการแยกตัวของเบสนั้นอ่อน:
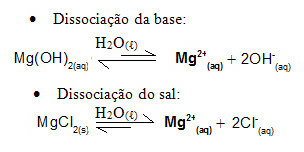
- การเติมกรดแก่จำนวนเล็กน้อย:
ในกรณีนี้ ไอออน H3โอ+1 จากการเติมกรดแก่จะทำให้เป็นกลางโดย OH ไอออน-มาจากการแตกตัวของเบสที่อ่อนแอ สิ่งนี้จะเปลี่ยนความสมดุลของการแยกฐานไปทางขวา
ดังนั้นค่า pH ที่แปรผัน (ถ้ามี) จะน้อยมาก เนื่องจากความเข้มข้นของ OH ions- คงที่ เอฟเฟกต์บัฟเฟอร์จะหยุดเมื่อแยกฐานทั้งหมดออก
- เพิ่มฐานที่แข็งแกร่งจำนวนเล็กน้อย:
ฐานที่แข็งแรงเพิ่มผ่านการแยกตัวออกโดยปล่อย OH ไอออน-. เนื่องจากแมกนีเซียมไฮดรอกไซด์เป็นเบสที่อ่อนแอ แมกนีเซียมที่ปล่อยออกมาจากการแยกตัวออกจากเกลือจะมีแนวโน้มที่จะทำปฏิกิริยากับ OH มากขึ้น-:

ดังนั้นการเพิ่มขึ้นของ OH ไอออน- ถูกชดเชยด้วยการเพิ่มขึ้นตามสัดส่วนใน Mg(OH)2(aq). เป็นผลให้ค่า pH ไม่ได้รับการเปลี่ยนแปลงที่สำคัญ
เอฟเฟกต์นี้จะสิ้นสุดลงเมื่อบริโภคแมกนีเซียมไอออนบวกทั้งหมด
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "สารละลายบัฟเฟอร์คืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/o-que-uma-solucao-tampao.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี

ทดสอบความรู้ของคุณและเรียนรู้เพิ่มเติมด้วยรายการแบบฝึกหัดที่แก้ไขแล้วเกี่ยวกับความสมดุลทางเคมี ด้วยเนื้อหานี้ คุณจะสามารถเข้าใจวิธีการทำงานของค่าคงที่สมดุล (Kp, Kc และ Ki) ได้ดีขึ้น การเลื่อนสมดุล pH และ pOH ตลอดจนสมดุลในสารละลายบัฟเฟอร์ที่เรียกว่า
โซลูชั่น โซลูชั่นที่เป็นของแข็ง สารละลายของเหลว สารละลายแก๊ส สารละลายที่เกิดจากแก๊สและของเหลว สารละลายที่เกิดจากของเหลว


