В текста "Заглавие или масов процент”Видяхме как да изчислим връзката между масата на разтвореното вещество и масата на разтвора за твърди, течни и газообразни разтвори. В този текст обаче ще видим, че е възможно също да се изчисли титърът по отношение на обема, за разтвори с течни или газообразни компоненти.

Заглавието в обем може да се изчисли чрез израза:
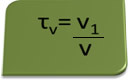
Да разгледаме като пример воден разтвор на етилов алкохол, използван като антисептик и дезинфектант, който е приготвя се чрез добавяне на 70 ml чист алкохол към достатъчно вода, за да се получи обем от 100 ml решение. Така че имаме:
τ = 70 мл = 0,7
100 мл
Можем да изразим заглавието и в проценти, просто умножавайки резултата по 100%. Така че в този случай имаме 70% разтвор на етилов алкохол, което означава, че от всеки 100 обемни единици от разтвора, 70 обемни единици са алкохол.
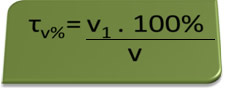
В случая по-долу имаме 70% разтвор на етилов алкохол в 250 ml обем разтвор; което означава, че 175 мл са алкохол, според изчисленията:
100 ml 70 ml алкохол
250 ml х
x = 70. 250
100
Х = 175 мл алкохол

Не можем обаче да кажем, че в този случай имаме 75 ml (250-175) вода. За разлика от масовия титър, при който можем да добавим масата на разтворителя към масата на разтвореното вещество, за да намерим масата на разтвора, това не може да се направи по отношение на обемния титър.

Това означава, че обемът на разтвора не е равен на сумата от обема на разтворителя и обема на разтвореното вещество (въпреки че често разликата може да се счита за незначителна). Това е така, защото междумолекулните сили, които съществуват в тези течности, влияят на крайния обем.
В случая на гореспоменатия разтвор, например етилов алкохол, когато смесваме алкохол с вода, има свиване на общия обем на разтвора; тоест крайният обем ще бъде по-малък, отколкото ако добавим обема само на алкохол и вода. Това е така, защото алкохолните молекули установяват връзки или водородни връзки с водните молекули, намалявайки пространствата между тях.
Следователно в този и други случаи обемът на разтвора трябва да бъде измерен експериментално, когато не е предвиден в упражнението.
Обемният процент се използва широко в случаите на алкохолни напитки и търговски алкохол, както бе споменато по-горе. Вижте две важни приложения на това изчисление:
- Алкотестер: алкотестерът измерва концентрацията на етилов алкохол в кръвта, а в Бразилия е забранено на всеки да управлява какъвто и да е тип превозно средство със съдържание на алкохол в кръвта, равно или по-голямо от 0,1% обемни. Човек с това алкохолно съдържание има за всеки литър кръв 1 мл алкохол, както е показано от следните изчисления:
τv%=V1. 100%
v
0,1 % = V1. 100%
1L
V1 = 0,1% → V1 = 0,001 L = 1 ml
100%

- Съдържание на етанол в бензина: в Бразилия бензинът се регулира чрез добавяне на етанол. Но съдържанието на етанол в бензина трябва да бъде най-много 24 обемни% безводен алкохол (тъй като бензинът трябва да е без вода). Колкото повече етанол се добавя към бензина, толкова повече цветът на горивото става по-светъл и плътността му се увеличава.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm

