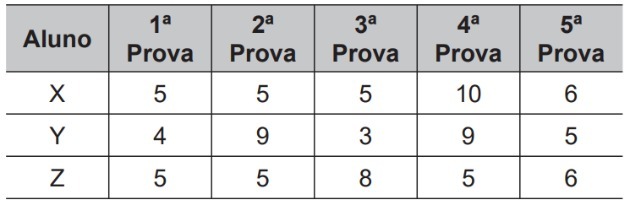
О балансиране на уравнения ни позволява да съпоставим броя на атомите, присъстващи в химичното уравнение, така че то да стане вярно и да представлява химична реакция.
Използвайте въпросите по-долу, за да проверите знанията си и да проверите отговорите, коментирани след обратната връзка, за да отговорите на вашите въпроси.
Въпрос 1
(Mackenzie-SP)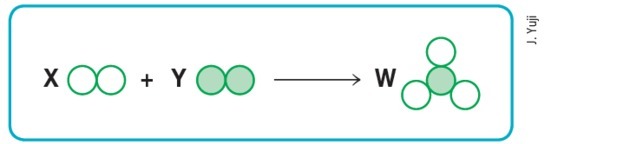
Ако приемем, че празните и запълнените кръгове съответно означават различни атоми, тогава схемата по-горе ще представлява балансирана химическа реакция, ако заменим буквите X, Y и W, съответно, с стойности:
а) 1, 2 и 3.
б) 1, 2 и 2.
в) 2, 1 и 3.
г) 3, 1 и 2.
д) 3, 2 и 2.
Алтернатива г) 3, 1 и 2.
1-ва стъпка: Присвояваме букви, за да улесним разбирането на уравнението.
2-ра стъпка: събираме индексите, за да разберем кой има най-много атоми в уравнението.
| НА | |
| Б. |
А и В се появяват само веднъж във всеки член на уравнението. Ако обаче добавим индексите, виждаме, че A има най-висока стойност. Затова започнахме балансирането за него.
3-та стъпка: Балансираме елемент А, като транспонираме индексите и ги превръщаме в коефициенти.
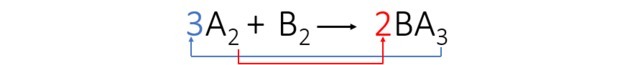
Забелязахме, че елемент В е автоматично балансиран и коефициентите на уравнението са: 3, 1 и 2.
въпрос 2
(Unicamp-SP) Прочетете следното изречение и го трансформирайте в (балансирано) химическо уравнение, като използвате символи и формули: „молекула газообразен азот, съдържаща два атома от азот на молекула, реагира с три молекули двуатомен газообразен водород, като произвежда две молекули газообразен амоняк, който се състои от три водородни атома и един от азот ".
Отговор:
Представяйки атомите, описани във въпроса, можем да разберем, че реакцията протича по следния начин:
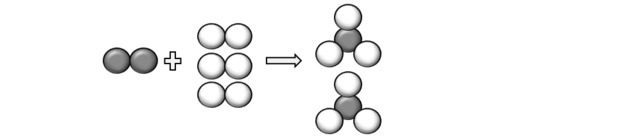
И така, стигаме до уравнението:
въпрос 3
Водородният пероксид е химично съединение, което може да се разложи, образувайки вода и кислород, съгласно химичното уравнение по-долу.
По отношение на тази реакция, правилно балансираното уравнение е:
а) Н2О2 → The2 + Н2О
б) 2 часа2О2 → The2 + 2Н2О
в) Н2О2 → 2O2 + Н2О
г) 2 часа2О2 → 2O2 + 2Н2О
Правилна алтернатива: б) 2Н2О2 → The2 + 2Н2О
Имайте предвид, че водородният прекис е химикал, съставен от атоми на два химични елемента: водород и кислород.
След реакцията на разлагане трябва да имате еднакъв брой атоми на двата елемента както в реагентите, така и в продуктите. За това трябва да балансираме уравнението.
Имайте предвид, че имаме 2 водородни атома в реагента (H2О2) и два атома в продукта (H2О). Въпреки това кислородът има два атома в реагента (Н2О2) и три атома в продуктите (H2O и O2).
Ако поставим коефициента 2 преди водородния прекис, удвояваме броя на атомите в елементите.
Имайте предвид, че ако сложим един и същ коефициент заедно с формулата за вода, ще имаме еднакво количество атоми от двете страни.
Следователно, правилно балансираното химично уравнение е 2Н2О2 → The2 + 2Н2О.
въпрос 4
(UFPE) Помислете за химичните реакции по-долу.
Можем да кажем, че:
а) всички са балансирани.
б) 2, 3 и 4 са балансирани.
в) балансирани са само 2 и 4.
г) само 1 е небалансиран.
д) никой не е правилно балансиран, тъй като физичните състояния на реагентите и продуктите са различни.
Алтернатива б) 2, 3 и 4 са балансирани.
Алтернативи 1 и 5 са неправилни, защото:
- Уравнение 1 е небалансирано, правилният баланс ще бъде:
- Уравнение 5 е неправилно, тъй като съединението, образувано в реакцията, би било Н2САМО3.
За образуване на H2САМО4 трябва да бъде включено в уравнението окисление на SO2.
въпрос 5
(Mackenzie-SP) Загрет до 800 ° C, калциевият карбонат се разлага на калциев оксид (необработена вар) и въглероден диоксид. Правилно балансираното уравнение, което съответства на описаното явление, е:
(Дадено: Ca - алкалноземен метал.)
Алтернатива в)
Калцият е алкалноземен метал и за да има стабилност калцият се нуждае от 2 електрона (Ca2+), което е зарядът на кислорода (O2-).
По този начин калциевият атом се свързва с кислороден атом и образуваното съединение е CaO, което е негасена вар.
Другият продукт е въглероден диоксид (CO2). И двете се образуват от калциев карбонат (CaCO3).
Поставяйки го в уравнение:
Отбелязваме, че количествата на атомите вече са правилни и не се нуждаят от балансиране.
въпрос 6
(UFMG) Уравнението не е балансиран. Балансирайки го с възможно най-малките числа, сумата от стехиометричните коефициенти ще бъде:
а) 4
б) 7
в) 10
г) 11
д) 12
Алтернатива д) 12
Използвайки пробния метод, редът за балансиране ще бъде:
1-ва стъпка: Тъй като елементът, който се появява само веднъж във всеки член и има най-висок индекс, е калций, започнахме да балансираме за него.
2-ра стъпка: Ние следваме балансирането от радикалния PO43-, който също се появява само веднъж.
3-та стъпка: балансираме водорода.
С това наблюдаваме, че автоматично се регулира количеството кислород и балансът на уравнението е:
Спомняйки си, че когато коефициентът е 1, не е нужно да го записвате в уравнението.
Добавяне на коефициентите, които имаме:
въпрос 7
Изгарянето е вид химическа реакция, при която енергията се отделя под формата на топлина.
При пълното изгаряне на вещество, образувано от въглерод и водород, се образуват въглероден диоксид и вода.
Наблюдавайте реакциите на горене на въглеводороди и отговорете кое от уравненията по-долу е неправилно балансирано:
а) СН4 + 2O2 → CO2 + 2Н2О
б) С3Н8 +502 → 3CO2 + 4Н2О
в) С4Н10 + 13 / 3O2 → 4CO2 + 5ч2О
г) С2Н6 + 7 / 2O2 → 2CO2 + 3Н2О
Неправилен отговор: в) В4Н10 + 13 / 3O2 → 4CO2 + 5ч2О
За да балансираме химическите уравнения, нека първо разгледаме кой елемент се появява само веднъж във всеки член на уравнението.
Имайте предвид, че въглеродът и водородът образуват само един реагент и един продукт във всяко представено уравнение.
Така че нека започнем да балансираме с водород, тъй като той има по-голям брой атоми.
Следователно редът на балансиране ще бъде:
- Водород
- Въглерод
- Кислород
Водород
Тъй като продуктът има 2 водородни атома, ние вмъкваме число като коефициент, умножен по 2, което води до броя на водородните атоми в реагента.
а) СН4 + O2 → CO2 + 2Н2О
б) С3Н8 + O2 → CO2 + 4Н2О
в) С4Н10 + O2 → CO2 + 5Н2О
г) С2Н6 + O2 → CO2 + 3Н2О
Въглерод
Балансирането се извършва чрез транспониране на въглеродния индекс в реагента и използването му като коефициент върху продукта, който има атоми на този елемент.
а) СН4 + O2 → 1CO2 + 2Н2О
б) С3Н8 + O2 → 3CO2 + 4Н2О
в) С4Н10 + O2 → 4CO2 + 5ч2О
г) С2Н6 + O2 → 2CO2 + 3Н2О
Кислород
Добавяйки броя на кислородните атоми в образуваните продукти, намираме броя на атомите на елемента, който трябва да реагира.
За това трябва да поставим като коефициент число, умножено по 2, което води до броя на кислородните атоми в продуктите.
а) СН4 + O2 → 1CO2 + 2Н2О
2x = 2 + 2
2x = 4
x = 2
Така че правилното уравнение е: CH4 + 2О2 → 1CO2 + 2Н2О.
б) С3Н8 + O2 → 3CO2 + 4Н2О
2x = 6 + 4
2x = 10
x = 5
Така че правилното уравнение е: C3Н8 + 5О2 → 3CO2 + 4Н2О
в) С4Н10 + O2 → 4CO2 + 5ч2О
2x = 8 + 5
2x = 13
x = 13/2
Така че правилното уравнение е: C4Н10 + 13/2О2 → 4CO2+ 5ч2О
г) С2Н6 + O2 → 2CO2 + 3Н2О
2x = 4 + 3
2x = 7
x = 7/2
Така че правилното уравнение е: C2Н6 + 7/2О2 → 2CO2 + 3Н2О
Правилно балансирани уравнения са:
а) СН4 + 2O2 → CO2 + 2Н2О
б) С3Н8 +502 → 3CO2 + 4Н2О
в) С4Н10 + 13 / 2O2 → 4CO2 + 5ч2О
г) С2Н6 + 7 / 2O2 → 2CO2 + 3Н2О
По този начин алтернатива в) В4Н10 + 13 / 3O2 → 4CO2 + 5ч2Работата е там, че няма правилния баланс.
въпрос 8
(Enem 2015) Варовиците са материали, съставени от калциев карбонат, които могат да действат като сорбенти за серен диоксид (SO2), важен замърсител на въздуха. Реакциите, участващи в процеса, са активиране на варовик чрез калциниране и фиксиране на SO2 с образуването на калциева сол, както е илюстрирано от опростените химични уравнения.
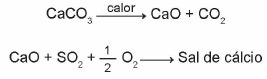
Имайки предвид реакциите, свързани с този процес на десулфуризация, химическата формула на калциевата сол съответства на:
Алтернатива б)
Тъй като реакцията е балансирана, атомите в реагентите трябва да бъдат в същото количество в продуктите. Поради това,
Образуваната сол се състои от:
1 калциев атом = Ca
1 серен атом = S
4 кислородни атома = O4
Следователно химическата формула на калциевата сол съответства на CaSO4.
въпрос 9
(UFPI) Реакцията на X с Y е показана по-долу. Определете кое уравнение най-добре представлява балансираното химично уравнение.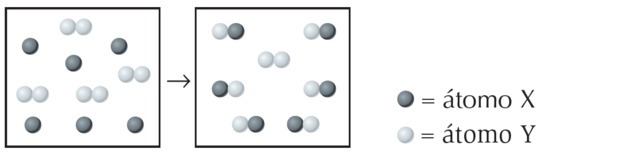
Алтернатива а)
На фигурата наблюдаваме, че видът X е единичен атом, докато Y е двуатомен, т.е. образува се чрез свързване на 2 атома. Така X реагира с Y2.
Образуваният продукт се представя с XY, като уравнението е небалансирано:
Балансираме уравнението, както следва:
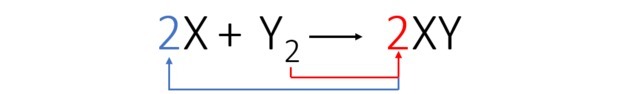
Според балансираното уравнение, фигурата по-долу ни показва как протича реакцията и нейното съотношение.
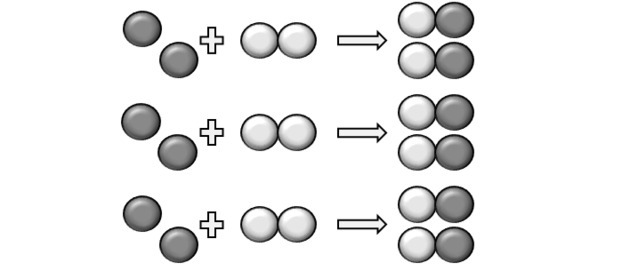
За да настъпи реакция, трябва да има фиксирано съотношение и следователно някои съединения може да не реагират. Това показва фигурата, защото в продукта виждаме, че Y2 не реагира.
въпрос 10
(Enem 2010) Мобилизациите за насърчаване на по-добра планета за бъдещите поколения са все по-чести. Понастоящем повечето средства за масов транспорт се захранват от изгаряне на изкопаеми горива. Като пример за тежестта, причинена от тази практика, е достатъчно да се знае, че една кола произвежда средно около 200 g въглероден диоксид на изминат км.
Списание за глобално затопляне. Година 2, 8. Публикация на Instituto Brasileiro de Cultura Ltda.
Една от основните съставки на бензина е октанът (C8Н18). Чрез изгарянето на октанова енергия е възможно, което позволява на колата да започне да се движи. Уравнението, което представлява химичната реакция на този процес, показва, че:
а) в процеса се отделя кислород под формата на О2.
б) стехиометричният коефициент за вода е 8 до 1 октан.
в) в процеса има потребление на вода, така че да се отделя енергия.
г) стехиометричният коефициент за кислород е 12,5 до 1 октан.
д) стехиометричният коефициент за въглероден диоксид е 9 до 1 октан
Алтернатива г) стехиометричният коефициент за кислород е 12,5 до 1 октан.
Когато балансираме уравнението, намираме следните коефициенти:
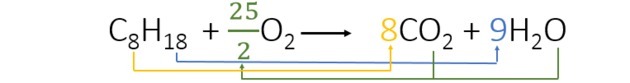
- Започнахме балансирането с водород, който се появява само веднъж във всеки член и има по-висок индекс. Тъй като има 18 реагиращи водородни атома, в продукта има 2, така че трябва да добавим число, умножено по 2, дава 18. Значи 9 е коефициентът.
- След това добавяме коефициента 8 пред CO2 да има 8 въглерода във всеки член на уравнението.
- И накрая, просто добавете количеството кислород в продукта и намерете стойността, умножена по 2, ни дава 25 кислородни атома. Така че избрахме 25/2 или 12.5.
По този начин за изгарянето на 1 октан се изразходва 12,5 кислорода.
въпрос 11
(Fatec-SP) Съществена характеристика на торовете е тяхната разтворимост във вода. Следователно торовата индустрия превръща калциевия фосфат, чиято разтворимост във вода е много ниска, в много по-разтворимо съединение, което е калциев суперфосфат. Този процес е представен от уравнението:
където стойностите на x, y и z са съответно:
а) 4, 2 и 2.
б) 3, 6 и 3.
в) 2, 2 и 2.
г) 5, 2 и 3.
д) 3, 2 и 2.
Алтернатива д) 3, 2 и 2.
Използвайки алгебричния метод, ние формираме уравнения за всеки елемент и изравняваме броя на атомите в реагента с броя на атомите в продукта. Следователно:
Балансирано уравнение:
въпрос 12
Балансирайте уравненията по-долу, като използвате пробния метод.
Отговор:
Уравнението се състои от елементите водород и хлор. Балансираме елементите само като добавим коефициент 2 пред продукта.
Не е необходимо уравнението да бъде балансирано, тъй като количествата на атомите вече са коригирани.
Фосфорът има два атома в реагентите, така че за да балансираме този елемент, ние регулираме количеството фосфорна киселина в продукта до 2Н3ПРАХ4.
След това забелязахме, че водородът има 6 атома в продукта, балансирахме количеството на този елемент, добавяйки коефициент 3 към реагента, който го съдържа.
С предишните стъпки количеството кислород беше коригирано.
Разглеждайки уравнението, виждаме, че количествата водород и бром в продуктите са двойно повече от това ако има в реагентите, добавяме коефициент 2 към HBr, за да балансираме тези два елементи.
Хлорът има 3 атома в продуктите и само 1 в реагентите, така че балансираме, поставяйки коефициент 3 преди HCl.
Водородът има 3 атома в реагентите и 2 атома в продуктите. За да коригираме количествата, трансформираме H индекса2 в коефициент умножаваме по 3, което вече беше в HCl и получаваме резултата от 6HCl.
Регулираме количествата хлор в продуктите, за да имаме също 6 атома и получаваме 2AlCl3.
Алуминият имаше 2 атома в продуктите, коригирахме количеството в реагентите на 2Al.
Балансираме количеството водород в продукта до 3Н2 и побираме количеството от 6 атома на този елемент във всеки член на уравнението.
В уравнението нитратният радикал (NO3-) има индекс 2 в продукта, ние трансформираме индекса в коефициент в реагента за 2AgNO3.
Количеството сребро трябваше да се коригира, тъй като сега има 2 атома в реактивите, така че имаме 2Ag в продукта.
В реагентите имаме 4 водородни атома и за балансиране на този елемент добавяме коефициент 2 към HCl продукта.
Хлорът вече има 4 атома в продуктите, така че регулираме количеството в реагента на 2Cl2.
Имаме 6 водородни атома в реагентите и за да балансираме този елемент, регулираме количеството вода до 3H2О.
Имаме 2 въглеродни атома в реагентите и за да балансираме този елемент, регулираме количеството въглероден диоксид на 2CO2.
Кислородът трябва да има 7 атома в реагентите и за да балансираме този елемент, ние регулираме количеството молекулен кислород на 302.
Разглеждайки уравнението, нитратният радикал (NO3-) има индекс 2 в продукта. Ние трансформираме индекса в коефициент 2 в реагента AgNO3.
Имаме 2 сребърни атома в реагентите и за да балансираме този елемент, регулираме количеството сребърен хлорид в продукта до 2AgCl.
Имаме 3 калциеви атома в продукта и за да балансираме този елемент, регулираме количеството калциев нитрат в реагента на 3Ca (NO3)2.
След това ни остават 6 NO радикали3- в реагентите и за да балансираме този радикал, регулираме количеството азотна киселина в продуктите до 6HNO3.
Сега имаме 6 водородни атома в продуктите и за да балансираме този елемент, регулираме количеството фосфорна киселина в реагента на 2Н3ПРАХ4.
Научете повече за изчисленията с химични уравнения на адрес:
- Балансиране на химични уравнения
- Стехиометрия
- Стехиометрични изчисления
- Упражнения за стехиометрия
- Упражнения за периодична таблица