Въглеродът е химичен елемент с атомно число (Z), равно на 6, което означава, че атомите, които го образуват, имат в ядрото си шест протона. Моларната му маса е 12011 g / mol и в природата се откриват три изотопа на въглерода, които са: o въглерод-12, въглерод-13 и въглерод-14. С-12 има шест протона и шест неутрона в ядрото и е най-разпространен.
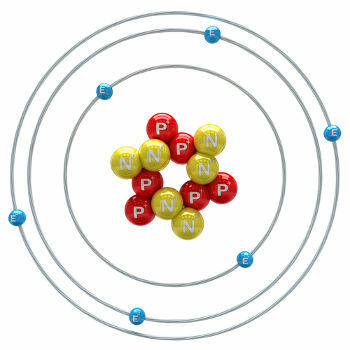
въглероден атом-12 илюстрация
C-13 има седем неутрона и е най-слабо разпространен (1,01 до 1,14%). C-14 има осем неутрона и е a радиоактивен елемент който излъчва β частици (електрони), образуващи се в стратосферата на Земята, когато неутроните на космическите лъчи бомбардират азота-14, присъстващ в тези горни слоеве на атмосферата. Той е включен от всички растения и животни и, знаейки, че неговият полуживот е около 5730 години, се използва за определяне на възрастта на вкаменелостите между 100 и 40 000 години. Повече подробности за C-14 и техниката за запознанства можете да видите в текста. Какво е въглерод-14?
Въглеродът е четиривалентен, тоест той се нуждае от още четири протона във своя валентен слой (най-външния слой), за да се подчинява на правилото на октета. Следователно, той обикновено прави четири ковалентни връзки, споделяйки четири двойки електрони с други елементи, както и с други въглероди. Тези връзки могат да бъдат единични, двойни или тройни и да доведат до образуването на милиони различни съединения. Поради тази причина е създадена област на химията,
Органична химия, който изучава основните съединения, получени от въглерод, с изключение на някои случаи, които са с минерален произход, като например въглероден диоксид (CO2), О въглероден оксид (CO), О калциев карбонат (CaCO3), натриев хидроген карбонат или натриев бикарбонат (NaHCO3), между други. Тези съединения са изследвани в Неорганична химия.Въглеродът извършва алотропия, образувайки прости вещества, т.е. вещества, които се образуват само от връзки между въглеродните атоми. Има най-малко седем алотропи на въглерод, които са графит (алфа и бета), диамант, лонсдалит (шестоъгълен диамант), хаоит, въглерод (VI) и фулерени. Всъщност има няколко вида фулерени, които са синтетични алотропни форми на въглерод. Те имат полиедрична структура с въглероден атом във всеки връх и пример е ° С60 Наречен buckminsterfullerene, а структурата му прилича на футболна топка.
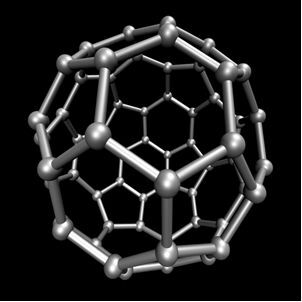
Въглерод-60 (buckminsterfullerene)
Сред тези алотропи на въглерода обаче има само два, които са естествени. графитЕ от Диамант. Те се различават само по кристалното разположение на атомите в пространството, както е показано на фигурата по-долу, и това води до напълно различни физикохимични свойства. Прочети текста въглеродна алотропия за повече информация.

Двете естествени алотропни форми на въглерод са графит и диамант.
Друга синтетична алотропна форма на въглерод е нанотръби (изображението по-долу), които имат широко биологично приложение, включително медицинска диагностика и лечение.

Илюстрация на микроскопична въглеродна нанотръба
Поради това, въглеродът присъства във всичко около нас и в нас, защото той композира естествени органични съединения - като изкопаеми горива, които включват нефт, въглища и природен газ и други горива като етанол и биогорива - селскостопански продукти, наред с други. форма също синтетични органични съединения, като синтетични влакна, които съставляват тъкани, лекарства, полимери, които съставляват пластмаси и каучуци, инсектициди, багрила и много други. В нас, животните и зеленчуците, въглеродът образува много важни съединения, като въглехидрати, като захар, глюкоза и целулоза; протеините, които образуват например ДНК и заедно с липидите образуват мембраните на червените кръвни клетки и белите кръвни клетки.
Всичко това показва значението на въглерода за поддържането на живота. Но това е свързано и с негативни аспекти, като засилването на парников ефект и последващото глобално затопляне, това е така, защото основният злодей на тези проблеми е неговото въглеродно диоксидно съединение (CO2). Главно поради голямото изгаряне на изкопаеми горива, които отделят този газ, концентрацията на CO2 в атмосферата се е увеличил. Като парников газ причинява гореспоменатите проблеми. От друга страна, въглеродният диоксид присъства и в жизненоважни реакции като фотосинтеза и дишане.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm