แบตเตอรี่ เป็นอุปกรณ์ที่ผลิตกระแสไฟฟ้าจากพลังงานเคมีที่มาจาก a ปฏิกิริยาออกซิเดชันนั่นคือสารตั้งต้นชนิดหนึ่งสูญเสียอิเล็กตรอน (ออกซิเดชัน) ในขณะที่อีกชนิดหนึ่งได้รับอิเล็กตรอน (ลดลง)
ดูการแสดงแทนปฏิกิริยาออกซิเดชันและการรีดักชันที่เกิดขึ้นในกองใดๆ:
ออกซิเดชัน: X → และ + X+
สปีชี่ X สูญเสียอิเล็กตรอนและกลายเป็นไอออนบวก
ลด: Y- + และ → Y
ไอออน Y Y- รับอิเล็กตรอนและเปลี่ยนเป็นสปีชีส์ Y ที่เป็นกลาง
ส่วนประกอบพื้นฐานของ stack
องค์ประกอบพื้นฐานของสแต็กคือ:
แอโนด: อิเล็กโทรดลบที่เกิดปฏิกิริยาออกซิเดชันนั่นคือการสูญเสียอิเล็กตรอน
แคโทด: อิเล็กโทรดบวกที่เกิดปฏิกิริยารีดักชัน นั่นคือ การเพิ่มของอิเล็กตรอน
สารละลายอิเล็กโทรไลต์ (สะพานเกลือ) หรือวัสดุนำไฟฟ้า (เช่น แท่งกราไฟท์): เป็นวิธีที่อิเลคตรอนที่แอโนดมอบให้ไปถึงแคโทด
พื้นฐานการทำงานของแบตเตอรี่
การทำงานของสแต็กเกิดขึ้นจากเหตุการณ์ต่อไปนี้:
หลักการที่ 1: แอโนดออกซิเดชัน
โลหะในแอโนดเนื่องจากมีแนวโน้มที่จะสูญเสียอิเล็กตรอนมากขึ้น กลายเป็นไอออนบวก ดังที่เราสังเกตในสมการด้านล่าง:
สังกะสี → Zn2+ + 2 และ
หลักการที่ 2: ลดแคโทด
ไอออนบวกที่เป็นส่วนหนึ่งของวัสดุที่มีอยู่ในแคโทด (เราจะใช้ทองแดงเป็นตัวอย่าง) เมื่อได้รับ อิเล็กตรอนจากแอโนดเปลี่ยนเป็นทองแดงโลหะ ดังที่เราเห็นในสมการ ร้อง:
ตูด2+ + 2e → Cu
กองแรก
ก) แบตเตอรี่ของ Alessandro Volta
กองหลังของอเลสซานโดร (กองแรกในประวัติศาสตร์) ที่ประกอบขึ้นในปี ค.ศ. 1800 ถูกสร้างขึ้นโดยแผ่นโลหะที่มีการสอดประสาน ดังภาพด้านล่าง:

การประกอบที่คล้ายกับ Alessandro's Back to your pile
แผ่นดิสก์ถูกสอดแทรกเนื่องจากมีองค์ประกอบต่างกัน อันหนึ่งทำจากโลหะสังกะสี และอีกอันทำจากทองแดง โดยแยกจากผ้าฝ้ายที่แช่ในน้ำเกลือเสมอ (สารละลายที่เกิดจากน้ำและเกลือ)
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
ข) กองของแดเนียล
กองของแดเนียลซึ่งประกอบขึ้นในปี พ.ศ. 2379 ประกอบด้วยเซลล์ครึ่งเซลล์สองเซลล์ที่เชื่อมต่อกันด้วยลวดนำไฟฟ้าและสะพานเกลือ
ครึ่งเซลล์ 1: มันคือขั้วบวก นั่นคือ ขั้วลบของแบตเตอรี่
ประกอบด้วยแผ่นสังกะสี และส่วนหนึ่งของจานนี้ถูกแช่ในสารละลายที่เกิดจากน้ำและซิงค์ซัลเฟต (ZnSO4).
ครึ่งเซลล์ 2: มันคือแคโทด นั่นคือ ขั้วบวกของแบตเตอรี่
ประกอบด้วยแผ่นทองแดง และส่วนหนึ่งของแผ่นนี้ถูกจุ่มลงในสารละลายที่เกิดจากน้ำและคอปเปอร์ซัลเฟต (CuSO4).
สะพานเกลือ
หลอดรูปตัวยูที่มีสารละลายที่เกิดจากน้ำและโพแทสเซียมคลอไรด์ (KCl) ซึ่งเชื่อมต่อครึ่งเซลล์ทั้งสอง (สังกะสีและทองแดง) และมีใยแก้วที่ปลายทั้งสอง
แบตเตอรี่ในปัจจุบัน
ขณะนี้มีสแต็คหลายรุ่น แต่โดยทั่วไปแล้วจะมีลักษณะดังนี้:
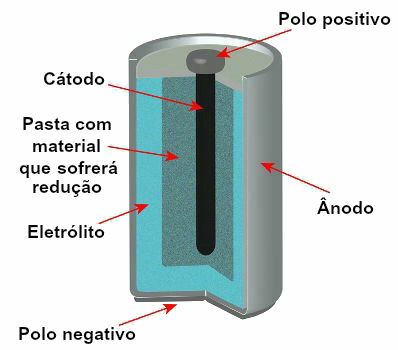
แผนผังแสดงแบบจำลองของสแต็กปัจจุบัน
รุ่นที่ใช้มากที่สุดคือแบตเตอรี่ที่เรียกว่า Leclanche และแบตเตอรี่อัลคาไลน์ ซึ่งมีความแตกต่างดังต่อไปนี้:
ก) Leclanche กอง
มีแอโนดที่เกิดจากสังกะสีโลหะ
มีแคโทดที่เกิดจากการวางด้วยแอมโมเนียมคลอไรด์ น้ำ แป้ง และแมงกานีสไดออกไซด์
มีแถบกราไฟท์ที่ทำหน้าที่เป็นตัวนำสำหรับอิเล็กตรอนที่ออกจากแคโทดไปทางแอโนด
ข) แบตเตอรี่อัลคาไลน์
มีแอโนดที่เกิดจากสังกะสีหรือแคดเมียมเป็นโลหะ
มีแคโทดที่เกิดจากปรอทออกไซด์ นิกเกิลออกไซด์และไอโอดีน
จะต้องมีฐานผสมในวัสดุที่ประกอบเป็นแคโทด
By Me. ดิโอโก้ โลเปส ดิอาส
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "แบตเตอรี่คืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-pilha.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.