พันธะไอออนิกเกิดขึ้นระหว่างไอออนตามชื่อของมัน เนื่องจากมีประจุตรงข้ามกัน ไอออนบวก (องค์ประกอบที่มีประจุบวก) และแอนไอออน (องค์ประกอบที่มีประจุลบ) จะดึงดูดกันด้วยไฟฟ้าสถิต ทำให้เกิดพันธะ อย่างไรก็ตาม ของแข็งไอออนิกประกอบด้วยการรวมตัวของไพเพอร์และแอนไอออนที่รวมตัวกันด้วยรูปทรงเรขาคณิตที่กำหนดไว้อย่างดี เรียกว่าแลตทิซหรือแลตทิซผลึก
ตัวอย่างเช่น เกลือ (โซเดียมคลอไรด์) เกิดขึ้นจากการถ่ายโอนอิเล็กตรอนจากโซเดียมไปยังคลอรีนขั้นสุดท้าย ทำให้เกิดโซเดียมไอออนบวก (Na+) และคลอไรด์ไอออน (Cl-). ในทางปฏิบัติ ปฏิกิริยานี้ไม่ได้เกี่ยวข้องกับอะตอมเพียงสองอะตอมเท่านั้น แต่ยังรวมถึงอะตอมจำนวนมหาศาลและไม่ทราบแน่ชัดซึ่งก่อตัวเป็นโครงผลึกรูปลูกบาศก์ ดังที่แสดงด้านล่าง:
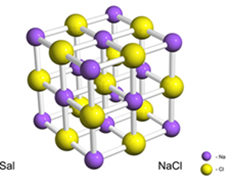
ถ้าเราดูที่ผลึกเกลือด้วยกล้องจุลทรรศน์อิเล็กตรอนแบบส่องกราด เราจะเห็นว่ามันเป็นลูกบาศก์จริงๆ เนื่องจากโครงสร้างภายในของพวกมัน

เนื่องจากสารประกอบไอออนิกทุกตัวประกอบด้วยไอออนที่ไม่แน่นอนและมีจำนวนมาก เราจะแสดงสารประกอบไอออนิกได้อย่างไร
สูตรที่มักใช้คือ สูตรหน่วยซึ่งก็คือตัวที่ แสดงถึงสัดส่วนที่แสดงโดยจำนวนไอออนบวกและแอนไอออนที่น้อยที่สุดที่เป็นไปได้ที่ประกอบเป็นผลึกขัดแตะ เพื่อให้ประจุทั้งหมดของสารประกอบเป็นกลาง
. เพื่อให้สิ่งนี้เกิดขึ้นได้ จำเป็นที่จำนวนอิเล็กตรอนที่อะตอมมอบให้ต้องเท่ากับจำนวนอิเล็กตรอนที่อะตอมอื่นได้รับลักษณะบางประการเกี่ยวกับสูตรหน่วยของสารประกอบไอออนิกมีความสำคัญ ดูบางส่วน:
- เขียนประจุบวกก่อนเสมอจากนั้นจึงตามด้วยประจุลบ
- เนื่องจากสารประกอบไอออนิกทุกตัวมีความเป็นกลางทางไฟฟ้า จึงไม่จำเป็นต้องเขียนประจุไอออนแต่ละตัว
- หมายเลขตัวห้อยที่ปรากฏทางด้านขวาของแต่ละไอออนระบุอัตราส่วนของอะตอมของไอออนบวกต่อประจุลบ ตัวเลขเหล่านี้เรียกว่าดัชนีและไม่ได้เขียนหมายเลข 1
ตัวอย่างเช่น ในกรณีของโซเดียมคลอไรด์ เรามีสูตรหน่วยของมันคือ NaCl เนื่องจากเรามีโซเดียมไอออนบวก 1 ตัวสำหรับแอนไอออนของคลอไรด์แต่ละตัว
ดูตัวอย่างอื่น Al3+ มีประจุบวกสามประจุ ในขณะที่ F- มันมีประจุลบเพียงตัวเดียว ดังนั้นจำเป็นต้องมีแอนไอออนฟลูออไรด์สามตัวเพื่อทำให้สารประกอบเป็นกลาง ดังนั้นเราจึงสรุปได้ว่าสูตรหน่วยของมันคือ AlF3.
วิธีง่ายๆ ในการหาสูตรหน่วยของสารประกอบไอออนิกคือ การแลกเปลี่ยนประจุเป็นค่าดัชนี ดังที่แสดงไว้ในวิธีทั่วไปด้านล่าง:
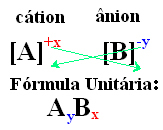
ตัวอย่าง:

อีกสูตรหนึ่งที่ใช้แทนสารไอออนิกคือ สูตรลูอิส หรือ สูตรอิเล็กทรอนิกส์, อะไร หมายถึงอิเล็กตรอนจากเปลือกความจุของไอออน "ลูก" รอบสัญลักษณ์ธาตุ ในกรณีของเกลือ เรามี:

โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/formulas-para-representar-as-ligacoes-ionicas.htm