สารต่างๆ ที่มีอยู่ในจักรวาลประกอบด้วยอะตอม ไอออน หรือโมเลกุล องค์ประกอบทางเคมีรวมกันผ่านพันธะเคมี ลิงค์เหล่านี้สามารถ:
| พันธะโควาเลนต์ | พันธะไอออนิก | การเชื่อมต่อโลหะ |
|---|---|---|
การแบ่งปันอิเล็กตรอน |
การถ่ายโอนอิเล็กตรอน |
ระหว่างอะตอมของโลหะ |
ใช้คำถามด้านล่างเพื่อทดสอบความรู้เกี่ยวกับพันธะเคมี
แบบฝึกหัดที่เสนอ
คำถามที่ 1
ในการตีความคุณสมบัติของสารต่าง ๆ จำเป็นต้องรู้พันธะระหว่างอะตอมและพันธะระหว่างโมเลกุลที่เกี่ยวข้อง เกี่ยวกับพันธะระหว่างอะตอม อาจกล่าวได้ว่า...
(A) ระหว่างอะตอมที่ถูกยึดเหนี่ยวแรงดึงดูดมีชัยเหนือกว่า
(B) เมื่อเกิดพันธะระหว่างอะตอม ระบบที่ก่อตัวขึ้นจะมีพลังงานสูงสุด
(C) แรงดึงดูดและแรงผลักของโมเลกุลไม่ได้เป็นเพียงไฟฟ้าสถิตในธรรมชาติเท่านั้น
(D) ระหว่างอะตอมที่ถูกผูกไว้มีความสมดุลระหว่างแรงดึงดูดของไฟฟ้าสถิตและการผลัก
ทางเลือกที่ถูกต้อง: (D) ระหว่างอะตอมที่ถูกผูกไว้มีความสมดุลระหว่างแรงดึงดูดของไฟฟ้าสถิตและการขับไล่
อะตอมเกิดขึ้นจากประจุไฟฟ้าและเป็นแรงไฟฟ้าระหว่างอนุภาคที่นำไปสู่การก่อตัวของพันธะ ดังนั้นพันธะเคมีทั้งหมดจึงมีลักษณะเป็นไฟฟ้าสถิต
อะตอมมีกองกำลังของ:
- แรงผลักระหว่างนิวเคลียส (ประจุบวก);
- แรงผลักระหว่างอิเล็กตรอน (ประจุลบ);
- แรงดึงดูดระหว่างนิวเคลียสและอิเล็กตรอน (ประจุบวกและประจุลบ)
ในระบบเคมีทั้งหมด อะตอมพยายามที่จะมีเสถียรภาพมากขึ้นและเกิดความเสถียรนี้ในพันธะเคมี
ความเสถียรเกิดจากความสมดุลระหว่างแรงดึงดูดและแรงผลัก เนื่องจากอะตอมมีสถานะพลังงานต่ำกว่า
คำถาม2
จับคู่ประโยคในคอลัมน์ I และประเภทการเชื่อมโยงในคอลัมน์ II ให้ถูกต้อง
| ผม | II |
|---|---|
| (A) ระหว่างนาอะตอม | 1. พันธะโควาเลนต์เดี่ยว |
| (B) ระหว่างอะตอม Cl | 2. พันธะโควาเลนต์คู่ |
| (C) ระหว่างอะตอมของ O | 3. การเชื่อมต่อโลหะ |
| (D) ระหว่าง N อะตอม | 4. พันธะไอออนิก |
| (E) ระหว่าง Na และ Cl อะตอม | 5. พันธะโควาเลนต์สามตัว |
ตอบ:
อะตอม |
ประเภทการเชื่อมต่อ |
การเป็นตัวแทน |
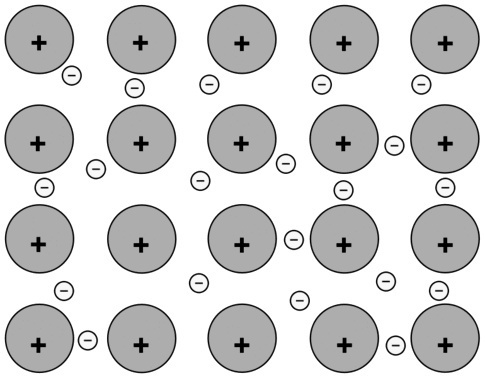
(A) ระหว่างนาอะตอม |
การเชื่อมต่อด้วยโลหะ อะตอมของโลหะนี้เชื่อมโยงกันผ่านพันธะโลหะ และปฏิกิริยาระหว่างประจุบวกและประจุลบจะเพิ่มความเสถียรของเซต |
 |
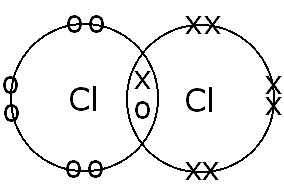
(B) ระหว่างอะตอม Cl |
พันธะโควาเลนต์เดี่ยว การแบ่งอิเล็กตรอนและการเกิดพันธะเดี่ยวเกิดขึ้นเพราะมีอิเล็กตรอนพันธะคู่เดียว |
 |
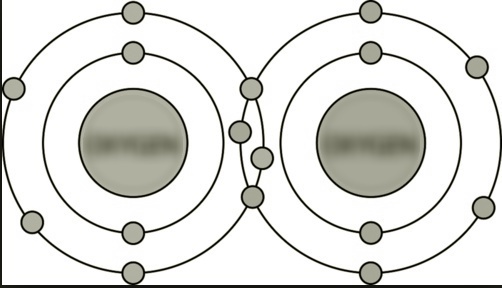
(C) ระหว่างอะตอมของ O |
พันธะโควาเลนต์คู่ มีอิเล็กตรอนพันธะสองคู่ |
 |
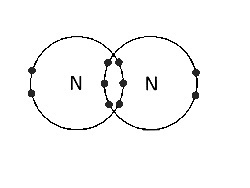
(D) ระหว่าง N อะตอม |
พันธะโควาเลนต์สามชั้น มีอิเล็กตรอนพันธะสามคู่ |
 |
(E) ระหว่าง Na และ Cl อะตอม |
พันธะไอออนิก เกิดขึ้นระหว่างไอออนบวก (ไพเพอร์) และไอออนลบ (แอนไอออน) ผ่านการถ่ายโอนอิเล็กตรอน |
 |
คำถาม 3
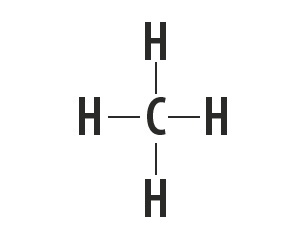
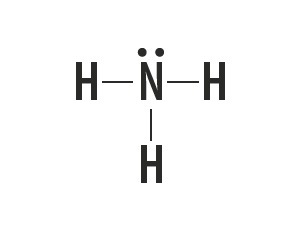
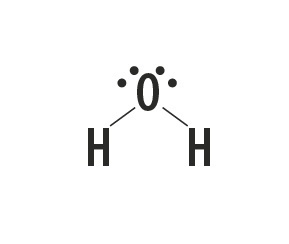
มีเทน แอมโมเนีย น้ำ และไฮโดรเจนฟลูออไรด์เป็นสารโมเลกุลที่มีโครงสร้างลูอิสแสดงในตารางต่อไปนี้
| มีเทน CH4 | แอมโมเนีย NH3 | น้ำ H2อู๋ | ไฮโดรเจนฟลูออไรด์ HF |
|---|---|---|---|
 |
 |
 |
 |
ระบุประเภทของพันธะที่สร้างขึ้นระหว่างอะตอมที่ประกอบเป็นโมเลกุลเหล่านี้
คำตอบที่ถูกต้อง: พันธะโควาเลนต์อย่างง่าย
เมื่อดูจากตารางธาตุจะเห็นว่าธาตุที่ไม่ใช่โลหะ
ประเภทของพันธะที่องค์ประกอบเหล่านี้ก่อตัวระหว่างพวกมันคือพันธะโควาเลนต์เนื่องจากพวกมันใช้อิเล็กตรอนร่วมกัน
อะตอมของคาร์บอน ไนโตรเจน ออกซิเจน และฟลูออรีนประกอบขึ้นเป็นอิเล็กตรอนแปดตัวในเปลือกเวเลนซ์เนื่องจากจำนวนของพันธะที่พวกมันสร้างขึ้น จากนั้นพวกเขาก็ปฏิบัติตามกฎออคเต็ต
ในทางกลับกัน ไฮโดรเจนมีส่วนร่วมในการก่อตัวของสารโมเลกุลโดยการแบ่งปันอิเล็กตรอนคู่หนึ่ง ทำให้เกิดพันธะโควาเลนต์อย่างง่าย
ดูด้วย: พันธะเคมี
คำถามสอบเข้า
คำถามเกี่ยวกับพันธะเคมีมักเกิดขึ้นในการสอบเข้าวิทยาลัย ดูด้านล่างว่าสามารถเข้าถึงหัวข้อได้อย่างไร
คำถามที่ 1
(UEMG) คุณสมบัติที่แสดงโดยวัสดุบางชนิดสามารถอธิบายได้ด้วยประเภทของพันธะเคมีที่มีอยู่ระหว่างหน่วยการขึ้นรูป ในการวิเคราะห์ในห้องปฏิบัติการ นักเคมีได้ระบุคุณสมบัติต่อไปนี้สำหรับวัสดุบางชนิด:
- อุณหภูมิหลอมเหลวและเดือดสูง
- การนำไฟฟ้าที่ดีในสารละลายที่เป็นน้ำ
- ตัวนำไฟฟ้าโซลิดสเตตไม่ดี
จากคุณสมบัติที่แสดงโดยวัสดุนี้ ให้ทำเครื่องหมายทางเลือกที่ระบุประเภทการเชื่อมต่อที่เด่นในนั้น:
(A) เมทัลลิก
(B) โควาเลนต์
(C) ไดโพลเหนี่ยวนำ
(D) อิออน
ทางเลือกที่ถูกต้อง: (D) อิออน
วัสดุที่เป็นของแข็งมีอุณหภูมิหลอมเหลวและจุดเดือดสูง กล่าวคือ จะต้องใช้พลังงานจำนวนมากเพื่อเปลี่ยนเป็นสถานะของเหลวหรือก๊าซ
ในสถานะของแข็ง วัสดุเป็นตัวนำไฟฟ้าที่ไม่ดี เนื่องจากการเรียงตัวของอะตอมที่สร้างรูปทรงเรขาคณิตที่กำหนดไว้อย่างดี
เมื่อสัมผัสกับน้ำ ไอออนจะปรากฏขึ้น ก่อตัวเป็นไพเพอร์และแอนไอออน ซึ่งช่วยให้กระแสไฟฟ้าไหลผ่านได้สะดวก
ประเภทของพันธะที่ทำให้วัสดุมีคุณสมบัติเหล่านี้คือพันธะไอออนิก
คำถาม2
(PUC-SP) วิเคราะห์คุณสมบัติทางกายภาพในตารางด้านล่าง:
| ตัวอย่าง | จุดหลอมเหลว | จุดเดือด | การนำไฟฟ้าที่ 25°C | การนำไฟฟ้าที่ 1,000 °C |
|---|---|---|---|---|
| THE | 801°C | 1413°C | ฉนวน | ตัวนำ |
| บี | 43°C | 182 °C | ฉนวน | |
| ค | 1535 °C | 2760°C | ตัวนำ | ตัวนำ |
| ดี | 1248°C | 2250 °C | ฉนวน | ฉนวน |
ตามแบบจำลองพันธะเคมี A, B, C และ D สามารถจำแนกได้เป็น
(A) สารประกอบไอออนิก, โลหะ, สารโมเลกุล, โลหะ.
(B) โลหะ สารประกอบไอออนิก สารประกอบไอออนิก สารโมเลกุล
(C) สารประกอบไอออนิก, สารโมเลกุล, โลหะ, โลหะ.
(ง) สารโมเลกุล สารประกอบไอออนิก สารประกอบไอออนิก โลหะ
(E) สารประกอบไอออนิก สารโมเลกุล โลหะ สารประกอบไอออนิก
ทางเลือกที่ถูกต้อง: (E) สารประกอบไอออนิก สารโมเลกุล โลหะ สารประกอบไอออนิก
การวิเคราะห์สถานะทางกายภาพของตัวอย่างเมื่ออยู่ภายใต้อุณหภูมิที่นำเสนอ เราต้อง:
| ตัวอย่าง | สภาพร่างกายที่ 25°C | สภาพร่างกายที่ 1,000 ° C | การจำแนกประเภทของสารประกอบ |
| THE | แข็ง | ของเหลว | อิออน |
| บี | แข็ง | โมเลกุล | |
| ค | แข็ง | แข็ง | โลหะ |
| ดี | แข็ง | แข็ง | อิออน |
สารประกอบ A และ D ทั้งสองเป็นฉนวนในสถานะของแข็ง (ที่อุณหภูมิ 25 °C) แต่เมื่อตัวอย่าง A เปลี่ยนเป็นสถานะของเหลว สารดังกล่าวจะกลายเป็นสื่อกระแสไฟฟ้า เหล่านี้เป็นลักษณะของสารประกอบไอออนิก
สารประกอบไอออนิกแบบโซลิดสเตตไม่อนุญาตให้นำไฟฟ้าเนื่องจากอะตอมจัดเรียงตัวกันเอง
ในสารละลาย สารประกอบไอออนิกจะเปลี่ยนเป็นไอออนและปล่อยให้กระแสไฟฟ้าไหลผ่านได้
เป็นคุณลักษณะของโลหะที่มีการนำไฟฟ้าที่ดีเช่นตัวอย่าง C
สารประกอบโมเลกุลเป็นกลางทางไฟฟ้า กล่าวคือ ลูกถ้วยเช่นตัวอย่าง B
ดูด้วย: ลิงค์โลหะ
คำถาม 3
(Fuvest) พิจารณาองค์ประกอบของคลอรีนที่ก่อตัวเป็นสารประกอบที่มีไฮโดรเจน คาร์บอน โซเดียมและแคลเซียมตามลำดับ คลอรีนสร้างสารประกอบโควาเลนต์ด้วยธาตุใดต่อไปนี้
ตอบ:
| องค์ประกอบ | การโทรเกิดขึ้นได้อย่างไร | พันธะที่เกิดขึ้น | |
| คลอรีน | ไฮโดรเจน | 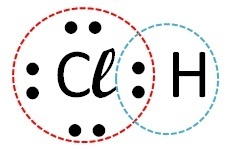 |
โควาเลนต์ (การแบ่งอิเล็กตรอน) |
| คลอรีน | คาร์บอน | 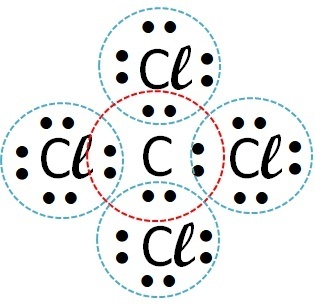 |
โควาเลนต์ (การแบ่งอิเล็กตรอน) |
| คลอรีน | โซเดียม |  |
อิออน (การถ่ายโอนอิเล็กตรอน) |
| คลอรีน | แคลเซียม | 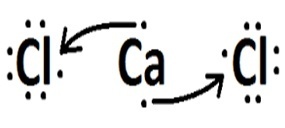 |
อิออน (การถ่ายโอนอิเล็กตรอน) |
สารประกอบโควาเลนต์เกิดขึ้นในอันตรกิริยาของอะตอมที่ไม่ใช่โลหะ อโลหะกับไฮโดรเจนหรือระหว่างอะตอมของไฮโดรเจนสองอะตอม
ดังนั้นพันธะโควาเลนต์จึงเกิดขึ้นกับคลอรีน + ไฮโดรเจน และคลอรีน + คาร์บอน
โซเดียมและแคลเซียมเป็นโลหะและพันธะกับคลอรีนผ่านพันธะไอออนิก
คำถามศัตรู
แนวทางของศัตรูในหัวข้อนี้อาจแตกต่างไปจากที่เราเคยเห็นมาเล็กน้อย ดูว่าพันธะเคมีปรากฏในการทดสอบปี 2018 อย่างไร และเรียนรู้เพิ่มเติมเล็กน้อยเกี่ยวกับเนื้อหานี้
คำถามที่ 1
(ศัตรู/2018) การวิจัยแสดงให้เห็นว่าอุปกรณ์นาโนที่มีพื้นฐานมาจากการเคลื่อนที่ของอะตอมในมิติที่เกิดจาก เบา อาจมีการใช้งานในเทคโนโลยีในอนาคต แทนที่ micromotors โดยไม่ต้องใช้ส่วนประกอบ กลศาสตร์. ตัวอย่างของการเคลื่อนที่ของโมเลกุลที่เกิดจากแสงสามารถเห็นได้จากการดัดแผ่นเวเฟอร์ซิลิคอนบางๆ ยึดติดกับพอลิเมอร์อะโซเบนซีนและวัสดุรองรับในความยาวคลื่นสองช่วงดังแสดงใน รูป. ด้วยการใช้แสง ปฏิกิริยาย้อนกลับของสายโซ่โพลีเมอร์จะเกิดขึ้น ซึ่งส่งเสริมการเคลื่อนไหวที่สังเกตได้
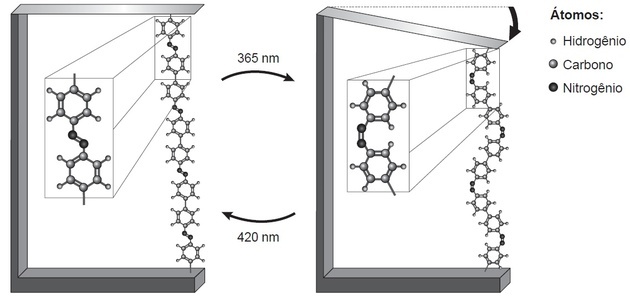
เทค, เอช. และ. นาโนเทคโนโลยีของโมเลกุล เคมีใหม่ที่โรงเรียน n. 21 พฤษภาคม 2548 (ดัดแปลง)
ปรากฏการณ์การเคลื่อนที่ของโมเลกุลที่เกิดจากอุบัติการณ์ของแสงเกิดจาก (ก)
(A) การเคลื่อนที่แบบสั่นของอะตอม ซึ่งทำให้พันธะสั้นลงและคลายตัว
(B) ไอโซเมอไรเซชันของพันธะ N=N รูปแบบ cis ของพอลิเมอร์มีขนาดกะทัดรัดกว่าทรานส์
(C) การทำให้เป็นเทาอัตโนมัติของหน่วยโมโนเมอร์ของพอลิเมอร์ ซึ่งนำไปสู่สารประกอบที่มีขนาดกะทัดรัดมากขึ้น
(D) เสียงสะท้อนระหว่างอิเล็กตรอน π ของกลุ่มเอโซกับอิเล็กตรอนของวงแหวนอะโรมาติกที่ทำให้พันธะคู่สั้นลง
(E) การแปรผันเชิงโครงสร้างของพันธะ N=N ที่ส่งผลให้เกิดโครงสร้างที่มีพื้นที่ผิวต่างกัน
ทางเลือกที่ถูกต้อง: (B) ไอโซเมอไรเซชันของพันธะ N=N รูปแบบ cis ของพอลิเมอร์มีขนาดกะทัดรัดกว่าทรานส์
การเคลื่อนที่ในสายโซ่โพลีเมอร์ทำให้เกิดการสังเกตโพลีเมอร์ที่ยาวขึ้นทางด้านซ้ายและตัวที่สั้นกว่าทางด้านขวา
เมื่อเน้นส่วนโพลีเมอร์ เราสังเกตสองสิ่ง:
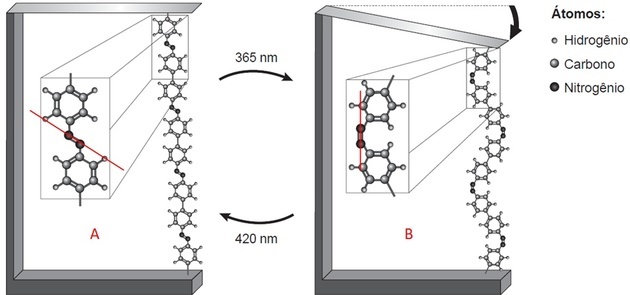
- มีสองโครงสร้างที่เชื่อมโยงกันด้วยพันธะระหว่างสองอะตอม (ซึ่งตำนานระบุว่าเป็นไนโตรเจน);
- ลิงค์นี้อยู่ในตำแหน่งต่างๆ ในแต่ละภาพ
การวาดเส้นบนรูปภาพ ใน A เราสังเกตว่าโครงสร้างอยู่ด้านบนและด้านล่างแกน นั่นคือด้านตรงข้าม ใน B พวกเขาอยู่ในด้านเดียวกันของเส้นที่ลาก
ไนโตรเจนทำให้พันธะสามตัวมีความเสถียร ถ้ามันผูกมัดกับโครงสร้างด้วยพันธะ มันก็จับกับไนโตรเจนอีกตัวหนึ่งผ่านพันธะคู่โควาเลนต์
การบดอัดของพอลิเมอร์และการงอของใบมีดเกิดขึ้นเนื่องจากสารยึดเกาะอยู่ในตำแหน่งที่แตกต่างกันเมื่อเกิดไอโซเมอริซึมของพันธะ N=N
ทรานส์ isomerism สังเกตพบใน A (ตัวเชื่อมที่อยู่ฝั่งตรงข้าม) และ cis ใน B (ตัวเชื่อมในระนาบเดียวกัน)
คำถาม2
(ศัตรู/2018) วัสดุที่เป็นของแข็งบางชนิดประกอบด้วยอะตอมที่ทำปฏิกิริยาซึ่งกันและกันทำให้เกิดพันธะที่สามารถเป็นโควาเลนต์ ไอออนิก หรือโลหะได้ รูปแสดงพลังงานศักย์ของการยึดเหนี่ยวตามฟังก์ชันของระยะห่างระหว่างอะตอมในของแข็งผลึก จากการวิเคราะห์รูปนี้ พบว่าที่อุณหภูมิศูนย์เคลวิน ระยะสมดุลของพันธะระหว่างอะตอม (R0) สอดคล้องกับค่าต่ำสุดของพลังงานศักย์ เหนืออุณหภูมินั้น พลังงานความร้อนที่จ่ายให้กับอะตอมจะเพิ่มพลังงานจลน์และสาเหตุ พวกมันแกว่งไปมารอบๆ ตำแหน่งสมดุลเฉลี่ย (วงกลมเต็ม) ซึ่งแตกต่างกันไปในแต่ละอัน อุณหภูมิ. ระยะการเชื่อมต่ออาจแตกต่างกันไปตามความยาวทั้งหมดของเส้นแนวนอน โดยระบุด้วยค่าอุณหภูมิของ T1 ที4 (อุณหภูมิที่เพิ่มขึ้น).
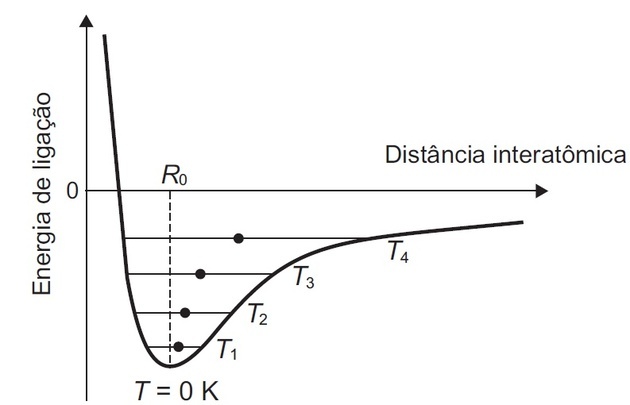
การกระจัดที่สังเกตได้ในระยะทางเฉลี่ยเผยให้เห็นปรากฏการณ์ของ
(A) การทำให้แตกตัวเป็นไอออน
(B) การขยาย
(ค) ความแตกแยก.
(D) การทำลายพันธะโควาเลนต์
(E) การก่อตัวของพันธะโลหะ
ทางเลือกที่ถูกต้อง: (B) การขยาย
อะตอมมีประจุบวกและลบ พันธะเกิดขึ้นเมื่อพวกมันไปถึงพลังงานขั้นต่ำโดยสร้างสมดุลระหว่างแรง (การผลักและแรงดึงดูด) ระหว่างอะตอม
จากนี้เราเข้าใจว่า: เพื่อให้เกิดพันธะเคมี มีระยะห่างในอุดมคติระหว่างอะตอมเพื่อให้มีความเสถียร
ภาพแสดงให้เราเห็นว่า:
- ระยะห่างระหว่างสองอะตอม (ระหว่างอะตอม) ลดลงจนกว่าจะถึงพลังงานต่ำสุด
- พลังงานจะเพิ่มขึ้นได้เมื่ออะตอมเข้าใกล้กันมากจนประจุบวกในนิวเคลียสเข้าใกล้ เริ่มผลักกัน และเพิ่มพลังงานตามมา
- ที่อุณหภูมิ T0 ของศูนย์เคลวินคือค่าต่ำสุดของพลังงานศักย์
- อุณหภูมิ T. สูงขึ้น1 ถึง T4 และพลังงานที่จ่ายไปทำให้อะตอมสั่นรอบตำแหน่งสมดุล (วงกลมเต็ม)
- การแกว่งเกิดขึ้นระหว่างเส้นโค้งและวงกลมเต็มตามอุณหภูมิแต่ละส่วน
เมื่ออุณหภูมิวัดระดับความปั่นป่วนของโมเลกุล ยิ่งอุณหภูมิสูงขึ้น อะตอมก็จะยิ่งสั่นมากขึ้น และพื้นที่ว่างที่เพิ่มขึ้น
อุณหภูมิสูงสุด (T4) บ่งชี้ว่าจะมีพื้นที่ว่างมากขึ้นโดยกลุ่มอะตอมนั้นและด้วยเหตุนี้วัสดุจึงขยายตัว
คำถาม 3
(ศัตรู/2019) เพราะพวกมันมีชั้นวาเลนซ์ที่สมบูรณ์ พลังงานไอออไนเซชันสูงและความสัมพันธ์ทางอิเล็กทรอนิกส์ แทบจะเป็นโมฆะ ถือว่าเป็นเวลานานแล้วที่ก๊าซมีตระกูลจะไม่ก่อตัวเป็นสารประกอบ สารเคมี อย่างไรก็ตาม ในปี 1962 ปฏิกิริยาระหว่างซีนอน (5s²5p⁶ วาเลนซ์เลเยอร์) กับแพลตตินัมเฮกซะฟลูออไรด์ได้สำเร็จลุล่วงไปด้วยดี และตั้งแต่นั้นมา สารประกอบของก๊าซมีตระกูลใหม่ ๆ ก็ได้ถูกสังเคราะห์ขึ้น
สารประกอบดังกล่าวแสดงให้เห็นว่าเราไม่สามารถยอมรับกฎออกเตตอย่างไม่มีวิจารณญาณได้ ซึ่งถือว่า ในพันธะเคมี อะตอมมักจะได้รับความเสถียรโดยสมมติการกำหนดค่าทางอิเล็กทรอนิกส์ของแก๊ส มีคุณธรรมสูง. ในบรรดาสารประกอบที่รู้จัก สารที่เสถียรที่สุดคือซีนอนไดฟลูออไรด์ซึ่งมีอะตอมของฮาโลเจนสองอะตอม ฟลูออรีน (ชั้นวาเลนซ์ 2s²2p⁵) พันธะโควาเลนต์กับอะตอมของก๊าซมีตระกูลซึ่งมีอิเล็กตรอนแปดตัว ความจุ
เมื่อเขียนสูตรลิวอิสสำหรับสารประกอบซีนอนดังกล่าว อะตอมของก๊าซมีตระกูลมีอิเล็กตรอนในเปลือกเวเลนซ์กี่ตัว?
(A) 6
(B) 8
(C) 10
(D) 12
ทางเลือกที่ถูกต้อง: c) 10.
ฟลูออรีนเป็นองค์ประกอบที่เป็นส่วนหนึ่งของกลุ่ม 17 ของตารางธาตุ ดังนั้นในเปลือกอิเล็กทรอนิกส์ชั้นนอกสุดมีอิเล็กตรอน 7 ตัว (2s2 2p5) เพื่อให้ได้ความเสถียร ตามกฎออกเตต อะตอมของธาตุนี้ต้องการอิเล็กตรอน 1 ตัวจึงจะมีอิเล็กตรอน 8 ตัวในเปลือกเวเลนซ์และสมมติการกำหนดค่าทางอิเล็กทรอนิกส์ของก๊าซมีตระกูล
ในทางกลับกัน ซีนอนเป็นก๊าซมีตระกูล ดังนั้นจึงมีอิเล็กตรอน 8 ตัวในชั้นสุดท้าย (5 วินาที)2 5p6).
โปรดทราบว่าชื่อของสารประกอบคือซีนอนไดฟลูออไรด์ ซึ่งหมายความว่าสารประกอบนี้ประกอบด้วยฟลูออรีนสองอะตอมและอะตอมซีนอนหนึ่งอะตอม XeF2.
ตามที่กล่าวไว้ พันธะเคมีระหว่างอะตอมเป็นชนิดโควาเลนต์ กล่าวคือ มีการแบ่งปันอิเล็กตรอน
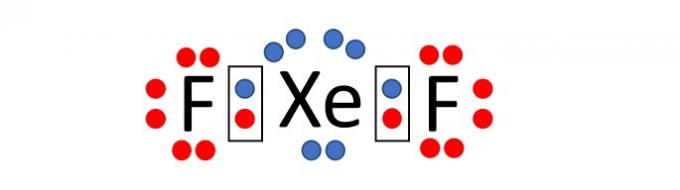
กระจายอิเล็กตรอนรอบ ๆ แต่ละอะตอม (7 รอบฟลูออรีนและ 8 รอบซีนอน) เราเห็น ว่าอะตอมของซีนอนเมื่อจับกับฟลูออรีนสองอะตอม มีอิเล็กตรอน 10 ตัวในเปลือกฟลูออรีน ความจุ
ดูด้วย:
- กฎออกเตต
- แบบฝึกหัดเกี่ยวกับการกระจายทางอิเล็กทรอนิกส์
- แบบฝึกหัดเกี่ยวกับไฮโดรคาร์บอน
