สมดุลความร้อน คือภาวะที่ร่างกายพบตัวเองใน เหมือนกันอุณหภูมิ กว่าสิ่งรอบตัวของพวกเขา สังเกตได้ว่าร่างกายทั้งหมดที่มีอุณหภูมิสูงกว่าเพื่อนบ้านมักจะให้ความร้อนตามธรรมชาติจนกว่าทั้งคู่จะมีอุณหภูมิเท่ากัน
ดูยัง:พื้นฐานของอุณหพลศาสตร์
สมดุลความร้อนและกฎศูนย์ของอุณหพลศาสตร์
สมดุลความร้อนเป็นแนวคิดหลักที่อยู่เบื้องหลังกฎศูนย์ของเทอร์โมไดนามิกส์ กฎหมายดังกล่าวกำหนดว่า ในกรณีที่ระบบเทอร์โมไดนามิกสองระบบ THE และ บีอยู่ในสภาวะสมดุลทางความร้อนด้วยระบบเทอร์โมไดนามิกที่สาม คแล้ว THE และ บี พวกเขาจะอยู่ในสมดุลทางความร้อนด้วย
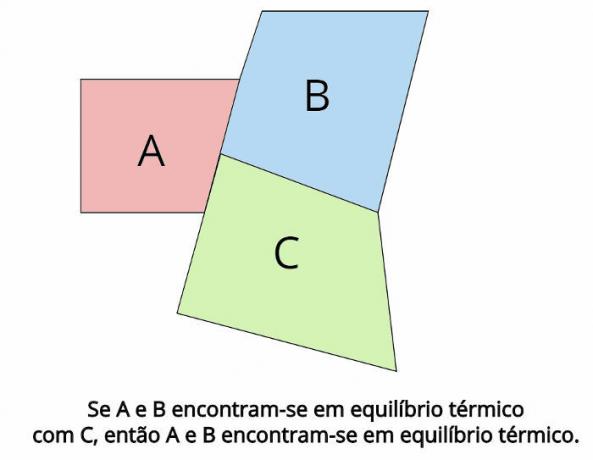
ในสภาวะสมดุลทางความร้อน อุณหภูมิสุดท้ายของร่างกายแต่ละส่วนต้องเท่ากัน: TTHE = Tบี = Tค
ตรวจสอบว่าคำกล่าวของกฎศูนย์ของอุณหพลศาสตร์กำหนดไว้อย่างไร:
“หากวัตถุทั้งสองอยู่ในสมดุลความร้อนกับวัตถุที่สาม วัตถุเหล่านั้นจะอยู่ในสมดุลความร้อนซึ่งกันและกัน”
อีกวิธีหนึ่งในการทำความเข้าใจสมดุลความร้อนนั้นขึ้นอยู่กับพลังงานภายในร่างกาย พลังงานภายในหรือเพียงแค่พลังงานความร้อนคือปริมาณทางกายภาพ โดยตรงสัดส่วน à อุณหภูมิ ของร่างกาย. ดังนั้น หากมีวัตถุที่มีอุณหภูมิต่างกันภายในระบบเทอร์โมไดนามิกเดียวกัน วัตถุเหล่านั้นจะมีโมดูลของ. ต่างกัน พลังงานภายในจึงถ่ายเทพลังงานบางส่วนระหว่างกัน จนกว่าจะไม่มีความแตกต่างระหว่างพลังงานของพวกมัน ภายใน. ต้องการทราบข้อมูลเพิ่มเติมเกี่ยวกับพลังงานภายในและคุณสมบัติของมันคืออะไร? เข้าถึงบทความ:
กำลังภายใน.อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
สมดุลความร้อนและความร้อน
การถ่ายเทความร้อนเกิดขึ้นเองตามธรรมชาติเสมอ จากร่างกายที่มีอุณหภูมิสูงสุดไปยังร่างกายที่มีอุณหภูมิต่ำสุด การถ่ายเทพลังงานในรูปของความร้อนนี้สามารถเกิดขึ้นได้ผ่านกระบวนการต่างๆ เช่น ขับรถ, การพาความร้อน และ รังสี
การขับรถ: เป็นการถ่ายเทความร้อนระหว่างวัตถุที่เกิดขึ้นโดยเฉพาะในของแข็ง ในการนำประเภทนี้จะไม่มีการถ่ายโอนมวลเกิดขึ้น การถ่ายเทความร้อนประเภทนี้จะอธิบายว่าสมดุลทางความร้อนเกิดขึ้นในโลหะอย่างไร
การพาความร้อน: เป็นการถ่ายเทความร้อนที่เกิดขึ้นในของเหลว ในโหมดการถ่ายเทความร้อนนี้ มีการถ่ายเทมวล เมื่อของเหลวที่ให้ความร้อนเคลื่อนตัว ทำให้เกิดกระแสการพาความร้อนจนของเหลวทั้งหมดถึงสมดุลทางความร้อน
รังสี: มันคือการส่งความร้อนผ่านคลื่นแม่เหล็กไฟฟ้า ดังนั้นกระบวนการนี้จึงเกิดขึ้นแม้ว่าจะไม่มีตัวกลางทางกายภาพระหว่างร่างกายกับวัตถุอื่นที่อุณหภูมิต่างกัน ความร้อนที่ถ่ายเทในกรณีนี้ มีค่าเท่ากับคลื่นแม่เหล็กไฟฟ้าที่มีพลังงานน้อยกว่า แสงที่มองเห็นได้ซึ่งก็คือการแผ่รังสีความร้อนซึ่งอยู่ในบริเวณของ อินฟราเรด.
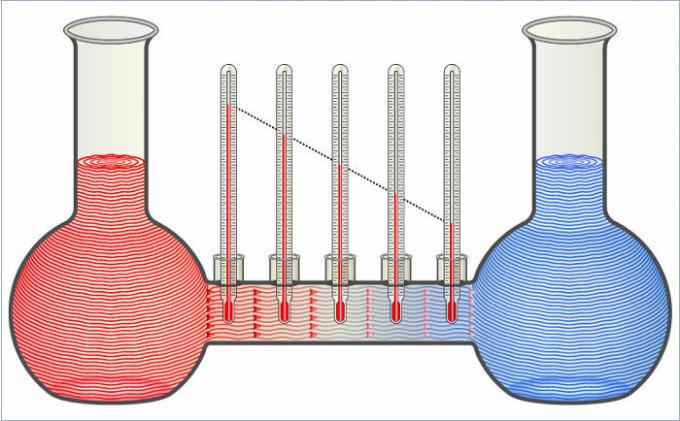
ของเหลวทั้งสองในรูปจะถ่ายเทความร้อนซึ่งกันและกันจนกว่าอุณหภูมิจะเท่ากัน
คุณต้องการทราบข้อมูลเพิ่มเติมเกี่ยวกับวิธีการถ่ายเทความร้อนแต่ละกระบวนการหรือไม่? เข้าถึงบทความ: กระบวนการกระจายความร้อน.
ความร้อนที่เหมาะสม
เมื่อมี ความแตกต่างในอุณหภูมิ ระหว่างร่างทั้งสองหรือระหว่างร่างกายกับสภาพแวดล้อมจะมีการแลกเปลี่ยนความร้อนระหว่างกันโดยธรรมชาติเพื่อให้ อุณหภูมิร่างกายที่สูงขึ้นจะเย็นลง และวัตถุที่มีอุณหภูมิต่ำกว่าจะร้อนขึ้นจนกระทั่งถึงอุณหภูมิทั้งหมด ใน สมดุลความร้อน
ปริมาณความร้อนที่แลกเปลี่ยนระหว่างร่างกายที่อุณหภูมิต่างกันเรียกว่า ความร้อนที่เหมาะสม และจำนวนเงินนี้สามารถคำนวณได้จากสูตรที่แสดงในรูปด้านล่าง:
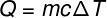
คิว – ความร้อน (มะนาวหรือเจ)
ม – มวล (g หรือ kg)
ค - ความร้อนจำเพาะ (cal/gºC หรือ J/kg. เค)
ΔT – ความแปรผันของอุณหภูมิ (°C หรือ K)
ในสูตรที่แสดงด้านบนนี้ สิ่งสำคัญคือต้องเน้นย้ำถึงความยิ่งใหญ่ของชื่อ ความร้อนจำเพาะ. ขนาดดังกล่าววัดค่า ปริมาณพลังงานต่อมวลที่สารต้องการผลิตหรือดูดซับ เพื่อให้อุณหภูมิเปลี่ยนแปลงไป 1°C ตัวอย่างเช่น ในกรณีของน้ำบริสุทธิ์ และภายใต้สภาวะความดันปกติ หากต้องการเปลี่ยนแปลงอุณหภูมิของน้ำ 1ºC จะต้องให้พลังงาน 1.0 แคลอรีต่อน้ำ 1 กรัม
ดังนั้น สารทั้งหมดที่มีการสัมผัสทางความร้อนระหว่างกันมักจะเข้าสู่สภาวะของ สมดุลความร้อน อย่างไรก็ตาม เมื่อเวลาผ่านไปโดยธรรมชาติ บางชนิดต้องการพลังงานจำนวนมากขึ้นจึงจะทำเช่นนั้นได้ และสิ่งนี้ส่งผลกระทบโดยตรงต่ออุณหภูมิในการไปถึงสมดุลทางความร้อน
อ่านยัง:อุณหภูมิคืออะไร?
ความร้อนแฝง
เป็นไปได้ว่าระหว่างการแลกเปลี่ยนความร้อนกับสิ่งแวดล้อม ร่างกายจะเกิดแรงดัน อุณหภูมิ และปริมาตรที่ทำให้ร่างกายเปลี่ยนแปลงสภาพร่างกาย การเปลี่ยนแปลงเหล่านี้เกิดขึ้นใน อุณหภูมิค่าคงที่ (สำหรับร่างกายที่ประกอบด้วยสารเดี่ยวที่ไม่มีสิ่งเจือปน) นั่นคือแม้จะได้รับหรือให้ความร้อนกับสภาพแวดล้อมภายนอก แต่อุณหภูมิของร่างกายเหล่านี้ก็ไม่เปลี่ยนแปลง
สิ่งนี้เป็นไปได้เพราะในกรณีนี้ พลังงานทั้งหมดที่แลกเปลี่ยนจะถูกใช้เพื่อเปลี่ยนโครงสร้างของโมเลกุลของคุณ จากช่วงเวลาที่อุปสรรคพลังงาน "เอาชนะ" และเนื้อหาทั้งหมดของร่างกายอยู่ในสถานะทางกายภาพอื่น, ร่างกายยังคงแลกเปลี่ยนความร้อนกับสิ่งแวดล้อมรอบตัวต่อไป เว้นแต่แน่นอนว่าอุณหภูมิของมันเท่ากับอุณหภูมิภายนอก
โอ ความร้อนแฝง สามารถคำนวณได้จากสูตรที่แสดงในรูปด้านล่าง ตรวจสอบได้:
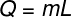
คิว – ความร้อนแฝง (มะนาวหรือเจ)
ม – มวล (g หรือ kg)
หลี่ – ความร้อนแฝงจำเพาะ (cal/g หรือ J/kg)
สูตรสมดุลความร้อน
ในกรณีที่เราต้องการค้นหาว่า .คืออะไร อุณหภูมิในสมดุล ของระบบอุณหพลศาสตร์บางระบบ จำเป็นต้องพิจารณาระบบที่เป็นปัญหาเป็น a ระบบโดดเดี่ยวนั่นคือเราต้องสมมติว่าไม่มีการแลกเปลี่ยนความร้อนกับย่านใกล้เคียงของระบบนี้
จากเงื่อนไขนี้ เราสามารถพูดได้ว่าปริมาณความร้อนทั้งหมดแลกเปลี่ยนกันระหว่างร่างกายที่ประกอบขึ้นเป็นระบบนี้เท่านั้น ไม่คำนึงถึงการสูญเสียความร้อน สำหรับผนังตู้คอนเทนเนอร์ เป็นต้น ในกรณีนี้ เราว่าภาชนะมี ความจุความร้อน เล็กน้อยคือไม่ดูดซับความร้อนใดๆ
ลองนึกภาพสถานการณ์ต่อไปนี้: เทน้ำแข็งลงในถ้วยชาร้อนที่มีความจุความร้อนเพียงเล็กน้อย เพื่อที่จะกำหนดอุณหภูมิสมดุลทางความร้อน นอกเหนือจากการรู้เงื่อนไขเริ่มต้นของระบบแล้ว เราต้องพิจารณาบางประการ:
ปริมาณความร้อนทั้งหมดที่ชาร้อนมอบให้กับน้ำแข็งจะถูกดูดซับอย่างเต็มที่ เนื่องจากถ้วยมีความจุความร้อนเพียงเล็กน้อย
เราต้องละเลยการสูญเสียความร้อนในอากาศและสภาพแวดล้อมอื่น ๆ เพื่อให้ถ้วยชานี้สามารถเข้าใจได้ว่าเป็นระบบเทอร์โมไดนามิกแบบปิด
ด้วยวิธีนี้ เราสามารถระบุได้ว่าปริมาณความร้อนทั้งหมดที่ได้รับจากน้ำแข็งนั้นหมดไปโดยชาร้อน ด้วยเหตุนี้ เราจึงเขียนสูตรสำหรับคำนวณสมดุลทางความร้อน
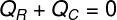
คิวR – ความร้อนที่ได้รับ
คิวค – ความร้อนที่ได้รับใน
ความร้อนที่ให้ใน (Qค) หมายถึงปริมาณความร้อนที่ชาร้อนถ่ายโอนไปยังก้อนน้ำแข็งที่ใส่เข้าไป ได้รับความร้อนแล้ว (QR) คือปริมาณความร้อนที่ก้อนน้ำแข็งเหล่านี้ได้รับ ความร้อนปริมาณนี้จะมี 2 ลักษณะคือ ความร้อน อ่อนไหว และร้อน แฝงเนื่องจากการเข้าสู่สภาวะสมดุลทางความร้อน ก้อนน้ำแข็งจึงมีแนวโน้มที่จะละลาย
การหาอุณหภูมิสมดุลทางความร้อน
ลองหาอุณหภูมิสมดุลทางความร้อนจากสถานการณ์ต่อไปนี้:
ถ้วยที่มีความจุความร้อนเพียงเล็กน้อย ซึ่งบรรจุชา 200 มล. (200 กรัม) ที่อุณหภูมิเริ่มต้นที่ 70°C จะได้รับน้ำแข็ง 10 กรัมที่อุณหภูมิ -10°C กำหนดอุณหภูมิสมดุลความร้อนของระบบ (สมมติว่าความร้อนจำเพาะของชาเท่ากับความร้อนจำเพาะของน้ำ):
ข้อมูล:
คน้ำ = 1.0 cal/g°C
คน้ำแข็ง = 0.5 cal/g°C°
หลี่น้ำแข็ง = 80 แคลอรี/กรัม
อันดับแรก เราคิดว่าความร้อนทั้งหมดที่น้ำแข็งได้รับนั้นมาจากชา:

ถัดไป จำเป็นต้องให้รายละเอียดว่าได้รับและรับความร้อนรูปแบบใด:
ชา: ชาให้ความร้อนที่เหมาะสมเท่านั้น (Qส) เนื่องจากสภาพร่างกายของเขาไม่เปลี่ยนแปลง
น้ำแข็ง: น้ำแข็งเริ่มแรกที่อุณหภูมิ -10°C จึงได้รับความร้อนที่เหมาะสม (Qส) จนอุณหภูมิ 0 ºC แล้วจึงได้รับความร้อนแฝง (Qหลี่) ทำให้เป็นของเหลว กลายเป็นของเหลวแล้วได้รับความร้อนแฝง (Qส) จนกระทั่งเข้าสู่สมดุลความร้อน (TF) กับชา
การแปลสิ่งที่วิเคราะห์ข้างต้นในรูปของสมการ เราจะมีการคำนวณต่อไปนี้เพื่อแก้:
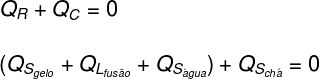
โดยการแทนที่ข้อมูลที่ได้จากแบบฝึกหัดในสมการข้างต้น เราจะต้องแก้การคำนวณต่อไปนี้:
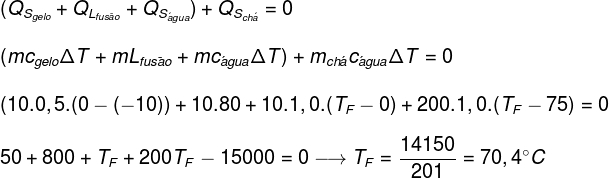
จากการคำนวณข้างต้น อุณหภูมิสมดุลของระบบชา+น้ำแข็งควรอยู่ที่ประมาณ 70.4°C
การทดสอบสมดุลความร้อน
ในการทดสอบสมดุลความร้อนระหว่างวัตถุทั้งสอง เราสามารถดำเนินการทดลองหลายอย่าง อย่างไรก็ตาม วิธีที่ง่ายที่สุดคือการใช้ a แคลอรีมิเตอร์ มันคือ เครื่องวัดอุณหภูมิ. แคลอริมิเตอร์เป็นภาชนะอะเดียแบติก (ซึ่งไม่อนุญาตให้ผ่านความร้อน) โดยมีความจุความร้อน เกี่ยวกับไม่สำคัญอย่างเช่นหม้อที่ปูด้วยโฟม เป็นต้น ซึ่งเป็นฉนวนกันความร้อนที่ดี

แคลอรีมิเตอร์ใช้สำหรับวัดความแปรผันของอุณหภูมิของระบบภายใน
สมดุลความร้อนและชีวิตบนโลก
โอ สมดุลความร้อน มันมีบทบาทสำคัญในชีวิตบก หากไม่มีก๊าซเรือนกระจกในชั้นบรรยากาศของโลก รังสีความร้อน ของโลกก็จะปล่อยมันออกไปแพร่กระจายสู่อวกาศ เมื่อเวลาผ่านไป สิ่งนี้จะทำให้โลกเย็นลงอย่างมาก ทำให้มหาสมุทรกลายเป็นน้ำแข็งเมื่อเวลาผ่านไป
นอกจากนี้ มหาสมุทรยังมีบทบาทสำคัญใน สมดุลความร้อน ของดาวเคราะห์ โดยอาศัยความยิ่งใหญ่ของมัน พาสต้า และ ความร้อนเฉพาะ มหาสมุทรมีมากมาย ความจุความร้อน, นั่นคือพวกเขาต้องได้รับความร้อนจำนวนมากเพื่อเปลี่ยนอุณหภูมิ ด้วยเหตุนี้เอง พวกมันจึงสามารถควบคุมอุณหภูมิของดาวเคราะห์ได้อย่างมีประสิทธิภาพ พื้นที่ห่างไกลจากมหาสมุทรและมีน้ำน้อยมักจะมีขนาดใหญ่ tend ช่วงความร้อนเช่นเดียวกับกรณีของทะเลทรายซึ่งร้อนจัดในตอนกลางวันและเย็นจัดในตอนกลางคืน
ดังนั้น สมดุลความร้อน มันเป็นกระบวนการที่มีความสำคัญขั้นพื้นฐานสำหรับการรักษากระบวนการทางกายภาพ เคมี และชีวภาพบนโลก และดังนั้นจึงจำเป็นสำหรับการดำรงอยู่ของสิ่งมีชีวิตบนโลก
By Me. ราฟาเอล เฮเลอร์บร็อก

