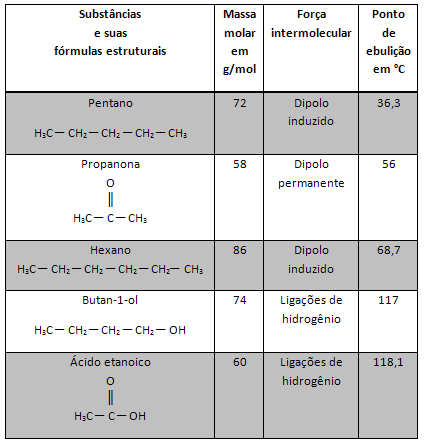
ปฏิกิริยาลดการเกิดออกซิเดชันมีลักษณะเป็นกระบวนการสูญเสียและรับอิเล็กตรอนไปพร้อม ๆ กัน เนื่องจากอิเล็กตรอนที่สูญเสียไปโดยอะตอม ไอออน หรือโมเลกุลจะได้รับโดยผู้อื่นทันที
เพื่อให้เข้าใจ ดูตัวอย่าง:
สารละลายคอปเปอร์ซัลเฟต (CuSO4(aq)) เป็นสีน้ำเงินเนื่องจากมี Cu ion2+ ละลายในนั้น ถ้าเราใส่แผ่นสังกะสีโลหะ (Zn(ส)) ในสารละลายนี้ เมื่อเวลาผ่านไป เราอาจสังเกตเห็นการเปลี่ยนแปลงสองอย่าง: สีของสารละลายจะกลายเป็นไม่มีสี และคราบทองแดงที่เป็นโลหะจะปรากฏบนแผ่นสังกะสี
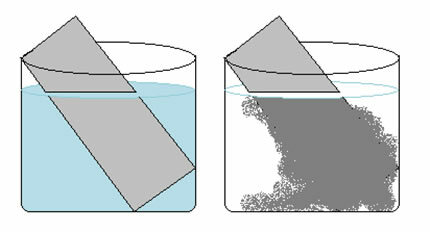
ดังนั้นปฏิกิริยาที่เกิดขึ้นในกรณีนี้จึงเป็นดังนี้:
สังกะสี(ส) + CuSO4(aq) → คู(ส) + ZnSO4(aq)
หรือ
สังกะสี(ส) + Cu2+(ที่นี่) + OS42-(ที่นี่) → คู(ส) + Zn2+(ที่นี่) + OS42-(ที่นี่)
หรือยัง
สังกะสี(ส) + Cu2+(ที่นี่) → คู(ส) + Zn2+(ที่นี่)
โปรดทราบว่ามีการถ่ายโอนอิเล็กตรอนจากสังกะสีไปเป็นทองแดง การวิเคราะห์การแยกการเปลี่ยนแปลงที่เกิดขึ้นในแต่ละองค์ประกอบเหล่านี้ เรามี:
- สังกะสี(ส) → Zn2+(ที่นี่)
สังกะสีสูญเสียอิเล็กตรอนไป 2 ตัวจากสังกะสีเป็นไอออนบวก ในกรณีนั้น, สังกะสีได้รับการออกซิเดชัน
- ตูด2+(ที่นี่) → คู(ส)
ในทางตรงกันข้ามกับทองแดงได้รับอิเล็กตรอน 2 ตัวผ่านจากไอออนบวกของทองแดงเป็นทองแดงที่เป็นโลหะ ทองแดงลดลง
สิ่งนี้อธิบายการเปลี่ยนแปลงทั้งสองที่สังเกตได้ เนื่องจากสารละลายไม่มีสีเนื่องจากไอออนของทองแดงถูกเปลี่ยนเป็นทองแดงที่เป็นโลหะ ซึ่งถูกสะสมอยู่บนแผ่นสังกะสี
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
เนื่องจากมีการสูญเสียและรับอิเล็กตรอนพร้อมกัน ปฏิกิริยานี้จึงเป็นตัวอย่างของปฏิกิริยารีดอกซ์ และเราสามารถสร้างแนวคิดต่อไปนี้ซึ่งทำซ้ำสำหรับปฏิกิริยาอื่น ๆ ทั้งหมดของสิ่งนี้ ประเภท:

โลหะที่มีปฏิกิริยามากที่สุดจะเกิดปฏิกิริยาออกซิเดชันดังนั้น ในตัวอย่างที่เสนอ สังกะสีมีปฏิกิริยามากกว่าทองแดง
ปฏิกิริยารีดอกซ์อื่นที่สามารถอ้างถึงได้เกิดขึ้นเมื่อเราใส่แมกนีเซียมหรืออะลูมิเนียมลงในสารละลายกรดไฮโดรคลอริก ในปฏิกิริยาเหล่านี้ ไฮโดรเจนจากกรดไฮโดรคลอริกรับอิเล็กตรอน 3 ตัวจากอะลูมิเนียม (หรือ 2 อิเล็กตรอนจากแมกนีเซียม) ส่งผ่านจากไอออนของ H+ สำหรับก๊าซไฮโดรเจน (H2) ในขณะที่โลหะกลายเป็นไอออนบวก:
2 อัล(ส) + 6 ชั่วโมง+(ที่นี่) → 2 อัล3+(ที่นี่) + 3H2 (ก.)
มก.(ส) + 2 ชั่วโมง+(ที่นี่) → มก2+(ที่นี่) + โฮ2 (ก.)
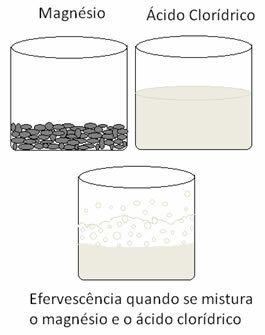
โลหะได้รับการออกซิเดชันและไฮโดรเจนได้รับการลดลง ด้านล่างเป็นรูปที่แสดงว่าการเพิ่มแมกนีเซียมในกรดไฮโดรคลอริกทำให้เกิด causes ฟู่ซึ่งเกิดจากการปล่อยก๊าซไฮโดรเจนและแมกนีเซียมก็หายไปตามที่เป็นอยู่ บริโภค
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ปฏิกิริยาออกซิเดชัน"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี
การทำงานของถุงลมนิรภัย อุปกรณ์ที่ออกแบบมาเพื่อปกป้องคนขับ แรงกระตุ้นไฟฟ้า ปฏิกิริยาการสลายตัวทางเคมี การชนกัน, ส่วนผสมทางเคมีของโซเดียมเอไซด์, เซ็นเซอร์ที่กันชนรถ, อัลคาไลซิลิเกต, แก๊ส ไนโตรเจน
เคมี

เลนส์ไวแสง ปฏิกิริยาลดการเกิดออกซิเดชัน การสูญเสียหรือได้รับอิเล็กตรอน เลนส์สังเคราะห์แสงในแว่นกันแดด องค์ประกอบของแก้วโฟโตโครมาติก, อะตอมออกซิเจนเตตระฮีดรัล, โครงสร้างผลึกของซิลเวอร์คลอไรด์, แสงอัลตราไวโอเลต, โลหะเงิน