THE เอนทาลปี (H) สามารถกำหนดเป็นปริมาณพลังงานของวัสดุแต่ละชนิดหรือเป็นพลังงานโดยรวมของระบบ อย่างไรก็ตาม ในทางปฏิบัติ เป็นไปไม่ได้ที่จะกำหนดเอนทาลปีของสาร ดังนั้น สิ่งที่วัดได้โดยทั่วไปคือ การเปลี่ยนแปลงของเอนทาลปี 

เราจะวิเคราะห์ความผันแปรของเอนทัลปีในปฏิกิริยาคายความร้อน (คำว่า "exo" มาจากภาษากรีกและแปลว่า "ออก, ออกจาก, ออก") ซึ่งเป็นปฏิกิริยาที่มีการปล่อยความร้อน ในชีวิตประจำวัน มีตัวอย่างมากมายของปฏิกิริยาเหล่านี้ที่เกิดขึ้น เช่น การเผาไหม้และส่วนผสมของปูนขาวกับน้ำ
ในกรณีเหล่านี้ ความผันแปรของเอนทาลปี 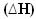 จะเท่ากับปริมาณความร้อนที่ปล่อยออกมา โดยกำหนดจากค่าเอนทาลปีสุดท้ายลบด้วยเอนทาลปีเริ่มต้น (Hฉ - โฮผม) หรือเนื่องจากเป็นปฏิกิริยา ค่าเอนทาลปีของผลิตภัณฑ์ลบด้วยค่าของสารตั้งต้น (Hพี - โฮR).
จะเท่ากับปริมาณความร้อนที่ปล่อยออกมา โดยกำหนดจากค่าเอนทาลปีสุดท้ายลบด้วยเอนทาลปีเริ่มต้น (Hฉ - โฮผม) หรือเนื่องจากเป็นปฏิกิริยา ค่าเอนทาลปีของผลิตภัณฑ์ลบด้วยค่าของสารตั้งต้น (Hพี - โฮR).
เมื่อปล่อยความร้อน พลังงานจะหายไป ดังนั้นพลังงานทั้งหมดของระบบจึงลดลง ดังนั้นเอนทาลปีของผลิตภัณฑ์จะต่ำกว่า. เสมอ ของรีเอเจนต์ ดังนั้นการแปรผันของเอนทาลปีในปฏิกิริยาคายความร้อนจะเป็นลบเสมอ น้อยกว่า ศูนย์ 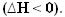
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
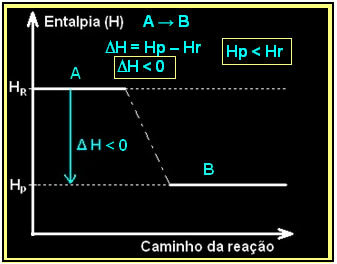
พิจารณาปฏิกิริยาคายความร้อนทั่วไป:
| A → B + ความร้อน |
สิ่งนี้สามารถแสดงได้โดยใช้ไดอะแกรมเอนทาลปีดังตัวอย่างด้านล่าง:
การเผาไหม้ของก๊าซไฮโดรเจนด้วยการก่อตัวของน้ำของเหลวเกิดขึ้นพร้อมกับการปล่อยพลังงาน ค่าความแปรผันของเอนทาลปีของระบบในปฏิกิริยานี้กำหนดโดย:
2 ชม2(ก.) + โอ2(ก.) → 2H2โอ(1)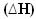 = - 572 kJ
= - 572 kJ
ไดอะแกรมของคุณจะแสดงดังนี้:
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "การเปลี่ยนแปลงของเอนทัลปีในปฏิกิริยาคายความร้อน"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/variacao-entalpia-reacoes-exotermicas.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี

เทอร์โมเคมี, เอนทัลปี, ความร้อนที่ปล่อยออกมา, ปฏิกิริยาคายความร้อน, ปฏิกิริยาการเผาไหม้, สภาพแวดล้อมภายนอก, ปฏิกิริยาดูดความร้อน, ปฏิกิริยา เคมี, การแลกเปลี่ยนพลังงาน, รีเอเจนต์, การปล่อยแสง, การดูดกลืนแสง, ความร้อน, ไฟฟ้า, ส่วนประกอบ, สถานะทางกายภาพ, สินค้า.