Niekedy sa to môže stať minimálny vzorec byť rovnaké ako molekulárny vzorec zlúčeniny; to však nie je vždy pravda.
Napríklad empirický alebo minimálny vzorec pre vodu je H2O, čo naznačuje, že medzi prvkami, ktoré tvoria molekuly vody, je pomer 2: 1. A zhodou okolností to je tiež molekulárny vzorec pre vodu. Ak sa však chcete presvedčiť, že sa tak nestane vždy, pozrite si nasledujúce dva príklady:
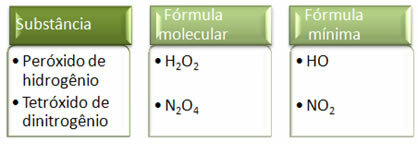
Pretože minimálny vzorec predstavuje iba pomer atómov každého prvku a nie ich skutočné množstvo v molekulárnom vzorci, môže sa vyskytnúť rôznych zlúčenín majúcich rovnaký empirický vzorec a dokonca aj minimálny vzorec zlúčeniny môže byť rovnaký ako molekulárny vzorec iné. V nasledujúcom príklade si všimnite, ako sa to môže stať:
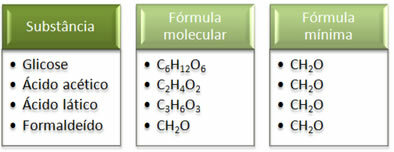
Vidíme, že minimálny vzorec CH2To isté je rovnaké pre všetky látky, to znamená, že tento minimálny vzorec vyjadruje, že vo všetkých prípadoch atómy uhlíka, vodíka a kyslíka sú prítomné v molekulárnych vzorcoch v pomere 1:2:1. Ďalej, jediný, ktorý má rovnaký molekulárny vzorec ako empirický vzorec, je formaldehyd.
- Výpočet minimálneho alebo empirického vzorca:
Na stanovenie empirického vzorca zlúčeniny je najskôr potrebné vedieť, aké je jej percento alebo najbližší vzorec. To sa dá urobiť zmeraním hmotnosti každého prvku v 100 g vzorky. Text „Percento alebo centimálny vzorec”Objasňuje túto záležitosť lepšie.
Teraz neprestávajte... Po reklame je toho viac;)
Napríklad, povedzme, že najbližšie zloženie danej zlúčeniny je dané: 40,00% C, 6,67% H a 53,33% O. Tieto hodnoty odovzdáme gramom, berúc do úvahy hmotnosť 100 g vzorky kompostu. Máme teda: 40 g C, 6,67 g H a 53,33 g O.
Teraz je potrebné odovzdať tieto hodnoty množstvu hmoty (mol). Robíme to tak, že každú z nájdených hodnôt vydelíme ich príslušnými molárnymi hmotnosťami:
C: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Keďže hodnoty nie sú celé čísla, použijeme nasledujúce zariadenie: všetky hodnoty vydelíme najmenšou z nich, aby sa pomer medzi nimi nezmenil.
V tomto prípade je najmenšia hodnota 3,33, takže výsledok bude:
C: 3,33 / 3,33 = 1
H: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Minimálny vzorec tejto neznámej látky sa teda rovná: Ç1H2O1 alebo CH2O.
Stručne povedané, kroky potrebné na nájdenie empirického alebo minimálneho vzorca látky sú:

Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. "Minimálny alebo empirický vzorec"; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Prístup k 28. júnu 2021.