Тази смес от газове води до хомогенни смеси или газообразни разтвори. Например, газовете, които излизат от фабричните комини или автомобилните отработени газове, се разпространяват във въздуха атмосферни и с течение на времето не успяхме да ги различим повече, тъй като имаше дифузия на тези газове през въздух.

Газовете, отделяни от комините, се дифундират и „изгубват“ в атмосферния въздух, тъй като обемът на въздуха е много по-голям от този на дима.
| THE дифузия на газ е спонтанно движение на газ през друг, тоест разпространението му в друга газова среда. |
| THE излив на газове е особен вид дифузия, при която има изтичане на газове през малки дупки (или порести стени, които представляват набор от малки дупки). |
Например балони, продавани на деца, са пълни с газ хелий. С течение на времето този газ преминава през гумените пори на балона, тоест има неговия излив. Това се доказва от факта, че балонът се изпуска след няколко часа.
Шотландският химик Томас Греъм през 1829 г. изследва това поведение на газовете. Той заключи, че скоростта, с която един газ дифундира или излива в друг, е свързана с неговата плътност. Тъй като неговите експериментални данни се повтарят за всички газове, той създава следния закон, който носи неговото име:
Законът на Греъм: скоростта на дифузия или изливане на газ е обратно пропорционална на корен квадратен от неговата плътност.
Математически този закон може да се изрази с уравнението:
v α 
Или, свързвайки два различни газа, имаме:
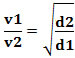
Използваната единица в този случай е „обемът, който се изпуска за единица време“; следователно като цяло л/мин (литри в минута).
Така газовете с по-ниска плътност дифундират по-бързо. Ако е в същото състояние на температура и налягане, можете също да направите връзка между това с масата газов моларен: колкото по-голяма е плътността на газа, толкова по-голяма е моларната му маса и по-ниска е скоростта му на дифузия; и обратно. Така имаме:
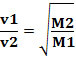
От Дженифър Фогаса
Завършил химия
Училищен отбор на Бразилия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/difusao-efusao-dos-gases.htm
