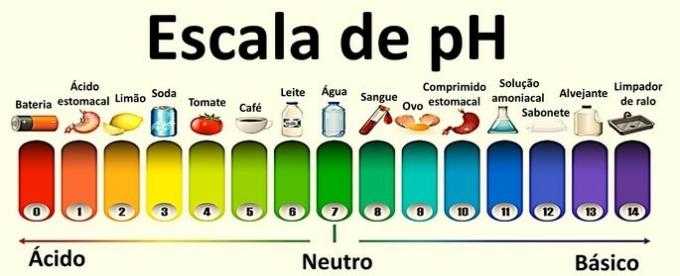
pH представлява водородния йонен потенциал, а pOH е хидрокси йонният потенциал на разтворите.
Това са логаритмични скали, използвани за измерване на киселинния и основния характер на пробата.
Стойностите, които ги съставят, варират от 0 до 14 и са получени от йонния баланс на водата.
Неутрален разтвор има рН 7. Стойности под 7 класифицират разтворите като киселинни, докато след 7 разтворите са основни.
Със стойността на рН е възможно да се намери съответната по скалата pOH, само като се извади.
Йонен воден баланс
Водната молекула има способността да се йонизира съгласно уравнението:
Тук имаме йонен баланс, тъй като процесът е обратим и йоните също могат да се обединят и отново да образуват водна молекула.
Друг начин за демонстриране на баланса, който се получава, е чрез автоионизация.
Водна молекула генерира хидрониеви йони (H3О+) и хидроксил (OH-) чрез разрушаване на втора молекула.
Йонен продукт на водата (Kw)
Константата за йонния баланс на водата е:
Тъй като водата е чиста течност, нейната концентрация се приема за 1 и не пречи на постоянната стойност. Следователно изразът става:
О йонен продукт на Вода é .
Този израз получава символа Kw (W идва от английската дума water - вода) и подобно на равновесната константа, тя варира в зависимост от температурата.

Определяне на pH и pOH
При температура 25 ° C йонният продукт на водата е:
При йонизацията на чиста вода 1 mol H3О+ се образува с 1 mol OH- .
Скоро,
Тъй като тези стойности са изключително ниски, беше решено да се използват стойностите на кологаритмите, които съответстват на логаритъма със заменен знак.
Прилагайки кологаритъма към йонния продукт на водата, трябва да:
Можем да забележим, че: ако знаем рН на разтвор, стойността на pOH може да бъде намерена чрез изваждане на първата стойност от 14.
Киселинност и основност на разтворите
Неутрално решение: концентрацията на хидрониеви йони е равна на тази на хидроксилите.
| [H3О+] = 1,0. 10-7 mol / L | рН = 7 |
| [о-] = 1,0. 10-7 mol / L | pOH = 7 |
Пример: чиста вода.
киселинен разтвор: концентрацията на хидрониеви йони е по-голяма от тази на хидроксилите.
| [H3О+] |
рН |
| [о-] |
pOH |
Пример: сода, лимон и домат.
основно решение: концентрацията на хидроксили е по-голяма от тази на хидрониевите йони.
| [H3О+] |
рН |
| [о-] |
pOH |
Пример: яйце, сапун и белина.
изчисление на pH
Концепцията за хидрогенен потенциал е създадена от датския химик Петер Лауриц Соренсен (1868-1939), за да изрази киселинността на разтвора чрез концентрацията на Н+.
Вижте таблицата по-долу, показваща йонизацията на a киселина:
| Първоначална моларност | 0,020 | 0 | 0 |
| йонизация | 0,001 | 0,001 | 0,001 |
| Моларност в баланса | 0,019 | 0,001 | 0,001 |
В примера имаме, че концентрацията на H йони+ é 0,001. Следователно, рН на разтвора е:
[H+] = 0,001 = 10-3
pH = - log 10-3 = 3
Тъй като рН на разтвора е по-малко от 7, този разтвор е кисел.
Обобщение на pH и pOH
| Дефиниции | pH: водороден йон потенциал на разтвора. | |
|---|---|---|
| pOH: хидроксилен потенциал на разтвора. | ||
| обща формула | pH + pOH = 14 | |
| Решения | Неутрален | рН = pOH = 7 |
| кисела |
рН pOH> 7 |
|
| Основи |
pOH рН> 7 |
|
| изчисление на pH | pH = - log [H+] | |
| Изчисляване на pOH | pOH = -log [OH-] |
Упражнения за pH и pOH
1. (FMTM) рН на стомашния сок, воден разтвор на солна киселина (HCℓ), е приблизително 2. Следователно, масата, в грамове, HCℓ, съществуваща във всеки литър стомашен сок, е
Данни: Моларни маси (g / mol) H = 1, Cℓ = 35,5
а) 7,3 · 10-2
б) 3.65 · 10-1
в) 10-2
г) 2
д) 10
Правилна алтернатива: б) 3.65 · 10-1.
1-ва стъпка: изчислете концентрацията на H-йони+.
2-ра стъпка: изчислява се моларната маса на HCl.
3-та стъпка: изчислете масата на солната киселина във всеки литър стомашен сок.
2. (UEMG) Няколко почистващи продукта имат амоняк в състава си. Етикетът на един от тези продукти показва рН = 11. Това означава, че концентрацията на хидроксониеви катиони и хидроксилни аниони в този продукт са съответно:
до 1. 10-3 и 1. 10-11
б) 1. 10-11 и 1. 10-7
в) 1. 10-11 и 1. 10-3
г) 1. 10-11 и 1. 10-11
Правилна алтернатива: в) 1. 10-11 и 1. 10-3.
а) ГРЕШНО. Тези концентрации съответстват на разтвор с рН = 3.
б) ГРЕШНО. Въпреки че концентрацията на Н+ показват, че рН на разтвора е 11, концентрацията на OH йони- е погрешно, тъй като трябва да е 3, тъй като: pOH = 14 - pH.
в) ПРАВИЛНО. pH = 11 и pOH = 3, тъй като pH + pOH = 14.
г) ГРЕШНО. Въпреки че концентрацията на Н+ показват, че рН на разтвора е 11, концентрацията на OH йони- е погрешно, тъй като трябва да е 3, тъй като: pOH = 14 - pH.
а) 0,1 mol / L NaOH
б) NaCl 0,5 mol / L
в) Н2САМО4 1,0 mol / L
г) 1,0 mol / L HCl
д) 0,2 mol / L KOH
Правилна алтернатива: д) KOH 0,2 mol / L.
а) ГРЕШНО. Разтворът е основен, тъй като неговото рН е по-голямо от 7, но няма по-високо рН на алтернативите.
б) ГРЕШНО. NaCl е сол, тъй като е продукт на силна киселинна и алкална реакция. Следователно неговото рН е неутрално.
в) ГРЕШНО. Сярната киселина е силна киселина, така че нейното рН е ниско.
г) ГРЕШНО. Солната киселина е силна киселина, така че нейното рН е ниско.
д) ПРАВИЛНО. Разтворът е основен, тъй като рН е по-голямо от 7.