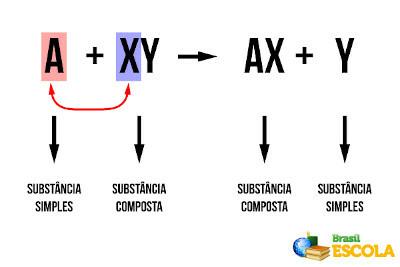
Редукционните реакции включват трансфер на електрони между атоми, йони или молекули.
При реакция на окисление-редукция настъпват промени в окислителното число (nox). Окислението се състои от процесите на окисление и редукция:
- Окисление: резултати в загуба на електрони и увеличен nox.
- Намаляване: резултати в печалба на електрон и намален nox.
Тъй като един елемент се отказва от електрони, друг ще ги получи. По този начин общият брой получени електрони е равен на общия брой загубени електрони.
Примери за окислително-редукционни реакции при горене, корозия и фотосинтеза.
Примери
В зависимост от елемента, който приема или дарява електрони, имаме следните имена:
- Редуциращ агент: Този, който претърпява окисление, причинява редукция и увеличава своя nox брой. Това е, което губи електрони.
- Оксидиращ агент: Този, който претърпява редукция, причинява окисляване и намалява неговото nox число. Това е, което печели електрони.
О окислително число представлява електрическия заряд на елемент в момента, в който той участва в a химическа връзка.
Това състояние е свързано с електроотрицателност, което е тенденцията на някои елементи да получават електрони.
1. Наблюдавайте първия пример, обърнете внимание, че в реакцията между желязото и хлора има промяна в окислителното число. О хлор тъй като е по-електроотрицателен, той печели електрони:
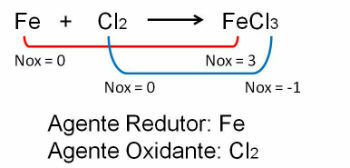
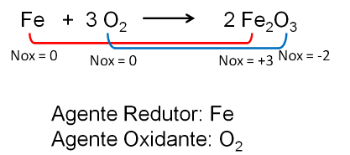
2. Реакция между желязо и кислород. Кислородът е по-електроотрицателен и в крайна сметка получава електрони и намалява окислителното им число.
Научете повече, прочетете също:
- Окисление
- Изгаряне
- Химична реакция
- електрони
Упражнението е решено
1. (PUC-RS) Във връзка с уравнението за окисление - небалансирана редукция Fe0 + CuSO4 → Fe2(САМО4)3 + Cu0, може да се каже, че:
а) окислителното число на медта в меден сулфат е +1.
б) железният атом губи 2 електрона.
в) медта претърпява окисляване.
г) желязото е окислител.
д) желязото претърпява окисляване.
Резолюция:
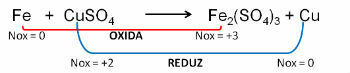
Отговор:
д) желязото претърпява окисляване.
Упражнения
1. (UFAC-AC) В следното химическо уравнение: Zn + 2 HCℓ → ZnCℓ2 + Н2
а) елементът Zn се окислява и реагира като окислител.
б) елементът Zn се окислява и реагира като редуциращ агент.
в) елементът Zn редуцира и реагира като редуктор.
г) HCℓ е редуциращ агент.
д) уравнението е класифицирано като обратимо.
б) елементът Zn се окислява и реагира като редуциращ агент.
2. (ITA-SP) В йонната реакция Ni (s) + Cu2+(aq) → Ni2+(aq) + Cu (s)
а) никелът е окислителят, защото е окислен.
б) никелът е редукторът, защото е окислен.
в) медният йон е окислителят, защото е окислен.
г) медният йон е редукторът, защото е редуциран.
д) това не е редокс реакция, следователно няма окислител или редуктор.
б) никелът е редукторът, защото е окислен.
3. (UFRGS) Активното вещество в домакинските белини е хипохлоритният йон, ClO-. В процесите на избелване този йон се редуцира; Това означава, че:
а) веществото, което претърпява действието на хипохлорит, получава електрони.
б) има намаляване на броя на електроните в неговата структура.
в) ClO- е редуциращ агент.
г) ClO- се превръща в елементарен хлор или хлориден йон.
д) не се извършва електронен трансфер.
г) ClO- се превръща в елементарен хлор или хлориден йон.