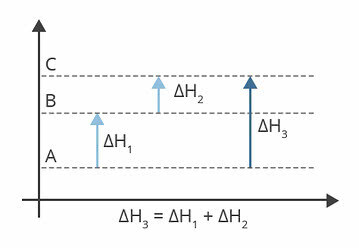
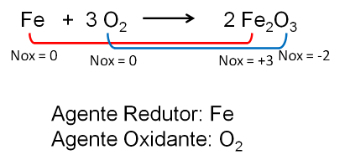
Реакциите на окислително-редукционни изследвания, изучавани главно във Физическата химия, са тези, при които се получава електронен трансфер. Реагиращият вид (атом, йон или молекула), който губи един или повече електрони, е този, който се подлага на окисление. Химичните видове, които получават електрони, от друга страна, са намалени.
Като цяло, когато този тип реакция се изучава в неорганичната химия, тя се нарича проста реакция на обмен или на изместване.
За да се осъществи реакция е необходимо да се изпълнят определени условия. Едно от тях е, че трябва да има химичен афинитет между реактивите, тоест те трябва да си взаимодействат по такъв начин, че да позволяват образуването на нови вещества.
В случай на окислително-редукционни реакции афинитетът означава, че единият от реагентите има тенденция да печели електрони, а другият да губи електрони. Тази тенденция съответства на реактивност на участващите химични елементи.
Нека да видим как е възможно да се сравни реактивността между металите.
Да приемем, че искаме да съхраняваме разтвор на меден II сулфат (CuSO
4). Не бихме могли да поставим този разтвор в алуминиев съд, защото ще се получи следната реакция:2 Ал(с) + 3 CuSO4 (aq)→ 3 Cu(с) + Ал2(САМО4)3 (aq)
Имайте предвид, че алуминият се е окислил, губейки по 3 електрона всеки и ставайки алуминиев катион:
Ал(с) → Ал3+(тук) + 3 и-
Едновременно с това медният катион (Cu2+), който присъства в разтвора, получава електрони от алуминий и редуцира, превръщайки се в метална мед. Всеки меден катион получава два електрона:
Задник2+(тук) + 2 и- → Cu(с)
Ако обаче беше обратното и искахме да съхраняваме разтвор на алуминиев сулфат (Al2(САМО4)3 (aq)), не би било проблем да го поставите в меден съд, тъй като тази реакция няма да настъпи:
Задник(с) + Ал2(САМО4)3 (aq) → не се случва
Тези наблюдавани факти могат да се обяснят с факта, че алуминият е по-реактивен от медта.
Металите имат тенденция да се отказват от електроните, тоест да се окисляват. Когато сравнявате различни метали, този с най-голяма тенденция да дарява електрони е най-реактивен. Следователно, реактивността на металите също е свързана с тяхната йонизационна енергия, тоест минималната енергия, необходима за отстраняване на електрон от газообразния атом в основно състояние.
Не спирайте сега... Има още след рекламата;)

Въз основа на това, опашка за реактивност на метали или ред електролитни напрежения, показано по-долу:
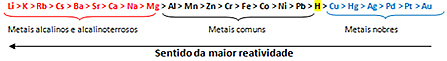
Най-реактивният метал реагира с йонни вещества, чиито катиони са по-слабо реактивни. С други думи, металът вляво реагира с веществото, образувано от йони вдясно. Обратното не се случва.
Спомняйки си дадения пример, вижте в реда за реактивност, че алуминият (Al) е вляво от медта (Cu). Следователно алуминият реагира с разтвора, образуван от медни катиони; но медта не реагира с разтвор, образуван от алуминиеви катиони.
Имайте предвид, че най-реактивният метал е литий (Li), а най-слабо реактивен е златото (Au).

Това е една от причините, поради които златото е толкова ценно, защото ако не реагира, то остава непокътнато дълго време. Това може да се види в покритите със злато египетски саркофази и скулптури, които датират от най-отдалечената древност. Това виждаме и когато сравняваме трайността на бижута от чисто злато с бижута, изработени от други метали, които са по-реактивни от златото.

От Дженифър Фогаса
Завършва химия
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
FOGAÇA, Дженифър Роча Варгас. „Ред на реактивност на металите“; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm. Достъп на 28 юни 2021 г.