ปฏิกิริยาฮาโลเจนเป็นปฏิกิริยาการแทนที่สารอินทรีย์ชนิดหนึ่ง กล่าวคือ ปฏิกิริยาที่ a อะตอมหรือกลุ่มของอะตอมจะถูกแทนที่ด้วยอะตอมหรือกลุ่มของอะตอมของโมเลกุลอื่น โดยธรรมชาติ.
โดยทั่วไป ปฏิกิริยาประเภทนี้เกิดขึ้นกับอัลเคนและอะโรมาติกไฮโดรคาร์บอน (เบนซีนและอนุพันธ์ของมัน)
เรียกว่าฮาโลเจนเนื่องจากเกิดขึ้นกับสารอย่างง่ายของฮาโลเจน: F2, Cl2, br2 เฮ้2. อย่างไรก็ตาม คลอรีนที่พบได้บ่อยที่สุด (Cl2) และโบรมิเนชัน (Br2) เนื่องจากฟลูออรีนมีปฏิกิริยาไว และปฏิกิริยาของมันระเบิดได้และควบคุมได้ยาก แม้กระทั่งทำลายอินทรียวัตถุ:
CH4(ก.) + 2 F2(ก.) → C(ส) + 4HF(ช)
ปฏิกิริยากับไอโอดีนจะช้ามาก
ด้านล่างนี้คือประเภทหลักของฮาโลเจนและตัวอย่างบางส่วน:
1. ฮาโลเจนกับอัลเคน: เนื่องจากอัลเคนมีปฏิกิริยาได้ไม่ดี ปฏิกิริยาฮาโลเจนของพวกมันจะเกิดขึ้นในที่ที่มีแสงแดดส่องถึง (λ) แสงอัลตราไวโอเลตหรือความร้อนสูงเท่านั้น ปฏิกิริยาประเภทนี้ทำขึ้นเพื่อให้ได้อัลคิลเฮไลด์
ตัวอย่าง: มีเทนโมโนคลอรีน:
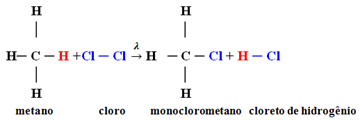
ในกรณีนี้เกิดขึ้นจากอะตอมไฮโดรเจนของมีเทน (CH4) ถูกแทนที่ด้วยอะตอมของคลอรีน ให้โมโนคลอโรมีเทน หากมีคลอรีนมากเกินไป ปฏิกิริยานี้สามารถดำเนินการต่อไป โดยแทนที่ไฮโดรเจนทั้งหมดในมีเทน
1.1. ฮาโลเจนในอัลเคนที่มีคาร์บอนมากกว่า 3 ตัว: ถ้าอัลเคนที่จะทำปฏิกิริยามีอะตอมของคาร์บอนอย่างน้อย 3 อะตอม เราก็จะได้ส่วนผสมของสารประกอบที่ถูกแทนที่ที่แตกต่างกัน ดูตัวอย่างด้านล่างของเมทิลบิวเทนโมโนคลอรีน:
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
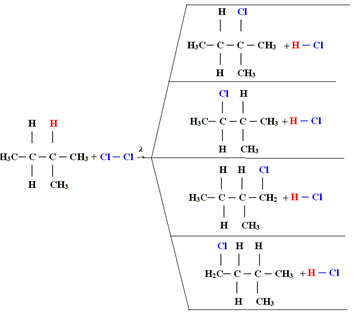
ปริมาณของสารประกอบแต่ละชนิดจะเป็นสัดส่วนกับลำดับความง่ายต่อไปนี้ซึ่งไฮโดรเจนถูกปล่อยออกสู่โมเลกุล:

ดังนั้น ในกรณีข้างต้น ปริมาณที่มากที่สุดจะเป็น 2-เมทิล-2-คลอโรบิวเทน และปริมาณที่น้อยที่สุดจะเป็น 2-เมทิล-1-คลอโรบิวเทน
2. เบนซีนฮาโลเจน: เบนซินมักไม่ทำปฏิกิริยากับคลอรีนหรือโบรมีน อย่างไรก็ตาม หากใช้กรดลูอิสเป็นตัวเร่งปฏิกิริยา (โดยปกติจะใช้ FeClCl3, กุมภาพันธ์3 หรือ AlCl3ทั้งหมดอยู่ในรูปแบบปราศจากน้ำ) เบนซินทำปฏิกิริยาได้ง่ายในปฏิกิริยาฮาโลเจน
คลอไรด์และเฟอริกโบรไมด์สามารถได้มาโดยเพียงแค่เติมธาตุเหล็กลงในของผสม และด้วยวิธีนี้จะทำให้ทำปฏิกิริยากับฮาโลเจนและผลิตกรดลิวอิส:
2 เฟ + 3 ห้องนอน2 → 2 ก.พ.3
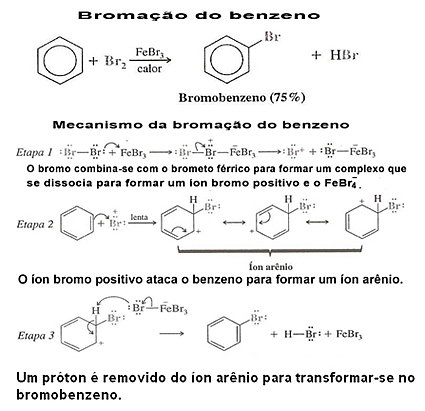
ดูตัวอย่างของเบนซีนฮาโลเจนและกลไกของมัน:
3. ฮาโลเจนของอนุพันธ์เบนซีน:ในกรณีดังกล่าว การแทนที่ถูกชี้นำโดยหมู่แทนที่หรือหมู่ฟังก์ชันที่ยึดติดกับนิวเคลียสอะโรมาติก หากต้องการดูว่าสิ่งนี้เกิดขึ้นได้อย่างไร โปรดอ่านข้อความ "สารก่อภูมิแพ้ในวงแหวนเบนซีน"และ"ผลกระทบทางอิเล็กทรอนิกส์ของอนุมูลเมตาและออร์โธต่อกรรมการ”.
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ปฏิกิริยาฮาโลเจนอินทรีย์"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.