THE auto-oxi-reduction หรือปฏิกิริยาที่ไม่สมส่วน เป็นปฏิกิริยารีดอกซ์ชนิดหนึ่งซึ่งมีองค์ประกอบทางเคมีเดียวกันผ่าน ออกซิเดชัน และการลดลง ลองดูตัวอย่างสองตัวอย่างของปฏิกิริยาประเภทนี้และวิธีปรับสมดุลโดยใช้วิธีรีดอกซ์:
ตัวอย่างที่ 1:
ที่2- + โฮ+ → ไม่3- + ไม่ + H2โอ
- โดยการคำนวณเลขออกซิเดชัน (NOX) ของอะตอมและไอออนทั้งหมดที่เกี่ยวข้องกับปฏิกิริยา สามารถตรวจสอบได้ว่าใครถูกออกซิไดซ์และใครทำปฏิกิริยา:
+3 -2 +1 +5 -2 +2 -2 +1 -2
ที่2- + โฮ+ → ไม่3- + ไม่ + H2โอ
- โปรดทราบว่าไนโตรเจนเป็นสปีชีส์ที่ทำปฏิกิริยาและออกซิไดซ์:
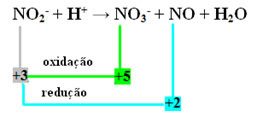
- เพื่อให้สมดุลของปฏิกิริยานี้โดยรีดอกซ์ เราต้องเชื่อมโยง NOX กับผลิตภัณฑ์ ไม่ใช่รีเอเจนต์:
ที่3- =∆น็อกซ์ = 5 - 3 = 2
NO=∆Nox = 3 - 2 = 1
- การกลับค่า ∆NOX ด้วยสัมประสิทธิ์ เรามี:
ที่3- =∆NOX= 2 → 2 จะเป็นสัมประสิทธิ์ของ NO
ไม่=∆NOX= 1→ 1 จะเป็นสัมประสิทธิ์ของ NO3-
ที่2- + โฮ+ → 1 ที่3- + 2 NO+H2โอ
- ด้วยเหตุนี้เราจึงทราบแล้วว่าในผลิตภัณฑ์มี 3 N ดังนั้นสัมประสิทธิ์ของ NO2- จะเป็น 3:
3 ไม่2- + โฮ+ → 1 ไม่3- + 2 ไม่ + H2โอ
- เพื่อกำหนดสัมประสิทธิ์ของH+ และจาก H2O จำไว้ว่าจำนวนอิเล็กตรอนที่ได้รับเท่ากับจำนวนอิเล็กตรอนที่บริจาคเท่ากัน ดังนั้นค่ารีเอเจนต์จะเท่ากับค่าผลิตภัณฑ์ ด้วยวิธีนี้ เราสามารถสร้างโครงร่างต่อไปนี้:
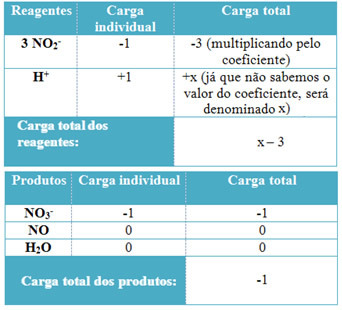
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
จากข้อมูลนี้ เรามีประจุรวมของรีเอเจนต์เท่ากับ x – 3 และได้ผลผลิตเท่ากับ -1. ตามที่ระบุไว้ค่าใช้จ่ายของทั้งสองจะต้องเท่ากัน เนื่องจากเรามีโหลดผลิตภัณฑ์ทั้งหมดแล้ว เราจึงสามารถคำนวณง่ายๆ เพื่อทราบว่าค่าของ x จะเป็นเท่าใด:
x -3 = -1
x = -1 +3
x = 2
ดังนั้นสัมประสิทธิ์ของ H+ เป็น 2 และดังนั้น ของ H2จะเป็น 1:
3 ไม่2- + 2 ชั่วโมง+ → 1 ไม่3- + 2 ไม่ + 1 ชั่วโมง2โอ
ตัวอย่างที่ 2:
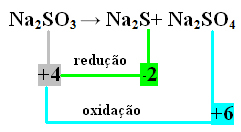
ในกรณีนี้ มันคือ S ที่รับการรีดักชันและออกซิเดชันในเวลาเดียวกัน ดังนั้น ดังที่เคยทำมาก่อนหน้านี้ เราสามารถเชื่อมโยง NOX กับผลิตภัณฑ์และกลับค่าของพวกมัน โดยกำหนดค่าสัมประสิทธิ์ให้กับพวกมัน:
ที่2 S=∆Nox = 4 – (-2) = 6 → 6 จะเป็นสัมประสิทธิ์ของ Na2 เท่านั้น4
ที่2 เท่านั้น4=∆Nox = 6 - 4 = 2 → 2 จะเป็นสัมประสิทธิ์ของ Na2 ส
ที่2 เท่านั้น3→ 2 ที่2 Y+ 6 ที่2 เท่านั้น4
เนื่องจากมีกำมะถันอยู่ 8 ตัวในกิ่งที่ 2 สัมประสิทธิ์นา2 เท่านั้น3 จะเป็น 8:
8 ใน2 เท่านั้น3→ 2 ใน2 S + 6 ใน2 เท่านั้น4
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ปฏิกิริยาออกซิเดชันในตนเอง"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.


