กรดและเบสเป็นหน้าที่ทางเคมีสองอย่างที่ถือว่าตรงกันข้ามนี่เป็นเพราะคุณสมบัติของพวกมันมักจะผกผัน ตัวอย่างเช่น หากเราพิจารณาอาหารที่มีอยู่ในชีวิตประจำวันของเราที่เป็นกรด เราจะเห็นว่าโดยทั่วไปแล้วรสชาติของอาหารนั้นมีรสเปรี้ยวเช่นเดียวกับมะนาว อย่างไรก็ตาม อาหารที่เป็นพื้นฐานจะมีรสฝาด (ซึ่ง “จับ” ปาก) เช่น กล้วยเขียว
แต่การระบุสารที่เป็นกรดหรือด่างเพียงแค่รสรวมทั้งเป็นวิธีที่มีโอกาสล้มเหลวมาก นอกจากนี้ยังเป็นอันตรายอย่างมากเนื่องจากมีกรดและเบสจำนวนมากที่แข็งแรง เป็นพิษ และยังสามารถฆ่าได้ เช่น กรด กำมะถัน (H2เท่านั้น4) ใช้ในแบตเตอรี่รถยนต์ และโซเดียมไฮดรอกไซด์ (NaOH) ที่รู้จักกันในเชิงพาณิชย์ว่าโซดาไฟ
ดังนั้น คุณสมบัติทางประสาทสัมผัส (คุณสมบัติที่เกี่ยวข้องกับประสาทสัมผัสของเรา เช่น รสและกลิ่น) จึงไม่ใช่คุณสมบัติที่ใช้ในการระบุกรดและเบส หมายเหตุด้านล่างคุณสมบัติอื่น ๆ ของฟังก์ชันอินทรีย์เหล่านี้ที่ใช้เพื่อเปรียบเทียบและแยกแยะ:
- การละลายในน้ำ:
คุณ กรด มักจะสบายดี ละลายน้ำได้ ในน้ำในขณะที่ส่วนใหญ่ ฐาน é ไม่ละลายน้ำ. เบสโลหะอัลคาไลละลายได้ เบสโลหะอัลคาไลน์เอิร์ทละลายได้ไม่ดี และเบสจากโลหะอื่นไม่ละลายน้ำ (ยกเว้นแอมโมเนียมไฮดรอกไซด์ NH
4OH ซึ่งมีอยู่ในสารละลายที่เป็นน้ำเท่านั้น ทำให้ก๊าซแอมโมเนียเดือดปุด ๆ ในน้ำจึงละลายได้)เมื่อเราพูดว่า "ไม่ละลายน้ำ" เราหมายความว่าสารเหล่านี้แทบจะไม่ละลาย เนื่องจากไม่มีสารใดที่ไม่ละลายในน้ำอย่างสมบูรณ์
- โครงสร้าง:
ทั้งหมด กรดเป็นโมเลกุลนั่นคือเกิดขึ้นจากพันธะโควาเลนต์ซึ่งใช้อิเล็กตรอนร่วมกัน ตัวอย่างคือก๊าซไฮโดรคลอริกซึ่งเกิดขึ้นจากการใช้อิเล็กตรอนร่วมกันระหว่างไฮโดรเจนกับคลอรีน:

แล้ว เบสสามารถเป็นไอออนิกหรือโมเลกุล. ผู้ที่มีโลหะอัลคาไลและอัลคาไลน์เอิร์ ธ เป็นไอออนิกและอื่น ๆ เป็นโมเลกุล
ตัวอย่าง:
NaOH: ฐานไอออนิกที่เกิดจาก Na ไอออน+ และโอ้-;
NH4OH: ฐานโมเลกุลของแอมโมเนียในน้ำ
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
- การนำไฟฟ้า:
ทั้งหมด กรดจะนำกระแสไฟฟ้าเมื่อละลายในน้ำเท่านั้นเพราะเมื่อพวกมันอยู่ในตัวกลางที่เป็นน้ำ พวกมันจะถูกทำให้แตกตัวเป็นไอออน นั่นคือพวกมันจะปล่อยไอออน
ตัวอย่าง:
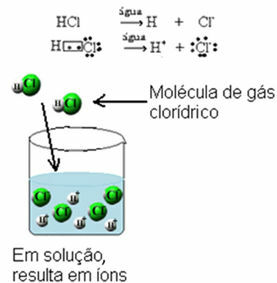
ทั้งหมด ฐานยังนำกระแสไฟฟ้าในสารละลายเนื่องจากไอออนิกเกิดการแตกตัว (ปล่อยไอออนที่มีอยู่แล้วในสูตร) และโมเลกุลได้รับการแตกตัวเป็นไอออน ทำปฏิกิริยากับน้ำและปล่อยไอออน ที่ ฐานโลหะอัลคาไลยังนำกระแสไฟฟ้าเมื่ออยู่ในสถานะของเหลว (หลอมเหลว)
- การดำเนินการกับตัวชี้วัด:
คุณ ตัวชี้วัดกรดเบส เป็นสารธรรมชาติหรือสารสังเคราะห์ที่มีการเปลี่ยนสีเมื่อสัมผัสกับกรดหรือเบส หากกรดทำให้ตัวบ่งชี้เปลี่ยนสี เบสจะทำให้ตัวบ่งชี้กลับเป็นสีเดิมและในทางกลับกัน
ตัวอย่างเช่น ฟีนอฟทาลีนเป็นตัวบ่งชี้ความเป็นกรด-เบสที่ใช้กันอย่างแพร่หลาย และในตัวกลางพื้นฐาน ฟีนอฟทาลีนจะกลายเป็นสีชมพูที่เข้มข้นมาก อยู่ในสื่อที่เป็นกรดก็จะกลายเป็นไม่มีสี กระดาษลิตมัสก็เป็นตัวบ่งชี้ที่ดีเช่นกัน เพราะในกรดจะเปลี่ยนเป็นสีแดง และบนฐานเดียว มันจะกลายเป็นสีน้ำเงิน
นอกจากนี้ยังใช้เพื่อระบุความแตกต่างของค่า pH ที่มีอยู่ระหว่างกรดและเบส
- พีเอช:
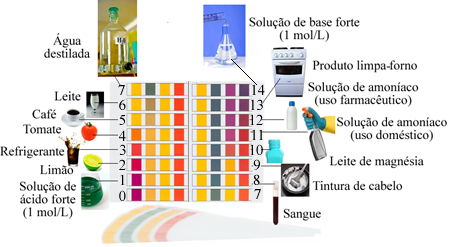
ตัวกลางที่ถือว่าเป็นกลางมีค่า pH เท่ากับ 7 เช่นเดียวกับน้ำกลั่น
กรดมีค่า pH น้อยกว่า 7, ในขณะที่ เบสมีค่า pH มากกว่า 7
ตัวอย่างของสารละลายที่มีค่า pH ใกล้เคียงกับที่ระบุโดยมาตราส่วน:
- การกระทำซึ่งกันและกัน:
เมื่อสัมผัสกัน กรดและเบสจะทำปฏิกิริยาซึ่งกันและกัน ทำให้เป็นกลางซึ่งกันและกัน กล่าวคือ ทำให้ pH ของตัวกลางเป็นกลาง นี่เป็นเพราะว่า H cation+ จากกรดทำปฏิกิริยากับ OH anion- จากฐานสร้างน้ำ ปฏิกิริยาประเภทนี้เรียกว่า a ปฏิกิริยาการวางตัวเป็นกลาง และยังผลิตเกลืออีกด้วย
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี