นักเคมีชาวอเมริกัน กิลเบิร์ต เอ็น. Lewis (1875-1946) เสนอกฎออกเตตซึ่งกล่าวว่า:
“อะตอมของธาตุต่าง ๆ จะสร้างพันธะเคมี การบริจาค รับหรือแบ่งปันอิเล็กตรอน เพื่อให้ได้มาซึ่งโครงแบบอิเล็กทรอนิกส์ของ ก๊าซมีตระกูล กล่าวคือ มีอิเล็กตรอน 8 ตัวในเปลือกสุดท้าย (หรือมีอิเล็กตรอน 2 ตัวในกรณีของอะตอมเหล่านั้นที่มีอิเล็กตรอนเพียงเปลือกเดียว ดังที่เกิดขึ้นกับ ไฮโดรเจน)"
ในปี ค.ศ. 1916 ลูอิสเสนอว่าให้คงตัวไว้ โดยให้ไปถึงออคเต็ตหรือดูเอ็ท ซึ่งเป็นองค์ประกอบที่ประกอบเป็น สารโมเลกุล ทำการแบ่งปันอิเล็กตรอนคู่ สารเหล่านี้เกิดจากอะตอมของ .เท่านั้น ไฮโดรเจน อโลหะ และกึ่งโลหะ, ทั้งหมดด้วย แนวโน้มที่จะรับอิเล็กตรอน. ดังนั้นจึงไม่มีทางใดที่พวกเขาจะบริจาคอิเล็กตรอน (เช่นที่เกิดขึ้นกับโลหะในพันธะไอออนิก) แต่ ทุกคนต้องได้รับ ดังนั้นพวกเขาจึงแบ่งอิเล็กตรอนผ่านพันธะโควาเลนต์หรือ โมเลกุล
ดังนั้น กิลเบิร์ต ลูอิสจึงเสนอวิธีการแสดงพันธะโควาเลนต์หรือพันธะโมเลกุล ซึ่งต่อมารู้จักกันในชื่อ สูตรลูอิส. เธอยังถูกเรียกว่า สูตรอิเล็กทรอนิกส์ หรือยัง สูตรอิเล็กทรอนิกส์ของลูอิสเพราะลักษณะเด่นของมันคือ แสดงอิเล็กตรอนในเปลือกเวเลนซ์ของแต่ละอะตอมและการก่อตัวของคู่อิเล็กทรอนิกส์
อิเล็กตรอนแต่ละตัวจะแสดงด้วยจุดซึ่งล้อมรอบสัญลักษณ์ขององค์ประกอบทางเคมีที่สอดคล้องกัน มีเพียงอิเล็กตรอนของเปลือกเวเลนซ์เท่านั้นที่อยู่รอบองค์ประกอบ
ดังที่แสดงในตารางด้านล่าง หากต้องการทราบปริมาณอิเล็กตรอนในเปลือกเวเลนซ์ ให้รู้จักตระกูลตารางธาตุ:

ในสูตรของลูอิส แต่ละคู่อิเล็กตรอนที่ใช้ร่วมกันแสดงถึงพันธะเคมี (โควาเลนต์)), โดยที่อิเล็กตรอนมาบรรจบกันในบริเวณอิเล็กโตรสเฟียร์ซึ่งพบได้ทั่วไปในอะตอมแต่ละคู่ที่เชื่อมเข้าด้วยกัน ดังนั้นในการเป็นตัวแทนจึงวางเคียงข้างกัน
ตัวอย่างเช่น ลองหาว่าสูตรของลิวอิสสำหรับแก๊สไฮโดรเจนมีสูตรอย่างไร ซึ่งมีสูตรโมเลกุลคือ H2.
อะตอมของไฮโดรเจนแต่ละอะตอมมีอิเล็กตรอนเพียงตัวเดียวในเปลือกเวเลนซ์ เนื่องจากองค์ประกอบนี้เป็นของตระกูล 1 ของตารางธาตุ แต่ละคนต้องการรับอิเล็กตรอนเพิ่มอีก 1 ตัวเพื่อให้มีความเสถียร โดยมีอิเล็กตรอนสองตัวในเปลือกอิเล็กตรอน K ดังนั้นพวกเขาจึงแบ่งอิเลคตรอนและทั้งสองได้สอง ดู:
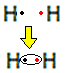
นี่คือสูตรของลิวอิสสำหรับโมเลกุลของก๊าซไฮโดรเจน
ออกซิเจนมีอิเล็กตรอน 6 ตัวในเปลือกอิเล็กตรอน ดังนั้นแต่ละตัวจึงต้องได้รับอิเล็กตรอนเพิ่มอีก 2 ตัวเพื่อให้มีความเสถียร โดยมีอิเล็กตรอน 8 ตัว ดังนั้นสูตรของลิวอิสสำหรับโมเลกุลของก๊าซออกซิเจนคือ:

เห็นว่ามีสองลิงก์ เนื่องจากมีคู่ที่ใช้ร่วมกันสองคู่
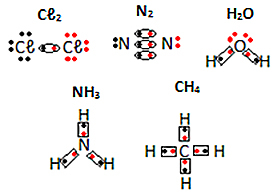
ดูตัวอย่างอื่นๆ ของสูตรอิเล็กทรอนิกส์ของสารโมเลกุลด้านล่าง:
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/formula-eletronica-lewis.htm
