เราจะเห็นในข้อความนี้ว่า a แผนภูมิของ การเปลี่ยนแปลงสภาพร่างกาย ถึงใด ๆ สารบริสุทธิ์วิธีตีความไดอะแกรมประเภทนี้และวิธีแสดงกราฟของสารผสม
ในการทำเช่นนี้ ให้พิจารณาตัวอย่างน้ำ ลองนึกภาพว่าเรานำน้ำแข็งหนึ่งแก้วที่อุณหภูมิ –10 ºC และเริ่มกระบวนการให้ความร้อนภายใต้แรงดัน 1 atm เมื่ออุณหภูมิเพิ่มขึ้น จาก -10 ºC ถึง -9 ºC ถึง -8 ºC เป็นต้น น้ำแข็งจะยังคงอยู่ในสถานะของแข็งจนกว่าจะถึงอุณหภูมิ 0 ºC
ณ จุดนี้มันเริ่มเปลี่ยนเป็นสถานะของเหลวนั่นคือการหลอมรวมเริ่มเกิดขึ้น อุณหภูมิจะไม่เพิ่มขึ้นเหมือนเดิม แต่จะคงที่ที่ 0 °C จนกว่าน้ำแข็งทั้งหมดจะละลาย:

หลังจากละลายของแข็งทั้งหมดแล้ว อุณหภูมิของระบบจะเพิ่มขึ้นเรื่อยๆ จนถึงอุณหภูมิ 100°C ที่อุณหภูมินี้ น้ำที่อยู่ในสถานะของเหลวจะเริ่มเปลี่ยนเป็นสถานะไอ กล่าวคือ มันจะเดือด
เช่นเดียวกับที่มันเกิดขึ้นใน จุดหลอมเหลวที่จุดเดือด อุณหภูมิจะคงที่จนกว่าของเหลวทั้งหมดจะเปลี่ยนเป็นไอ หลังจากนั้น หากเราให้ความร้อนแก่ระบบ อุณหภูมิก็จะสูงขึ้นต่อไป:
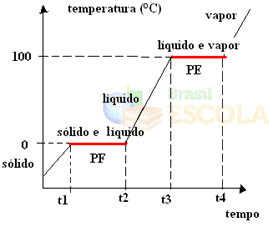
พร้อม! นี่คือกราฟหรือแผนภาพที่แสดงการเปลี่ยนแปลงในสถานะทางกายภาพของน้ำหรือกราฟความร้อนของน้ำ หากเป็นกระบวนการผกผัน เราจะมีเส้นโค้งการระบายความร้อนด้วยน้ำต่อไปนี้:
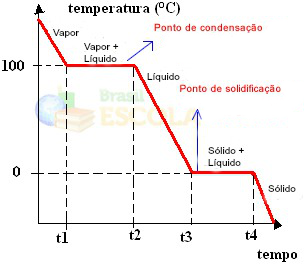
ลักษณะที่สำคัญมากของกราฟเหล่านี้คือกราฟเหล่านี้ประกอบด้วยสองระดับ กล่าวคือ มีจุดสองจุดที่อุณหภูมิคงที่ชั่วขณะหนึ่ง สิ่งนี้มักเกิดขึ้นในการเปลี่ยนแปลงสถานะของสารบริสุทธิ์ ข้อแตกต่างเพียงอย่างเดียวคือค่าจุดหลอมเหลวและจุดเดือด
ตัวอย่างเช่น ออกซิเจน ซึ่งแตกต่างจากน้ำ ไม่ใช่ของเหลว แต่เป็นก๊าซที่อุณหภูมิห้อง (ประมาณ 20ºC) เนื่องจากจุดหลอมเหลวที่ระดับน้ำทะเลอยู่ที่ -223.0 °C และจุดเดือดอยู่ที่ -183.0 °C ดูแผนภูมิการเปลี่ยนแปลงสถานะทางกายภาพของคุณ:

กราฟิกผสมทั่วไป
หากเรากำลังให้ความร้อนหรือทำให้ส่วนผสมเย็นลง จุดหลอมเหลวและจุดเดือดจะไม่มี ค่าที่กำหนดและค่าคงที่ กล่าวคือ ระดับสองระดับที่สังเกตได้ในกราฟจะไม่เกิดขึ้น ข้างบน.
การเปลี่ยนแปลงในสถานะทางกายภาพจะเกิดขึ้นในช่วงอุณหภูมิมากกว่าจำนวนคงที่ ตัวอย่างเช่น จุดหลอมเหลว จะเริ่มที่อุณหภูมิที่กำหนดและสิ้นสุดที่จุดอื่น และเช่นเดียวกันจะเกิดขึ้นกับจุดเดือด ดังแสดงในกราฟต่อไปนี้:
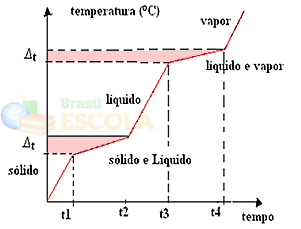
ข้อยกเว้นสองประการคือส่วนผสมของยูเทคติกและอะซีโอทรอปิก ดูว่าเกิดอะไรขึ้นกับพวกเขา:
ก) ส่วนผสมยูเทคติก
ส่วนผสมยูเทคติกมีพฤติกรรมราวกับว่าเป็นสารบริสุทธิ์ในระหว่างการหลอมรวม นั่นคือ ณ จุดนั้น อุณหภูมิจะคงที่ตั้งแต่ต้นจนจบการเปลี่ยนแปลงสถานะของการรวมกลุ่ม

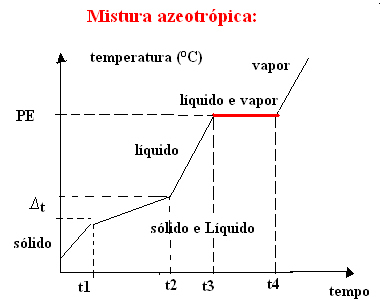
b) ส่วนผสม azeotropic
ส่วนผสม azeotropic มีลักษณะเหมือนสารบริสุทธิ์ในระหว่างการเดือด นั่นคือ ณ จุดนี้ อุณหภูมิจะคงที่ตั้งแต่ต้นจนจบการเปลี่ยนแปลงในสถานะการรวมตัว
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm
