อลูมิเนียมได้มาจากกระบวนการทางโลหะวิทยา โลหะวิทยาเป็นพื้นที่ที่ศึกษาการเปลี่ยนแปลงของแร่เป็นโลหะหรือโลหะผสม วิธีนี้ได้โลหะหลายชนิด เช่น ทองแดง ไททาเนียม เหล็ก และแมงกานีส
ในกรณีของอะลูมิเนียม แร่หลักที่ใช้คือ บอกไซต์ (รูป) ซึ่งมีอะลูมิเนียมออกไซด์ไฮเดรต (Aℓ2โอ3. x โฮ2O) และสิ่งสกปรกต่างๆ

ในโลหะวิทยาอลูมิเนียมมีสี่ขั้นตอนต่อไปนี้เกิดขึ้น:
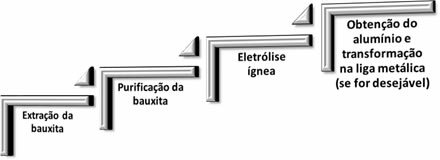
เมื่ออะลูมิเนียมออกไซด์ (Aℓ2โอ3(s)) แยกจากอะลูมิเนียม เปลี่ยนชื่อเป็น อลูมินา.
ก่อนหน้านี้ ทำสิ่งต่อไปนี้: อลูมินาได้รับการบำบัดด้วยกรดไฮโดรคลอริกเพื่อสร้างอะลูมิเนียมคลอไรด์ ซึ่งถูกนำไปทำปฏิกิริยากับโลหะโพแทสเซียมหรือโซเดียมทำให้สารประกอบลดลงและทำให้เกิดอะลูมิเนียมโลหะ:
อา2โอ3(s) + 6 HCℓ(ที่นี่)→ 4 AℓCℓ3(aq) + 3 ชั่วโมง2โอ(ℓ)
ACℓ3(aq) + 3K(ส)→ 3 KCℓ(ส) + อา(ส)
อย่างไรก็ตาม วิธีนี้มีราคาแพงมากและไม่มีประสิทธิภาพ ดังนั้นอะลูมิเนียมจึงถือเป็นโลหะหายาก
แต่ในปี พ.ศ. 2429 นักวิทยาศาสตร์สองคนได้พัฒนาวิธีการที่กล่าวถึงข้างต้นแยกจากกัน ซึ่งใช้อิเล็กโทรไลซิสแบบอัคนี นักวิทยาศาสตร์เหล่านี้คือ American Charles M. Hall และ Paul Héroult ชาวฝรั่งเศสจึงเรียกวิธีนี้ว่า กระบวนการ Hall-Héroult หรือง่ายๆกระบวนการฮอลล์ในขณะที่ Charles M. ฮอลล์จดสิทธิบัตรไว้
ประเด็นสำคัญที่พวกเขาค้นพบคือวิธีทำอะลูมิเนียมออกไซด์เหลว สามารถทำอิเล็กโทรไลซิสแบบอัคนีได้ เนื่องจากปัญหาอยู่ที่จุดหลอมเหลวสูงกว่า 2000 องศาเซลเซียส พวกเขาใช้ฟลักซ์แร่ไครโอไลต์ (Na3อัฟฟ6) ซึ่งสามารถลดอุณหภูมิหลอมเหลวของอะลูมิเนียมออกไซด์ลงเหลือประมาณ 1,000 °C
ดังที่แสดงในแผนภาพด้านล่าง ส่วนผสมของอะลูมิเนียมออกไซด์และไครโอไลต์นี้จึงถูกใส่ลงในภาชนะอิเล็กโทรไลต์ที่ทำจากเหล็กกล้าที่มีคาร์บอน กระแสไฟฟ้าไหลผ่านส่วนผสมที่หลอมเหลวนี้ ผนังของภาชนะที่สัมผัสกับส่วนผสมทำหน้าที่เป็นขั้วลบของอิเล็กโทรไลซิส (แคโทด) ซึ่งจะมีการลดลงของไพเพอร์อะลูมิเนียม ขั้วบวก (ขั้วบวก) เป็นกระบอกสูบที่ทำจากกราไฟท์หรือคาร์บอน นั่นคือ ทั้งสองทำจากคาร์บอน ซึ่งเกิดออกซิเดชันของออกซิเจนแอนไอออน:
ปฏิกิริยาครึ่งแคโทด: 4 Aℓ3+(ℓ) + 12 และ- → 4 Aℓ(ℓ)
แอโนดครึ่งปฏิกิริยา: 6 O2-(ℓ) → 12 และ- + 3 ออน2(ก.)
ออกซิเจนที่เกิดขึ้นทำปฏิกิริยากับคาร์บอนในแอโนดและยังสร้างคาร์บอนไดออกไซด์อีกด้วย:
3 ออนซ์2(ก.) + 3 C(ส) → 3 CO2(ก.)
ดังนั้น ปฏิกิริยาโดยรวมและโครงร่างของอิเล็กโทรไลซิสแบบอัคนีที่ก่อให้เกิดอะลูมิเนียมได้มาจาก:

อลูมิเนียมที่ได้รับจะอยู่ในรูปของเหลว เนื่องจากจุดหลอมเหลวของมันคือ 660.37 ºC ซึ่งต่ำกว่าของผสมของอลูมินาและไครโอไลต์ อลูมิเนียมยังมีความหนาแน่นมากกว่าส่วนผสมและดังนั้นจึงถูกวางที่ด้านล่างของภาชนะซึ่งจะถูกรวบรวม
ใช้ในการผลิตอลูมิเนียม 1 ตัน:
- บอกไซต์ 4-5 ตัน, จากที่เกี่ยวกับ อลูมินา 2 ตัน;
- ไครโอไลท์ 50 กิโลกรัม (มีไครโอไลต์สำรองตามธรรมชาติไม่มากนัก ดังนั้นจึงมักได้มาจากการสังเคราะห์จากฟลูออไรต์ (CaF2) แร่ธาตุที่มีมากที่สุดในธรรมชาติ);
- ถ่านหิน 0.6 ตัน สำหรับอิเล็กโทรด
การผลิตอลูมิเนียมต่อปีเกิน 27.4 ล้านตัน.
ในบรรดาโลหะผสมอลูมิเนียมหลัก เรามีดังต่อไปนี้:

โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/obtencao-aluminio-por-meio-eletrolise.htm
