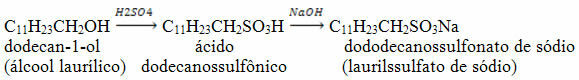การให้น้ำของอัลไคน์เป็นปฏิกิริยาของการเติมโมเลกุลของน้ำในตัวกลางที่เป็นกรดต่อหน้าตัวเร่งปฏิกิริยา HgSO4.
ปฏิกิริยาเหล่านี้มีความสำคัญเนื่องจากสามารถได้รับอัลดีไฮด์และคีโตนผ่านพวกมัน
สารประกอบอัลดีไฮด์เป็นสารประกอบอินทรีย์ที่มีหมู่คาร์บอนิลติดอยู่กับไฮโดรเจน ในทางกลับกัน คีโตนมีหมู่คาร์บอนิลระหว่างสองคาร์บอน ดังที่แสดงโดยกลุ่มฟังก์ชันด้านล่าง:
อัลดีไฮด์: คีโตน:
โอโอ
║║
เอช ─ ค ─ C ─ ค ─C
ถ้าอัลไคน์ที่ทำปฏิกิริยาไฮเดรชั่นคืออีเทน เราจะมีการก่อตัวของอัลดีไฮด์ เอทานัล เริ่มแรกจะเกิดสารประกอบขั้นกลางที่มีชื่อสามัญของอีนอล
อีนอลนี้เป็นสารประกอบที่ไม่เสถียรมากซึ่งผ่านการจัดเรียงโมเลกุลใหม่เนื่องจากมีอิเล็กโตรเนกาติวีตี้สูงของ ออกซิเจนทำให้เกิดแรงดึงดูดของอิเล็กตรอนจากพันธะคู่ของคาร์บอน ซึ่งเป็นพันธะที่อ่อนแอและง่าย ย้าย. ด้วยวิธีนี้ enol และ aldehyde จะอยู่ร่วมกันในสมดุลไดนามิก ปรากฏการณ์นี้เป็นกรณีของ aldoenolic tautomeria:
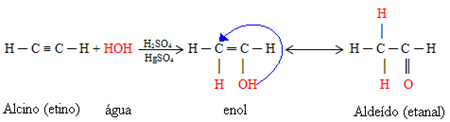
อย่างไรก็ตาม หากใช้อัลไคน์อื่นที่มีคาร์บอนสามตัวขึ้นไป คีโตนที่สอดคล้องกันจะก่อตัวขึ้น ทั้งนี้เป็นเพราะปฏิกิริยานี้เป็นไปตาม กฎของมาร์คอฟนิคอฟซึ่งบอกว่าไฮโดรเจนในน้ำจะเพิ่มคาร์บอนพันธะสามที่มีมากที่สุด ไฮโดรเจนถูกพันธะกับมัน ในขณะที่ OH ในน้ำจะจับกับพันธะสามลบด้วยคาร์บอน เติมไฮโดรเจน

โพรพาโนนเป็นอะซิโตน ใช้สำหรับขจัดยาทาเล็บ
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/hidratacao-alcinos.htm