การวิเคราะห์คุณสมบัติทางกายภาพและทางเคมีของสารประกอบที่ทำพันธะโควาเลนต์ (โดยใช้อิเล็กตรอนร่วมกัน) แสดงให้เราเห็นว่าวัสดุเหล่านี้มีความแตกต่างกันอย่างมาก แต่ก่อนที่เราจะมาดูลักษณะเหล่านี้ เรามาดูกันว่าสารโมเลกุลและสารโควาเลนต์แตกต่างกันอย่างไร
ที่ สารโมเลกุล พวกมันเป็นสิ่งที่เกิดขึ้นเมื่ออะตอมเชื่อมโยงกันผ่านพันธะโควาเลนต์ทำให้เกิดโมเลกุลของจำนวนที่กำหนด
อย่างไรก็ตาม พันธะโควาเลนต์ยังสามารถก่อกำเนิดสารประกอบในโครงสร้างเครือข่ายที่มีอะตอมจำนวนมากและไม่ทราบแน่ชัด ซึ่งก็คือ โมเลกุลขนาดใหญ่. สารดังกล่าวเรียกว่า สารประกอบโควาเลนต์ หรือ ของแข็งเครือข่ายโควาเลนต์. ตัวอย่างของสารประกอบเหล่านี้ ได้แก่ เพชร (C), กราไฟท์ (C), ซิลิกอนไดออกไซด์ (SiO2) และซิลิคอนคาร์ไบด์ (SiC)
ทีนี้มาดูคุณสมบัติหลักของมัน:
- สภาพร่างกายที่อุณหภูมิห้อง: ภายใต้สภาวะแวดล้อม จะพบสารประกอบโมเลกุลและโควาเลนต์ ในสถานะทางกายภาพทั้งสาม (ของแข็ง ของเหลว และก๊าซ)
ตัวอย่าง:
โอ ของแข็ง: น้ำตาล (ซูโครส), ซิลิกา (ทราย), เพชร, กราไฟท์;
โอ ของเหลว: น้ำ, อะซิโตน, เอทานอล;
โอ ก๊าซ: ไฮโดรเจนซัลไฟด์ ก๊าซคลอรีน ก๊าซโบรมีน ก๊าซไฮโดรเจน

- จุดหลอมเหลวและจุดเดือด: โดยทั่วไปแล้ว จุดหลอมเหลวและจุดเดือดของสารเหล่านี้คือ เล็กกว่าสารไอออนิก.
สารโควาเลนต์มีอุณหภูมิเดือดที่สูงกว่าโมเลกุล ซึ่งมักจะสูงกว่า 1,000 องศาเซลเซียสเสมอ เนื่องจากเมื่อโมเลกุลของมันถูกเชื่อมติดกันมากขึ้น จนเกิดเป็นผลึกขัดแตะ จึงจำเป็นต้องให้พลังงานมากขึ้นเพื่อทำให้มันเปลี่ยนสถานะ
ปัจจัยสองประการรบกวนจุดเดือดและจุดหลอมเหลวของสารประกอบโควาเลนต์และโมเลกุล: a มวลกราม และ แรงระหว่างโมเลกุล.
ยิ่งมวลโมลาร์มากเท่าใด ความเฉื่อยของโมเลกุลก็จะยิ่งมากขึ้น ด้วยเหตุนี้ จุดเดือดและจุดหลอมเหลวยิ่งสูงขึ้น ถ้ามวลโมลาร์มีค่าประมาณ เราจะดูที่แรงระหว่างโมเลกุล แรงระหว่างโมเลกุลที่รุนแรงที่สุดคือพันธะไฮโดรเจน ซึ่งนำไปสู่จุดเดือดและจุดหลอมเหลวที่สูงขึ้น ตัวกลางคือไดโพลถาวรและไดโพลที่อ่อนที่สุดซึ่งนำไปสู่จุดเดือดและจุดหลอมเหลวที่ต่ำกว่าคือไดโพลเหนี่ยวนำ
- กระแสไฟฟ้า: ในรูปแบบบริสุทธิ์ ทั้งของเหลวและของแข็งไม่นำกระแสไฟฟ้า
ข้อยกเว้นคือกราไฟต์ซึ่งนำกระแสไฟฟ้าในรูปของแข็งเนื่องจากอิเล็กตรอนพันธะคู่จะสะท้อนและมีความคล่องตัวบางอย่าง
- ความสามารถในการละลาย: ขั้วละลายเป็นขั้วและไม่มีขั้วละลายเป็นไม่มีขั้ว
- ความดื้อรั้น: ความต้านทานของสารโควาเลนต์ต่อการกระแทกหรือการกระแทกทางกลอยู่ในระดับต่ำ โดยทั่วไปแล้วจะเป็นของแข็งที่เปราะดังที่แสดงในกรณีของแก้วซึ่งเกิดจากโซเดียมและแคลเซียมซิลิเกต

- ความเหนียว: โดยทั่วไปแล้วจะมีความแข็งสูง ยกเว้นกราไฟต์ เนื่องจากอะตอมของคาร์บอนเชื่อมโยงกับอะตอมของคาร์บอนอื่นๆ อีกสามอะตอม ทำให้เกิดเพลตหกเหลี่ยมที่มีความคล่องตัวบางอย่าง ทำให้มันนิ่ม ด้วยเหตุนี้จึงใช้เป็นสารหล่อลื่น
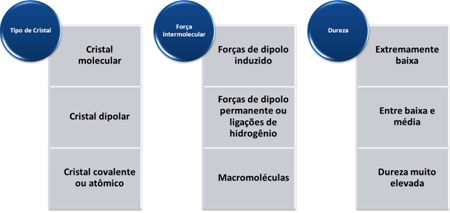
ความแข็งของสารเหล่านี้จะแตกต่างกันไปตามประเภทของคริสตัล ดังแสดงในตารางด้านล่าง:
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm


