ถึง ครอบครัวตารางธาตุ เป็นลำดับแนวตั้งของตารางและการรวบรวม องค์ประกอบทางเคมี ด้วยคุณสมบัติทางเคมีที่คล้ายคลึงกัน ความคล้ายคลึงกันดังกล่าวเกิดจากการมีอยู่ของเวเลนซ์อิเล็กตรอนในปริมาณที่เท่ากันสำหรับธาตุที่อยู่ในตระกูลเดียวกัน ครอบครัวรองรับองค์ประกอบตัวแทนในกลุ่ม 1 และ 2 ตั้งแต่ 13 ถึง 18 และองค์ประกอบเปลี่ยนผ่านในกลุ่ม 1 ถึง 12
อ่านด้วย:ธาตุทรานส์ยูเรนิก — องค์ประกอบทางเคมีที่มนุษย์สร้างขึ้นซึ่งเกิดขึ้นหลังจากยูเรเนียมในตารางธาตุ
หัวข้อของบทความนี้
- 1 - บทสรุปของครอบครัวตารางธาตุ
- 2 - องค์กรของครอบครัวตารางธาตุ
-
3 - ระบบการตั้งชื่อของตระกูลตารางธาตุ
- → องค์ประกอบที่เป็นตัวแทนของตารางธาตุ
- → องค์ประกอบการเปลี่ยนแปลงตารางธาตุ
- 4 - องค์ประกอบทางเคมีของตระกูลตารางธาตุ
-
5 - ลักษณะสำคัญของตระกูลตารางธาตุ
- → กลุ่มที่ 1 หรือตระกูลของโลหะอัลคาไล
- → กลุ่มที่ 2 หรือตระกูลของโลหะอัลคาไลน์เอิร์ธ
- → หมู่ 3 ถึง 12 หรือตระกูลของโลหะทรานซิชัน
- → หมู่ 13 หรือตระกูลโบรอน
- → กลุ่ม 14 หรือตระกูลคาร์บอน
- → หมู่ 15 หรือตระกูลไนโตรเจน
- → กลุ่ม 16 หรือกลุ่มออกซิเจน (chalcogens)
- → กลุ่ม 17 หรือตระกูลฮาโลเจน
- → กลุ่ม 18 หรือตระกูลก๊าซมีตระกูล
-
6 - ตารางธาตุและการจัดจำหน่ายทางอิเล็กทรอนิกส์
- → การกระจายอิเล็กทรอนิกส์ขององค์ประกอบตัวแทน
- → การกระจายอิเล็กทรอนิกส์ขององค์ประกอบการเปลี่ยนแปลง
- 7 - แบบฝึกหัดแก้ไขเกี่ยวกับตระกูลของตารางธาตุ
สรุปครอบครัวตารางธาตุ
ครอบครัวสอดคล้องกับเส้นแนวตั้งของ ตารางธาตุ.
เรียกอีกอย่างว่ากลุ่ม ครอบครัวในตารางธาตุมีหมายเลขตั้งแต่ 1 ถึง 18
องค์ประกอบทางเคมีในตระกูลเดียวกันมีคุณสมบัติทางเคมีที่คล้ายคลึงกัน
ความคุ้นเคยของชุดองค์ประกอบอธิบายได้จากการมีจำนวนเวเลนซ์อิเล็กตรอนเท่ากัน
องค์ประกอบตัวแทนแบ่งออกเป็นกลุ่ม 1, 2, 13, 14, 15, 16, 17 และ 18 แต่ละตระกูลมีชื่อเฉพาะ
องค์ประกอบการเปลี่ยนแปลงสร้างครอบครัวเดี่ยวที่แบ่งออกเป็นกลุ่ม 3, 4, 5, 6, 7, 8, 9, 10, 11 และ 12
อย่าหยุดตอนนี้... มีเพิ่มเติมหลังจากการประชาสัมพันธ์ ;)
องค์กรของครอบครัวตารางธาตุ
ครอบครัวในตารางธาตุ เป็นลำดับแนวตั้งของตารางนั่นคือคอลัมน์ เรียกอีกอย่างว่ากลุ่ม ตระกูลของตารางธาตุ มีหมายเลขตั้งแต่ 1 ถึง 18 จากซ้ายไปขวา
องค์ประกอบทางเคมีที่อยู่ในคอลัมน์เดียวกันจะถือว่าอยู่ในตระกูลเดียวกันเนื่องจากความคล้ายคลึงกันระหว่างคุณสมบัติทางเคมีซึ่งเกิดจากการที่พวกมันมีจำนวนเท่ากัน อิเล็กตรอน ที่ วาเลนซ์เชลล์. ตัวอย่างเช่น องค์ประกอบทางเคมีทั้งหมดของตระกูล 18 มีอิเล็กตรอน 8 ตัวในเวเลนซ์เชลล์ (ฟูลเชลล์) และไม่ค่อยมีส่วนร่วมใน พันธะเคมี.
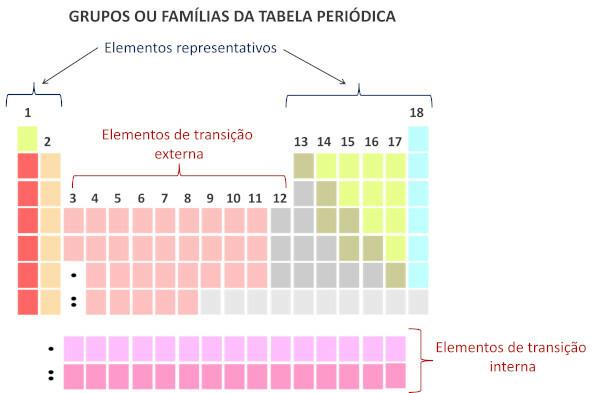
ตามระบบที่ทันสมัยของ สหภาพเคมีบริสุทธิ์และเคมีประยุกต์ระหว่างประเทศ (Iupac) แต่ละกลุ่มหรือตระกูลจะถูกระบุด้วยตัวเลขตั้งแต่ 1 ถึง 18 โดยเริ่มจากซ้ายไปขวาในตารางธาตุ
สิ่งสำคัญคือต้องเน้นว่าระบบ IUPAC แบบเก่าได้นำระบบตัวอักษรและตัวเลขมาใช้ โดยตัวอักษร A และ B เพื่ออ้างถึงตัวแทนและองค์ประกอบการเปลี่ยนผ่านตามลำดับ ปัจจุบันไม่ได้ใช้การตั้งชื่อประเภทนี้อีกต่อไป
ศัพท์เฉพาะของตระกูลตารางธาตุ
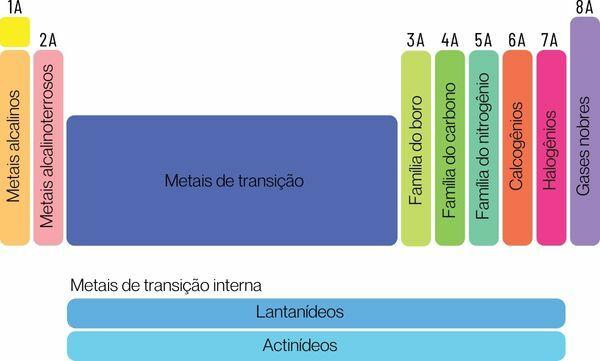
ธาตุเคมีสามารถจำแนกได้เป็นสองตระกูลใหญ่ๆ คือ ธาตุตัวแทนและธาตุแทรนซิชัน
→ องค์ประกอบที่เป็นตัวแทนของตารางธาตุ
องค์ประกอบตัวแทนแบ่งออกเป็นกลุ่ม 1, 2, 13, 14, 15, 16, 17 และ 18 แต่ละกลุ่มมีชื่อเฉพาะซึ่งสามารถทราบได้ ดู:
กลุ่มที่ 1: ครอบครัวของ โลหะ อัลคาไลน์
กลุ่มที่ 2: ครอบครัวของ โลหะอัลคาไลน์เอิร์ ธ.
กลุ่ม 13: โบรอนหรือโลหะตระกูลเอิร์ธ
กลุ่ม 14: ครอบครัวคาร์บอน
กลุ่มที่ 15: ไนโตรเจนหรือตระกูล Pnicogens
กลุ่ม 16: ตระกูลออกซิเจนหรือชาลโคเจน
กลุ่ม 17: ครอบครัวของ ฮาโลเจน.
กลุ่ม 18: ครอบครัวของ ก๊าซมีตระกูล.
→ องค์ประกอบการเปลี่ยนแปลงตารางธาตุ
คุณ องค์ประกอบการเปลี่ยนแปลงสร้างครอบครัวเดี่ยว แบ่งเป็นหมู่ 3, 4, 5, 6, 7, 8, 9, 10, 11 และ 12. อนุกรมแลนทาไนด์และแอกทิไนด์ก็เป็นส่วนหนึ่งของธาตุแทรนซิชันเช่นกัน
องค์ประกอบการเปลี่ยนแปลง เป็นโลหะทั้งหมดและมีคุณสมบัติทางเคมีที่คล้ายคลึงกันแม้จะมีอิเล็กตรอนต่างกันในเวเลนต์เชลล์ และดังนั้น ก็จะก่อตัวเป็นโลหะทรานซิชันเดี่ยวและตระกูลใหญ่
องค์ประกอบทางเคมีจากตระกูลของตารางธาตุ
แต่ละตระกูลหรือกลุ่มประกอบด้วยองค์ประกอบทางเคมีชุดหนึ่ง ดูคำอธิบายขององค์ประกอบทางเคมีที่ประกอบกันเป็นแต่ละตระกูล:
กลุ่มที่ 1:ลิเธียม, โซเดียม, โพแทสเซียม, รูบิเดียม, ซีเซียม, แฟรนเซียม.
กลุ่มที่ 2:เบริลเลียม, แมกนีเซียม, แคลเซียม, สตรอนเทียม, แบเรียม, วิทยุ.
กลุ่มที่ 3:สแกนเดียม, อิตเทรียมอนุกรมแลนทาไนด์และอนุกรมแอกทิไนด์
กลุ่มที่ 4: ไทเทเนียม, เซอร์โคเนียอ, ฮาฟเนี่ยม มันคือ รัทเทอร์ฟอร์เดียม.
กลุ่มที่ 5:วานาเดียม, ไนโอเบียม, แทนทาลัม มันคือ ดับเนียม.
กลุ่มที่ 6:โครเมียม, โมลิบดีนัม, ทังสเตน มันคือ ซีบอร์เจียม.
กลุ่มที่ 7:แมงกานีส, เทคนีเชียม, รีเนียม มันคือ โบริโอ.
กลุ่มที่ 8: เหล็ก, รูทีเนียม, ออสเมียม มันคือ แฮสเซียม.
กลุ่มที่ 9:โคบอลต์โรเดียม อิริเดียม และไมต์เนเรียม
กลุ่มที่ 10:นิกเกิล, แพลเลเดียม, แพลทินัม และดาร์มสตัดติโอ
กลุ่ม 11: ทองแดง, เงิน, ทอง และเรินต์เกเนียม
กลุ่ม 12:สังกะสี, แคดเมียม, ปรอท และโคเปอร์นิคัส
กลุ่ม 13: โบรอน, อลูมิเนียม, แกลเลียมอินเดียมและแทลเลียม
กลุ่ม 14: คาร์บอน, ซิลิคอน,เจอร์เมเนียม, ดีบุก, ตะกั่ว และฟลีโรเวียม
กลุ่มที่ 15:ไนโตรเจน, สารเรืองแสง, สารหนู, พลวง มันคือ บิสมัท.
กลุ่ม 16:ออกซิเจน, กำมะถัน, ซีลีเนียม, เทลลูเรียมพอโลเนียมและลิเวอร์มอเรียม
กลุ่ม 17: ฟลูออรีน, คลอรีน,โบรมีน, ไอโอดีน และแอสทาทีน
กลุ่ม 18:ฮีเลียม, นีออน, อาร์กอน, คริปทอน, ซีนอน มันคือ เรดอน.
สำคัญ: องค์ประกอบทางเคมี ไฮโดรเจน เป็นกรณีพิเศษ เนื่องจากแม้ว่าจะตั้งอยู่ถัดจากกลุ่มที่ 1 แต่ก็ไม่ได้เป็นส่วนหนึ่งของตระกูลโลหะอัลคาไล เนื่องจากไม่มีคุณสมบัติทางเคมีที่คล้ายคลึงกัน
รู้เพิ่มเติม: ธาตุกัมมันตภาพรังสีในตารางธาตุคืออะไร?
ลักษณะสำคัญของตระกูลตารางธาตุ
เป็นของแข็งโลหะ แวววาว และเรียบเนียน
มีค่าการนำความร้อนสูงและสูง การนำไฟฟ้า.
มี อุณหภูมิ การละลายค่อนข้างต่ำ
พวกเขามีปฏิกิริยาสูงกับ น้ำ.
มีแนวโน้มที่จะสร้างไอออนบวกแบบโมโนวาเลนต์ (ชาร์จ +1)
เป็นของแข็งที่เป็นโลหะ แวววาวและแข็งกว่าโลหะอัลคาไล
พวกเขาออกซิไดซ์ได้ง่าย
มีค่าการนำความร้อนสูงและค่าการนำไฟฟ้าสูง
มีอุณหภูมิหลอมเหลวสูงกว่าเล็กน้อยเมื่อเทียบกับโลหะอัลคาไล
พวกมันมีปฏิกิริยากับน้ำ
แนวโน้มที่จะก่อตัวเป็นไอออนบวกคู่ (ประจุ +2)
พวกเขาเป็นครอบครัวที่ใหญ่ที่สุดในตารางธาตุ
ของแข็งโลหะที่แข็งและแวววาว
มีค่าการนำความร้อนสูงและค่าการนำไฟฟ้าสูง
หนาแน่น.
อุณหภูมิหลอมเหลวสูง
อาจนำเสนอแตกต่างกัน สถานะออกซิเดชัน.
→ หมู่ 13 หรือตระกูลโบรอน
พวกเขามีคุณสมบัติระดับกลางระหว่างคุณสมบัติของโลหะและ ไม่ใช่โลหะ.
พวกมันแข็งภายใต้สภาวะแวดล้อม
แนวโน้มที่จะก่อตัวเป็นไอออนบวกแบบไตรวาเลนต์ (ประจุไฟฟ้า +3)
→ กลุ่ม 14 หรือตระกูลคาร์บอน
มีคุณสมบัติเป็นกลางระหว่างคุณสมบัติของโลหะและอโลหะ
พวกมันแข็งภายใต้สภาวะแวดล้อม
มีแนวโน้มที่จะสร้างพันธะทั้งสี่
พวกมันแข็งภายใต้สภาวะแวดล้อม
คาร์บอนและซิลิกอนสามารถสร้างพันธะลูกโซ่ได้
→ หมู่ 15 หรือตระกูลไนโตรเจน
มีคุณสมบัติเป็นกลางระหว่างคุณสมบัติของโลหะและอโลหะ
ของแข็งภายใต้สภาวะแวดล้อม ยกเว้นไนโตรเจนซึ่งเป็นก๊าซ
ไนโตรเจนและฟอสฟอรัสเป็นองค์ประกอบพื้นฐานในสิ่งมีชีวิต
สารหนูเป็นพิษอย่างมาก
→ กลุ่ม 16 หรือกลุ่มออกซิเจน (chalcogens)
พวกมันมีคุณสมบัติที่แตกต่างกัน โดยเปลี่ยนจากอโลหะเป็นธาตุโลหะเมื่อคุณลงไปตามตระกูล
ของแข็งภายใต้สภาวะแวดล้อม ยกเว้นออกซิเจนซึ่งเป็นก๊าซ
มีแนวโน้มที่จะก่อตัวเป็นประจุลบสองขั้ว (ประจุ -2)
→ กลุ่ม 17 หรือตระกูลฮาโลเจน
พวกเขาไม่ใช่โลหะ
ค่อนข้างมีปฏิกิริยา
ตัวนำความร้อนและไฟฟ้าไม่ดี
ภายใต้สภาพแวดล้อม ฟลูออรีนและคลอรีนมีอยู่เป็น ก๊าซโบรมีนเป็นของเหลวและไอโอดีนเป็นของแข็ง
มีแนวโน้มที่จะก่อตัวเป็นประจุลบชนิดโมโนวาเลนต์ (ประจุ -1)
→ กลุ่ม 18 หรือตระกูลก๊าซมีตระกูล
พวกเขาไม่ใช่โลหะ
มีปฏิกิริยาน้อยมาก จึงเรียกว่าก๊าซเฉื่อย
มีอยู่ในรูปของก๊าซ
พวกเขาไม่มีแนวโน้มที่จะก่อตัว ไอออน.
ตารางธาตุและการจัดจำหน่ายทางอิเล็กทรอนิกส์
องค์ประกอบทางเคมีที่อยู่ในตระกูลหรือกลุ่มเดียวกันมีคุณสมบัติทางเคมีที่คล้ายคลึงกันเพราะมี จำนวนอิเล็กตรอนในเวเลนต์เชลล์เท่ากัน
จำนวนอิเล็กตรอนในเวเลนซ์เชลล์มีความเกี่ยวข้องเนื่องจากเป็นตัวกำหนดแนวโน้มการก่อตัวของไอออนบวกหรือ ประจุลบ ประเภทของพันธะเคมีที่จะเกิดขึ้น พลังงานที่เกี่ยวข้องกับปฏิกิริยาเคมี และอื่นๆ ลักษณะเฉพาะ. ในการหาจำนวนเวเลนซ์อิเล็กตรอน มีความจำเป็นต้องรู้ เลขอะตอม ขององค์ประกอบและดำเนินการของคุณ การกระจายทางอิเล็กทรอนิกส์.
→ การกระจายอิเล็กทรอนิกส์ขององค์ประกอบตัวแทน
องค์ประกอบที่เป็นตัวแทน มีอิเล็กตรอนที่มีพลังมากที่สุดในชั้นย่อย ส มันคือ พี ของชั้นอิเล็กทรอนิกส์ (n) ตารางต่อไปนี้แสดงการกำหนดค่าอิเล็กทรอนิกส์ที่เกี่ยวข้องกับองค์ประกอบตัวแทนแต่ละตระกูล ระยะเวลา น แปรผันตั้งแต่ 1 ถึง 7 และแสดงถึงระดับพลังงานที่ครอบครองโดยเวเลนซ์อิเล็กตรอน เทียบเท่ากับคาบ (เส้นแนวนอน) ของตารางธาตุที่พบธาตุนั้น
การกระจายองค์ประกอบตัวแทนทางอิเล็กทรอนิกส์ | ||
ครอบครัวหรือหมู่คณะ |
จำหน่ายอิเล็คทรอนิกส์ |
ตัวอย่าง |
1 |
เรา1 |
Li (Z=3): 1 วินาที2 2 วินาที1 |
2 |
เรา2 |
เป็น (Z=4): 1 วินาที2 2 วินาที2 |
13 |
เรา2 น1 |
B (Z=5): 1 วินาที2 2 วินาที22 น1 |
14 |
เรา2 น2 |
C (Z=6): 1 วินาที2 2 วินาที22 น2 |
15 |
เรา2 น3 |
N (Z=7): 1 วินาที2 2 วินาที22 น3 |
16 |
เรา2 น4 |
O (Z=8): 1 วินาที2 2 วินาที22 น4 |
17 |
เรา2 น5 |
F (Z=9): 1 วินาที2 2 วินาที22 น5 |
18 |
เรา2 น6 |
เน่ (Z=10): 1 วินาที2 2 วินาที22 น6 |
→ การกระจายอิเล็กทรอนิกส์ขององค์ประกอบการเปลี่ยนแปลง
องค์ประกอบการเปลี่ยนแปลงจะกระจายระหว่างกลุ่ม 3 และ 12 และ มีระดับย่อย ง มันคือ ฉ ครอบครองโดยเวเลนซ์อิเล็กตรอน:
องค์ประกอบการเปลี่ยนแปลงภายนอก: เก็บเวเลนซ์อิเล็กตรอนไว้ในระดับย่อย งทำให้การกำหนดค่าอิเล็กตรอนเท่ากับ เรา2 (น-1)ง(1 ถึง 8). ตัวอย่างเช่น ธาตุนิเกิล (Z = 28) อยู่ในกลุ่ม 10 และการกำหนดค่าของมันคือ 1 วินาที2 2 วินาที2 2 น6 3 วินาที2 3 น6 4 วินาที2 3 มิติ8.
องค์ประกอบการเปลี่ยนแปลงภายใน: พวกมันเป็นส่วนหนึ่งของหมู่ 3 แต่เป็น "ภายใน" ของตารางธาตุ ซึ่งถูกขยายลงมาด้านล่าง ในคาบ 6 (แลนทาไนด์) และ 7 (แอกทิไนด์) องค์ประกอบเหล่านี้มีเวเลนซ์อิเล็กตรอนอยู่ในเปลือกย่อย ฉ และการกำหนดค่าอิเล็กทรอนิกส์ทั่วไปของ เรา2 (น-2)ฉ(1 ถึง 13). ตัวอย่างเช่น ธาตุแลนทานัม (Z = 57) เป็นธาตุแรกในอนุกรมแลนทาไนด์ และโครงแบบอิเล็กตรอนของมันคือ 1 วินาที2 2 วินาที2 2 น6 3 วินาที2 3 น6 4 วินาที2 3 มิติ10 4 น6 5 วินาที2 4 วัน10 5 น6 6 วินาที2 4ฉ1.
รู้ยัง:ที่มาของตารางธาตุคืออะไร?
แบบฝึกหัดเกี่ยวกับครอบครัวของตารางธาตุ
คำถามที่ 1
(UFC — ดัดแปลง) เกี่ยวกับการจำแนกธาตุสมัยใหม่ ให้ทำเครื่องหมายที่ข้อความจริง:
A) ในตารางธาตุ ครอบครัวหรือกลุ่มจะสอดคล้องกับเส้นแนวนอน
B) ธาตุในตระกูลมีคุณสมบัติทางเคมีที่แตกต่างกันมาก
C) ในครอบครัว ธาตุโดยทั่วไปมีจำนวนอิเล็กตรอนเท่ากันในชั้นสุดท้าย
D) ในช่วงหนึ่งองค์ประกอบมีคุณสมบัติทางเคมีที่คล้ายคลึงกัน
จ) องค์ประกอบที่เป็นตัวแทนจะกระจายอยู่ในกลุ่ม 3 ถึง 12
ปณิธาน:
อัลเทอร์เนทีฟซี
รายการ A ไม่ถูกต้อง: ตระกูลหรือกลุ่มคือคอลัมน์ (เส้นแนวตั้ง) ของตารางธาตุ
รายการ B และ D ไม่ถูกต้อง: ในตระกูลหนึ่ง ธาตุมีคุณสมบัติทางเคมีที่คล้ายคลึงกัน ในคาบต่างๆ ธาตุต่างๆ จะมีเปลือกอิเล็กตรอนแบบเดียวกันซึ่งครอบครองโดยเวเลนต์อิเล็กตรอน
ข้อ C ถูกต้อง: ในครอบครัว ธาตุมีจำนวนอิเล็กตรอนเท่ากันในชั้นสุดท้าย
รายการ E ไม่ถูกต้อง: องค์ประกอบตัวแทนคือกลุ่ม 1, 2, 13, 14, 15, 16, 17 และ 18 องค์ประกอบการเปลี่ยนแปลงจะกระจายในกลุ่ม 3 ถึง 12
คำถามที่ 2
(EAM) ธาตุ A, B และ C มีโครงแบบอิเล็กตรอนต่อไปนี้ในเวเลนต์เชลล์:
ตอบ: 3 วินาที1
B: 4 วินาที2 4 น4
ค: 3 วินาที2
จากข้อมูลนี้ เลือกตัวเลือกที่ถูกต้อง
A) ธาตุ A เป็นโลหะอัลคาไล
B) ธาตุ B เป็นฮาโลเจน
C) ธาตุ C เป็นแชลโคเจน
D) ธาตุ A และ B อยู่ในคาบที่สามของตารางธาตุ
จ) ธาตุทั้งสามอยู่ในกลุ่มเดียวกันของตารางธาตุ
ปณิธาน:
ทางเลือก ก
ข้อ A ถูกต้อง: ธาตุ A มีการแจกแจงแบบอิเล็กทรอนิกส์ที่มีเวเลนซ์อิเล็กตรอนเพียงตัวเดียว ดังนั้นมันจึงอยู่ในกลุ่ม 1 ของตารางธาตุ
รายการ B ไม่ถูกต้อง: ธาตุ B มีโครงแบบอิเล็กตรอน 4s2 4 น4แสดงว่ามีอิเล็กตรอน 6 ตัวในชั้นสุดท้ายและองค์ประกอบนี้อยู่ในกลุ่ม 16 (แชลโคเจน)
รายการ C ไม่ถูกต้อง: องค์ประกอบ C มีการกำหนดค่าทางอิเล็กทรอนิกส์โดยมีอิเล็กตรอน 2 ตัวในชั้นสุดท้าย ดังนั้นจึงเป็นองค์ประกอบของกลุ่ม 2 ในตาราง
รายการ D ไม่ถูกต้อง: องค์ประกอบ A อยู่ในช่วงเวลาที่สาม (n = 3) และองค์ประกอบ B อยู่ในช่วงเวลาที่สี่ (n = 4)
ข้อ E ไม่ถูกต้อง: ธาตุทั้งสามมีปริมาณอิเล็กตรอนต่างกันในชั้นสุดท้าย ดังนั้นพวกมันจึงไม่สามารถอยู่ในตระกูลเดียวกันได้
โดย Ana Luiza Lorenzen Lima
ครูสอนเคมี
คลิกที่นี่ เรียนรู้ว่าเลเยอร์วาเลนซ์คืออะไร และค้นหาว่าสามารถระบุได้อย่างไร
ทำความเข้าใจวิธีการแจกจ่ายทางอิเล็กทรอนิกส์และดูตัวอย่าง
เรียนรู้เกี่ยวกับลักษณะพิเศษของธาตุทรานซิชันภายใน (แอกทิไนด์และแลนทาไนด์) ซึ่งอยู่ในคาบที่หกและเจ็ดของกลุ่มที่ 3 ของตารางธาตุ
รู้จักองค์ประกอบทางเคมีที่มีอยู่ ทำความเข้าใจว่าองค์ประกอบเหล่านี้คืออะไรและจะเป็นตัวแทนขององค์ประกอบเหล่านี้ได้อย่างไร
ก๊าซมีตระกูลเป็นองค์ประกอบเดียวที่พบในธรรมชาติ เรียนรู้เพิ่มเติมเกี่ยวกับพวกเขาที่นี่ในบทความนี้!
เรียนรู้เกี่ยวกับฮาโลเจน คุณสมบัติ คุณลักษณะ และการใช้งานหลักในชีวิตประจำวัน
เรียนรู้เพิ่มเติมเกี่ยวกับโลหะอัลคาไลน์เอิร์ธ รู้จักคุณลักษณะ คุณสมบัติ และการใช้งาน
ทำความเข้าใจว่าเลขอะตอมคืออะไรและเรียนรู้ลักษณะของอะตอมที่สามารถกำหนดได้จากเลขอะตอม
ตรวจสอบที่นี่ว่าตารางธาตุคืออะไร และดูแบบจำลองเชิงโต้ตอบเพื่อให้คุณรู้จักองค์ประกอบทางเคมีทั้งหมดที่ประกอบขึ้นเป็นตารางธาตุ