อู๋ แอกทิเนียม, สัญลักษณ์ Ac และเลขอะตอม 89 เป็นองค์ประกอบที่อยู่ในบล็อก f ของ ตารางธาตุ, ที่เรียกว่าองค์ประกอบการเปลี่ยนแปลงภายใน. มีลักษณะทางเคมีคล้ายกับแลนทานัม (เช่น มีประจุเท่ากับ +3 ในสารประกอบ) แต่หาได้ยากและมีการใช้งานน้อย จากไอโซโทปประมาณ 30 ไอโซโทปของธาตุนี้ มีเพียงสองไอโซโทปที่เกิดขึ้นตามธรรมชาติเท่านั้น คือแอกทิเนียม-227 และแอกทิเนียม-228
แอกทิเนียมได้ดีที่สุดจากการทิ้งระเบิดนิวเคลียสของ วิทยุ (Ra) กับนิวตรอนความร้อนซึ่งเป็นเทคนิคที่ทำให้สามารถบรรลุค่าได้ในช่วงมิลลิกรัม แอปพลิเคชันยังคงถูก จำกัด แต่เป็นที่ทราบกันดีว่า สามารถใช้เป็นแหล่งพลังงานได้ สำหรับยานอวกาศและอุปกรณ์ที่ทำงานในพื้นที่ห่างไกล เช่นเดียวกับแอกทิเนียม-225 ที่เป็นตัวเลือกที่มีศักยภาพสำหรับการรักษามะเร็งบางชนิด
อ่านด้วย:Cesium-137 — ไอโซโทปกัมมันตภาพรังสีที่ทำให้เกิดอุบัติเหตุทางรังสีในGoiânia
หัวข้อในบทความนี้
- 1 - สรุปเกี่ยวกับแอกทิเนียม
- 2 - คุณสมบัติของแอกทิเนียม
- 3 - ลักษณะของแอกทิเนียม
- 4 - แอกทิเนียมสามารถพบได้ที่ไหน?
- 5 - รับแอกทิเนียม
- 6 - การประยุกต์ใช้แอกทิเนียม
- 7 - ประวัติของแอกทิเนียม
สรุปเกี่ยวกับแอกทิเนียม
เป็นโลหะที่อยู่ในบล็อก f ของตารางธาตุ
ในรูปแบบโลหะ มีสีขาวเงิน บางครั้งก็มีประกายสีทอง
ในสารละลาย เนื่องจากมีความคล้ายคลึงกับแลนทานัม จึง NOx é +3.
มีไอโซโทปประมาณ 30 ไอโซโทป มีเพียงสองไอโซโทปที่พบในธรรมชาติ: มวล 227 และ 228
มีอยู่ในตัวอย่างของ ยูเรเนียมแต่ได้มาจากการทิ้งระเบิดของไอโซโทปวิทยุด้วยนิวตรอนความร้อน
หาได้ยากและมีแอปพลิเคชันน้อย
อย่างไรก็ตาม บทบาทของไอโซโทปแอกทิเนียม-225 ในการต่อสู้กับมะเร็งบางชนิดมีความโดดเด่น
คุณสมบัติของแอกทิเนียม
เครื่องหมาย: ac
เลขอะตอม: 89
มวลอะตอม: 227 คิว
อิเล็กโตรเนกาติวีตี้: 1,1
จุดหลอมเหลว: 1050 °C
จุดเดือด: 3198 °C
ความหนาแน่น: 10.07 g.cm-3 (คำนวณ)
การกำหนดค่าทางอิเล็กทรอนิกส์: [Rn] 7s2 6 วัน1
ชุดเคมี: actinides, f-block, องค์ประกอบการเปลี่ยนแปลงภายใน
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
ลักษณะแอกทิเนียม
แอกทิเนียม, เลขอะตอม 89 และสัญลักษณ์ Ac, มันคือ โลหะ อยู่ในกลุ่มแอกทิไนด์ ซึ่งอยู่ในบล็อก f ของตารางธาตุ ในรูปแบบโลหะ มีสีขาวเงิน บางครั้งก็มีสีทอง
ในทางเคมี แอกทิเนียม ชวนให้นึกถึงแลนทานัมมากอาจกล่าวได้ว่าในเชิงคุณภาพไม่มีความแตกต่างระหว่างทั้งสอง ดังนั้น ในสารละลายและในการก่อตัวของสารประกอบ แอกทิเนียมจึงมีประจุเป็น +3 (Ac3+). เมื่อสัมผัสกับอากาศ มันจะเกิดปฏิกิริยาออกซิไดซ์อย่างรวดเร็วและก่อตัวเป็นชั้น Ac2อู๋3ซึ่งป้องกันความต่อเนื่องของ ออกซิเดชัน.
สารประกอบแอกทิเนียมที่รู้จักมีเพียงไม่กี่ชนิด ได้แก่ เฮไลด์ ออกซีเฮไลด์ ออกไซด์ และซัลไฟด์ คาดว่าจะมีบางส่วนอื่น ๆ เช่นเดียวกับกรณีของคาร์บอเนต แต่ยังไม่ได้ระบุ
รู้จักไอโซโทปของแอกทิเนียมประมาณ 30 ไอโซโทป, เป็นเพียงสองธรรมชาติ: 227acc 228ปีก่อนคริสตกาล อย่างแรกเป็นที่รู้จักกันเป็นอย่างดีมาจากชุดการสลายตัวของกัมมันตภาพรังสีของ 235คุณและมีเวลาของ ครึ่งชีวิต อายุ 21.77 ปี Actinium-228 ซึ่งมีครึ่งชีวิต 6.15 ชั่วโมง เป็นผลคูณของชุดการสลายตัวของสารกัมมันตรังสีของทอเรียม-232
อ่านด้วย:การสลายตัวของกัมมันตภาพรังสี — ปรากฏการณ์ที่อะตอมเปลี่ยนเป็นนิวเคลียสใหม่
แอกทิเนียมสามารถพบได้ที่ไหน?
Actinium (โดยเฉพาะอย่างยิ่งในรูปแบบ 227ปีก่อนคริสตกาล) ขึ้นอยู่กับปริมาณยูเรเนียม-235. โดยตรงกระจายตัวได้ดีทั่วเปลือกโลก ปริมาณยูเรเนียมเฉลี่ยในเปลือกโลกคือ 2.7 ppm (ส่วนต่อล้านหรือมิลลิกรัมต่อกิโลกรัม) โดย 0.72% ของมวลที่สอดคล้องกับ 235ยู. ทำให้สามารถคำนวณความอุดมสมบูรณ์ตามธรรมชาติของ 227Ac (ขึ้นอยู่กับครึ่งชีวิตของยูเรเนียมและไอโซโทปเอง) ซึ่งจะเท่ากับ 5.7 x 10-10 ppm
รับแอกทิเนียม
แม้ว่าจะมีอยู่ในแร่ยูเรเนียม แต่แอกทิเนียมที่รายงานสูงสุดที่ได้รับจากแหล่งธรรมชาตินี้คือประมาณ 7 ไมโครกรัม (ไมโครกรัม, 10-6 กรัม)
วิธีที่ดีที่สุดที่จะได้รับมันมาในปลายทศวรรษที่ 1940 เมื่อนักวิทยาศาสตร์สามารถได้รับมัน 227บี.ซี ผ่านการฉายรังสีของ 226Ra กับนิวตรอนความร้อน.

ด้วยเทคนิคนี้ ได้ปริมาณ Ac เป็นมิลลิกรัม
แอปพลิเคชั่นแอกทิเนียม
พลังงานจากอนุภาคทั้งห้า อัลฟ่า ที่เกิดขึ้นระหว่างอนุกรมการสลายกัมมันตภาพรังสีของ 227Ac อนุญาตให้ใช้เป็น แหล่งความร้อนในเครื่องกำเนิดความร้อนด้วยความร้อนจากไอโซโทปไอโซโทป. พลังงานจะถูกผลิตขึ้นสำหรับยานอวกาศหรืออุปกรณ์อื่น ๆ ที่ต้องใช้งานเป็นเวลานานในสถานที่ห่างไกล
แล้ว 225Ac ซึ่งมีครึ่งชีวิต 10 วัน เป็นไอโซโทปรังสีอัลฟ่าที่มีคุณสมบัติที่น่าสนใจสำหรับการทำลายเซลล์มะเร็งอย่างรวดเร็ว พลังงานที่สำคัญที่ปล่อยออกมาในการสลายตัวของ 225Ac ซึ่งสร้างอนุภาคอัลฟาสี่อนุภาค สามารถใช้ในการผ่าตัดเพื่อโจมตีเนื้องอกมะเร็งได้ ต่อมลูกหมาก เต้านม และไขกระดูก อีกจุดที่น่าสนใจคือชุดการสลายตัวของแอกทิเนียม-225 สิ้นสุดที่ 209Bi ซึ่งเป็นไอโซโทปที่เสถียรและปลอดสารพิษ
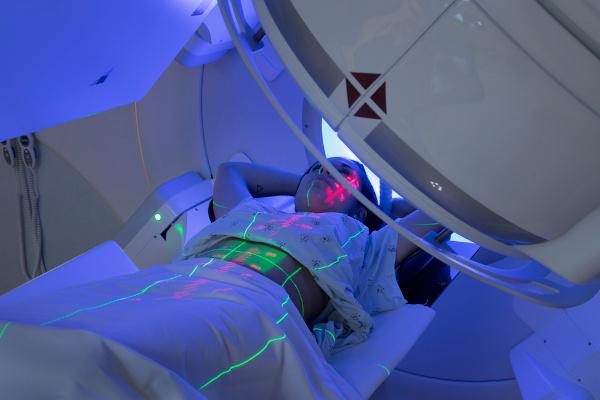
ความท้าทายในการใช้งาน 225Ac อยู่ในการไม่ก่อตัวของผู้อื่น ไอโซโทปรังสีเช่น อันตรายที่อาจเกิดขึ้นได้ 221Fr และในการปล่อยให้แอกตินไอโซโทปทำหน้าที่นานขึ้นบนเป้าหมายของเนื้องอก
ประวัติของแอกทิเนียม
ในปี พ.ศ. 2442 ในห้องทดลองของปิแอร์และ Marie Curie, André-Louis Debierne รายงานว่าเขาได้พบธาตุกัมมันตภาพรังสีใหม่ซึ่งจะเป็นสารเคมีใกล้เคียงกับ ไทเทเนียม. หกเดือนต่อมาในปี 1900 เดเบียนได้กล่าวถึงเศษไททาเนียมไม่เคลื่อนไหวอีกต่อไป และองค์ประกอบใหม่ที่เขากำลังตรวจสอบอยู่ในขณะนี้มีความคล้ายคลึงกับทอเรียมทางเคมี
Debierne อ้างสิทธิ์ในการค้นพบองค์ประกอบใหม่ให้บัพติศมาเป็นแอกทิเนียม (จากภาษากรีก aktisซึ่งหมายถึง “เรย์”) ในขณะนั้นการค้นพบของ Andre-Louis Debierne ไม่ได้ถูกวิพากษ์วิจารณ์ แต่จากสิ่งที่เป็นที่รู้จักในปัจจุบัน เห็นได้ชัดว่าการทดลองในปี 1899 ไม่ใช่ ไม่ได้ผลิตแอกทิเนียม ในขณะที่การทดลองในช่วงทศวรรษ 1900 ก่อให้เกิดส่วนผสมของนิวไคลด์กัมมันตรังสี ซึ่งอาจรวมถึงแอกทิเนียมที่มีขนาดเล็กกว่าด้วย
แม้ว่า, ในปี ค.ศ. 1902 ฟรีดริช ออสการ์ กีเซล ได้รายงานสาร "เล็ดลอดออกมา" ใหม่ (สารกัมมันตภาพรังสี) ท่ามกลางสิ่งเจือปนของ pitchblende (รูปแบบหนึ่งของแร่ pitchblende, ยูเรเนียมออกไซด์) Giesel สามารถสร้างคุณสมบัติทางเคมีหลายอย่างของสารใหม่นี้ได้อย่างถูกต้อง รวมทั้งข้อเท็จจริงที่สำคัญที่ว่ามันมีความคล้ายคลึงทางเคมีกับกลุ่มซีเรียมที่หายาก
ในปี ค.ศ. 1903 นักวิทยาศาสตร์พยายามทำให้ตัวอย่างมีสมาธิจนถึงจุดที่มีเพียงแลนทานัมเป็นสิ่งเจือปน ไม่สามารถตรวจจับทอเรียมได้ ปีถัดมา จีเซลให้บัพติศมาธาตุใหม่ “อีเมเนียม” เนื่องจากเห็นชัดว่าธาตุใหม่ องค์ประกอบวิทยุ.
Debierne โจมตีข้อเรียกร้องของ Giesel อย่างจริงจังโดยยืนยันว่าเป็นสารเดียวกันกับที่เขาค้นพบและตั้งชื่อว่าแอกทิเนียม แม้ว่าตัวเขาเองจะรายงานว่ามีความคล้ายคลึงทางเคมีกับไททาเนียมและทอเรียม
ต่อมา Debierne ได้ชัยชนะ ทำให้นักประวัติศาสตร์หลายคนมองว่าเขาเป็นผู้ค้นพบธาตุ 89 ที่แท้จริง แต่อาจเป็นเพราะอิทธิพลของคู่รัก Curie และความจริงที่ว่า Rutherford ได้ให้เครดิตคุณ อย่างไรก็ตาม คนอื่นๆ ชอบแบ่งเครดิตระหว่างเดเบียนและจีเซล
เธ การค้นพบแอคทิเนียมยังเป็นความต่อเนื่องของงานของ Curiesแต่ก็ไม่เคยได้รับผลกระทบเช่นเดียวกับเรเดียม (Ra) ที่เพิ่งค้นพบใหม่ แอกทิเนียมไม่เหมือนกับเรเดียมในขณะนั้น นอกจากจะหายากมากในธรรมชาติและหาได้ยากแล้ว
โดย Stefano Araújo Novais
ครูสอนเคมี


