อู๋ สมดุลสมการ ช่วยให้เราสามารถจับคู่จำนวนอะตอมที่มีอยู่ในสมการเคมีเพื่อให้เป็นจริงและแสดงถึงปฏิกิริยาเคมี
ใช้คำถามด้านล่างเพื่อทดสอบความรู้ของคุณและตรวจสอบคำตอบที่แสดงความคิดเห็นหลังความคิดเห็นเพื่อตอบคำถามของคุณ
คำถามที่ 1
(แมคเคนซี่-เอสพี)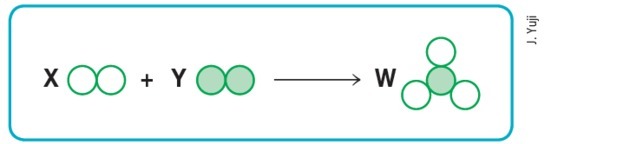
สมมติว่าวงกลมว่างและวงกลมเต็มตามลำดับหมายถึงอะตอมที่แตกต่างกัน ดังนั้นแผนภาพ ด้านบนจะแสดงปฏิกิริยาเคมีที่สมดุลหากเราแทนที่ตัวอักษร X, Y และ W ตามลำดับด้วย ค่า:
ก) 1, 2 และ 3
ข) 1, 2 และ 2
ค) 2, 1 และ 3
ง) 3, 1 และ 2
จ) 3, 2 และ 2
ทางเลือก ง) 3, 1 และ 2
ขั้นตอนที่ 1: เรากำหนดตัวอักษรเพื่อให้สมการเข้าใจง่ายขึ้น
ขั้นตอนที่ 2: เรารวมดัชนีเพื่อหาว่าใครมีอะตอมมากที่สุดในสมการ
| THE | |
| บี |
A และ B ปรากฏเพียงครั้งเดียวในแต่ละสมาชิกของสมการ อย่างไรก็ตาม หากเราเพิ่มดัชนี เราจะเห็นว่า A มีค่าสูงสุด ดังนั้นเราจึงเริ่มสร้างสมดุลให้กับเขา
ขั้นตอนที่ 3: เราสร้างสมดุลให้กับองค์ประกอบ A โดยการแปลงดัชนีและเปลี่ยนเป็นค่าสัมประสิทธิ์
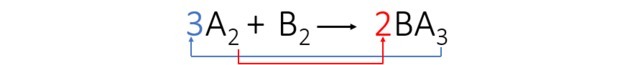
เราสังเกตว่าองค์ประกอบ B มีความสมดุลโดยอัตโนมัติและสัมประสิทธิ์ของสมการคือ 3, 1 และ 2
คำถาม2
(Unicamp-SP) อ่านประโยคต่อไปนี้แล้วแปลงเป็นสมการเคมี (สมดุล) โดยใช้สัญลักษณ์และสูตร “โมเลกุลของก๊าซไนโตรเจนซึ่งมีอะตอมสองอะตอมของ ไนโตรเจนต่อโมเลกุล ทำปฏิกิริยากับไดอะตอมมิกสามโมเลกุล ก๊าซไฮโดรเจน ทำให้เกิดก๊าซแอมโมเนียสองโมเลกุล ซึ่งประกอบด้วยไฮโดรเจนสามอะตอมและหนึ่งในนั้น ไนโตรเจน".
ตอบ:
เป็นตัวแทนของอะตอมที่อธิบายไว้ในคำถามเราสามารถเข้าใจได้ว่าปฏิกิริยาเกิดขึ้นดังนี้:
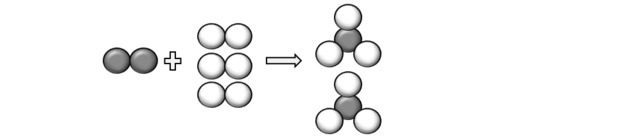
ดังนั้นเราจึงมาถึงสมการ:
คำถาม 3
ไฮโดรเจนเปอร์ออกไซด์เป็นสารประกอบทางเคมีที่สามารถย่อยสลายได้เป็นน้ำและออกซิเจนตามสมการทางเคมีด้านล่าง
เกี่ยวกับปฏิกิริยานี้ สมการสมดุลที่ถูกต้องคือ:
อา2อู๋2 → ดิ2 + โฮ2อู๋
ข) 2 ชั่วโมง2อู๋2 → ดิ2 + 2H2อู๋
ค) H2อู๋2 → 2O2 + โฮ2อู๋
ง) 2 ชั่วโมง2อู๋2 → 2O2 + 2H2อู๋
ทางเลือกที่ถูกต้อง: b) 2H2อู๋2 → ดิ2 + 2H2อู๋
โปรดทราบว่าไฮโดรเจนเปอร์ออกไซด์เป็นสารเคมีที่ประกอบด้วยอะตอมขององค์ประกอบทางเคมีสองชนิด ได้แก่ ไฮโดรเจนและออกซิเจน
หลังจากปฏิกิริยาการสลายตัว คุณต้องมีจำนวนอะตอมของธาตุทั้งสองเท่ากันทั้งในสารตั้งต้นและผลิตภัณฑ์ สำหรับสิ่งนี้ เราต้องทำให้สมการสมดุลกัน
โปรดทราบว่าเรามีไฮโดรเจน 2 อะตอมในตัวทำปฏิกิริยา (H2อู๋2) และสองอะตอมในผลิตภัณฑ์ (H2อ.) อย่างไรก็ตาม ออกซิเจนมีสองอะตอมในตัวทำปฏิกิริยา (H2อู๋2) และสามอะตอมในผลิตภัณฑ์ (H2O และ O2).
ถ้าเราใส่สัมประสิทธิ์ 2 ก่อนไฮโดรเจนเปอร์ออกไซด์ เราจะเพิ่มจำนวนอะตอมของธาตุเป็นสองเท่า
สังเกตว่าถ้าเราใส่ค่าสัมประสิทธิ์เดียวกันกับสูตรน้ำ เราก็จะมีปริมาณอะตอมเท่ากันทั้งสองข้าง
ดังนั้นสมการเคมีที่สมดุลอย่างถูกต้องคือ 2H2อู๋2 → ดิ2 + 2H2โอ.
คำถาม 4
(UFPE) พิจารณาปฏิกิริยาเคมีด้านล่าง
เราสามารถพูดได้ว่า:
ก) ทั้งหมดมีความสมดุล
b) 2, 3 และ 4 มีความสมดุล
c) มีเพียง 2 และ 4 เท่านั้นที่สมดุล
d) มีเพียง 1 เท่านั้นที่ไม่สมดุล
จ) ไม่มีสิ่งใดสมดุลอย่างถูกต้อง เนื่องจากสถานะทางกายภาพของสารตั้งต้นและผลิตภัณฑ์ต่างกัน
ทางเลือก b) 2, 3 และ 4 มีความสมดุล
ทางเลือกที่ 1 และ 5 ไม่ถูกต้องเนื่องจาก:
- สมการที่ 1 ไม่สมดุล ยอดคงเหลือที่ถูกต้องจะเป็น:
- สมการที่ 5 ไม่ถูกต้องเนื่องจากสารประกอบที่เกิดขึ้นในปฏิกิริยาจะเป็น H2เท่านั้น3.
เพื่อสร้าง H2เท่านั้น4 ควรรวมอยู่ในสมการการเกิดออกซิเดชันของSO2.
คำถาม 5
(Mackenzie-SP) เมื่อได้รับความร้อนถึง 800 °C แคลเซียมคาร์บอเนตจะสลายตัวเป็นแคลเซียมออกไซด์ (มะนาวบริสุทธิ์) และคาร์บอนไดออกไซด์ สมการสมดุลที่ถูกต้องซึ่งสอดคล้องกับปรากฏการณ์ที่อธิบายไว้คือ:
(ให้มา: Ca — โลหะอัลคาไลน์เอิร์ธ)
ทางเลือก c)
แคลเซียมเป็นโลหะอัลคาไลน์เอิร์ทและมีความเสถียร แคลเซียมต้องการ 2 อิเล็กตรอน2+) ซึ่งเป็นประจุออกซิเจน (O2-).
ดังนั้นอะตอมของแคลเซียมจะจับกับอะตอมออกซิเจนและสารประกอบที่เกิดขึ้นคือ CaO ซึ่งเป็นปูนขาว
อีกผลิตภัณฑ์หนึ่งคือคาร์บอนไดออกไซด์ (CO2). ทั้งสองเกิดจากแคลเซียมคาร์บอเนต (CaCO3).
นำมาเป็นสมการ:
เราสังเกตว่าปริมาณอะตอมนั้นถูกต้องอยู่แล้วและไม่จำเป็นต้องปรับสมดุล
คำถาม 6
(UFMG) สมการ ไม่สมดุล สมดุลกับจำนวนที่น้อยที่สุดที่เป็นไปได้ ผลรวมของสัมประสิทธิ์ปริมาณสัมพันธ์จะเป็น:
ก) 4
ข) 7
ค) 10
ง) 11
จ) 12
ทางเลือก จ) 12
โดยใช้วิธีการทดลอง ลำดับการปรับสมดุลจะเป็น:
ก้าวแรก: เนื่องจากธาตุที่ปรากฏเพียงครั้งเดียวในแต่ละสมาชิกและมีดัชนีสูงสุดคือแคลเซียม เราจึงเริ่มสร้างสมดุลให้กับธาตุนั้น
ขั้นตอนที่ 2: เราติดตามการทรงตัวโดย PO. ที่ต่างไปจากเดิมอย่างสิ้นเชิง43-ซึ่งยังปรากฏเพียงครั้งเดียว
ขั้นตอนที่ 3: เราปรับสมดุลไฮโดรเจน
ด้วยสิ่งนี้ เราสังเกตว่าปริมาณออกซิเจนถูกปรับโดยอัตโนมัติและสมดุลของสมการคือ:
จำไว้ว่าเมื่อสัมประสิทธิ์เป็น 1 คุณไม่จำเป็นต้องเขียนมันในสมการ
การเพิ่มสัมประสิทธิ์ที่เรามี:
คำถาม 7
การเผาไหม้เป็นปฏิกิริยาเคมีชนิดหนึ่งที่พลังงานถูกปล่อยออกมาในรูปของความร้อน
ในการเผาไหม้ที่สมบูรณ์ของสารที่เกิดจากคาร์บอนและไฮโดรเจน จะเกิดคาร์บอนไดออกไซด์และน้ำ
สังเกตปฏิกิริยาการเผาไหม้ของไฮโดรคาร์บอนและคำตอบว่าสมการใดด้านล่างนี้มีความสมดุลอย่างไม่ถูกต้อง:
ก) CH4 + 2O2 → CO2 + 2H2อู๋
ข) C3โฮ8 +502 → 3CO2 + 4H2อู๋
ค) C4โฮ10 +13/3O2 → 4CO2 + 5 ชม2อู๋
กระแสตรง2โฮ6 + 7/2O2 → 2CO2 + 3H2อู๋
คำตอบที่ไม่ถูกต้อง: c) C4โฮ10 +13/3O2 → 4CO2 + 5 ชม2อู๋
ในการทำให้สมการเคมีสมดุลกัน ก่อนอื่นเรามาดูว่าองค์ประกอบใดปรากฏเพียงครั้งเดียวในแต่ละสมาชิกของสมการ
โปรดทราบว่าคาร์บอนและไฮโดรเจนสร้างสารตั้งต้นเพียงตัวเดียวและหนึ่งผลิตภัณฑ์ในแต่ละสมการที่นำเสนอ
เรามาเริ่มสร้างสมดุลกับไฮโดรเจนกันเถอะ เพราะมันมีจำนวนอะตอมมากกว่า
ดังนั้น ลำดับของการทรงตัวจะเป็น:
- ไฮโดรเจน
- คาร์บอน
- ออกซิเจน
ไฮโดรเจน
เนื่องจากผลิตภัณฑ์มีไฮโดรเจน 2 อะตอม เราจึงใส่ตัวเลขเป็นสัมประสิทธิ์คูณด้วย 2 เพื่อให้ได้จำนวนไฮโดรเจนอะตอมของสารตั้งต้น
ก) CH4 + โอ2 → CO2 + 2โฮ2อู๋
ข) C3โฮ8 + โอ2 → CO2 + 4โฮ2อู๋
ค) C4โฮ10 + โอ2 → CO2 + 5โฮ2อู๋
กระแสตรง2โฮ6 + โอ2 → CO2 + 3โฮ2อู๋
คาร์บอน
การปรับสมดุลทำได้โดยการเปลี่ยนดัชนีคาร์บอนในสารตั้งต้นและใช้เป็นค่าสัมประสิทธิ์ของผลิตภัณฑ์ที่มีอะตอมของธาตุนี้
ก) CH4 + โอ2 → 1CO2 + 2H2อู๋
ข) C3โฮ8 + โอ2 → 3CO2 + 4H2อู๋
ค) C4โฮ10 + โอ2 → 4CO2 + 5 ชม2อู๋
กระแสตรง2โฮ6 + โอ2 → 2CO2 + 3H2อู๋
ออกซิเจน
การเพิ่มจำนวนอะตอมของออกซิเจนในผลิตภัณฑ์ที่เกิดขึ้น เราจะพบจำนวนอะตอมของธาตุที่ต้องทำปฏิกิริยา
เพื่อที่เราต้องใส่ค่าสัมประสิทธิ์ของจำนวนที่คูณด้วย 2 ผลลัพธ์ในจำนวนอะตอมออกซิเจนในผลิตภัณฑ์
ก) CH4 + โอ2 → 1CO2 + 2H2อู๋
2x = 2 + 2
2x = 4
x = 2
ดังนั้นสมการที่ถูกต้องคือ: CH4 + 2อู๋2 → 1CO2 + 2H2โอ.
ข) C3โฮ8 + โอ2 → 3CO2 + 4H2อู๋
2x = 6 + 4
2x = 10
x = 5
ดังนั้นสมการที่ถูกต้องคือ C3โฮ8 + 5อู๋2 → 3CO2 + 4H2อู๋
ค) C4โฮ10 + โอ2 → 4CO2 + 5 ชม2อู๋
2x = 8 + 5
2x = 13
x = 13/2
ดังนั้นสมการที่ถูกต้องคือ C4โฮ10 + 13/2อู๋2 → 4CO2+ 5 ชม2อู๋
กระแสตรง2โฮ6 + โอ2 → 2CO2 + 3H2อู๋
2x = 4 + 3
2x = 7
x = 7/2
ดังนั้นสมการที่ถูกต้องคือ C2โฮ6 + 7/2อู๋2 → 2CO2 + 3H2อู๋
สมการสมดุลที่ถูกต้องคือ:
ก) CH4 + 2O2 → CO2 + 2H2อู๋
ข) C3โฮ8 +502 → 3CO2 + 4H2อู๋
ค) C4โฮ10 + 13/2O2 → 4CO2 + 5 ชม2อู๋
กระแสตรง2โฮ6 + 7/2O2 → 2CO2 + 3H2อู๋
ดังนั้นทางเลือก c) C4โฮ10 +13/3O2 → 4CO2 + 5 ชม2ประเด็นคือ มันไม่มีความสมดุลที่ถูกต้อง
คำถาม 8
(ศัตรู 2015) หินปูนเป็นวัสดุที่ประกอบด้วยแคลเซียมคาร์บอเนตซึ่งสามารถทำหน้าที่เป็นตัวดูดซับซัลเฟอร์ไดออกไซด์ (SO2) ซึ่งเป็นมลพิษทางอากาศที่สำคัญ ปฏิกิริยาที่เกี่ยวข้องในกระบวนการนี้คือการกระตุ้นหินปูน ผ่านการเผา และการตรึง SO2 ด้วยการก่อตัวของเกลือแคลเซียม ดังแสดงโดยสมการทางเคมีแบบง่าย
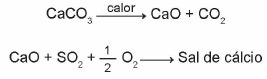
เมื่อพิจารณาปฏิกิริยาที่เกี่ยวข้องกับกระบวนการกำจัดซัลเฟตนี้ สูตรทางเคมีของเกลือแคลเซียมสอดคล้องกับ:
ทางเลือก b)
เนื่องจากปฏิกิริยามีความสมดุล อะตอมที่มีอยู่ในสารตั้งต้นต้องมีปริมาณเท่ากันในผลิตภัณฑ์ ดังนั้น
เกลือที่เกิดขึ้นประกอบด้วย:
1 แคลเซียมอะตอม = Ca
1 อะตอมของกำมะถัน = S
4 อะตอมออกซิเจน = O4
ดังนั้นสูตรทางเคมีของเกลือแคลเซียมจึงสอดคล้องกับCaSO4.
คำถาม 9
(UFPI) ปฏิกิริยาของ X กับ Y แสดงไว้ด้านล่าง พิจารณาว่าสมการใดแทนสมการเคมีที่สมดุลได้ดีที่สุด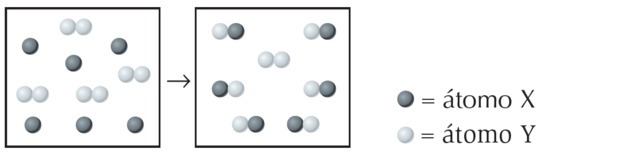
ทางเลือก ก)
ในรูปเราสังเกตว่าสปีชีส์ X เป็นอะตอมเดียวในขณะที่ Y เป็นไดอะตอม นั่นคือมันถูกสร้างขึ้นจากการรวมตัวของ 2 อะตอม ดังนั้น X ทำปฏิกิริยากับ Y2.
ผลิตภัณฑ์ที่เกิดขึ้นแสดงโดย XY สมการไม่สมดุล:
เราปรับสมดุลสมการดังนี้:
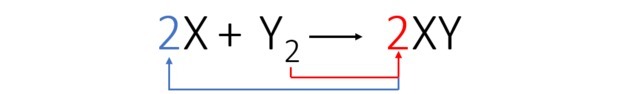
จากสมการที่สมดุล รูปด้านล่างแสดงให้เราเห็นว่าปฏิกิริยาเกิดขึ้นอย่างไรและสัดส่วนของมัน
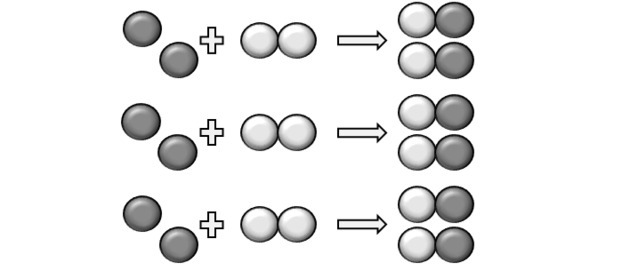
สำหรับปฏิกิริยาที่จะเกิดขึ้นจะต้องมีอัตราส่วนคงที่ ดังนั้นสารประกอบบางชนิดอาจไม่ทำปฏิกิริยา นี่คือสิ่งที่ภาพแสดงให้เห็นเพราะในผลิตภัณฑ์เราจะเห็นว่า Y2 ไม่ตอบสนอง
คำถาม 10
(ศัตรู 2010) การระดมพลเพื่อส่งเสริมโลกที่ดีกว่าสำหรับคนรุ่นต่อไปมีมากขึ้นเรื่อยๆ ปัจจุบันวิธีการขนส่งมวลชนส่วนใหญ่ใช้พลังงานจากการเผาเชื้อเพลิงฟอสซิล ตัวอย่างของภาระที่เกิดจากการปฏิบัตินี้ ก็เพียงพอแล้วที่จะรู้ว่ารถยนต์ผลิตก๊าซคาร์บอนไดออกไซด์โดยเฉลี่ยประมาณ 200 กรัมต่อกิโลเมตรที่เดินทาง
นิตยสารโลกร้อน. ปีที่ 2, 8 การตีพิมพ์ของ Instituto Brasileiro de Cultura Ltda.
หนึ่งในองค์ประกอบหลักของน้ำมันเบนซินคือออกเทน (C8โฮ18). โดยการเผาไหม้ของพลังงานออกเทนทำให้รถสามารถสตาร์ทได้ สมการที่แสดงถึงปฏิกิริยาเคมีของกระบวนการนี้แสดงให้เห็นว่า:
ก) ออกซิเจนถูกปล่อยในกระบวนการในรูปของ O2.
b) ค่าสัมประสิทธิ์ปริมาณสัมพันธ์สำหรับน้ำคือ 8 ต่อ 1 ออกเทน
c) ในกระบวนการมีปริมาณการใช้น้ำเพื่อให้พลังงานถูกปล่อยออกมา
d) ค่าสัมประสิทธิ์ปริมาณสัมพันธ์ของออกซิเจนคือ 12.5 ถึง 1 ออกเทน
e) สัมประสิทธิ์ปริมาณสัมพันธ์ของคาร์บอนไดออกไซด์คือ 9 ต่อ 1 ออกเทน
ทางเลือก d) สัมประสิทธิ์ปริมาณสัมพันธ์สำหรับออกซิเจนคือ 12.5 ถึง 1 ออกเทน
เมื่อสร้างสมดุลของสมการ เราจะพบค่าสัมประสิทธิ์ดังต่อไปนี้:
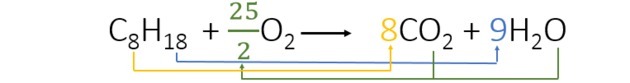
- เราเริ่มสร้างสมดุลด้วยไฮโดรเจนที่ปรากฏขึ้นเพียงครั้งเดียวในแต่ละสมาชิกและมีดัชนีสูงกว่า เนื่องจากมีอะตอมของไฮโดรเจนที่ทำปฏิกิริยาได้ 18 อะตอม ผลิตภัณฑ์จึงมี 2 ตัว เราจึงต้องบวกจำนวนที่คูณด้วย 2 ได้ 18 9 คือสัมประสิทธิ์
- จากนั้นเราบวกค่าสัมประสิทธิ์ 8 หน้าCO2 เพื่อให้มีคาร์บอน 8 ตัวในแต่ละสมาชิกของสมการ
- สุดท้าย แค่เพิ่มปริมาณออกซิเจนในผลิตภัณฑ์แล้วหาค่าที่คูณด้วย 2 ก็ได้ออกซิเจน 25 อะตอม เราก็เลยเลือก 25/2 หรือ 12.5
ดังนั้นสำหรับการเผาไหม้ 1 ออกเทน 12.5 ออกซิเจนจะถูกใช้
คำถาม 11
(Fatec-SP) ลักษณะสำคัญของปุ๋ยคือความสามารถในการละลายน้ำ ดังนั้น อุตสาหกรรมปุ๋ยจึงเปลี่ยนแคลเซียมฟอสเฟตซึ่งมีความสามารถในการละลายในน้ำต่ำมาก ให้กลายเป็นสารประกอบที่ละลายน้ำได้มากกว่ามาก ซึ่งก็คือแคลเซียมซูเปอร์ฟอสเฟต กระบวนการนี้แสดงโดยสมการ:
โดยที่ค่าของ x, y และ z ตามลำดับ:
ก) 4, 2 และ 2
ข) 3, 6 และ 3
ค) 2, 2 และ 2
ง) 5, 2 และ 3
จ) 3, 2 และ 2
ทางเลือก จ) 3, 2 และ 2
โดยใช้วิธีพีชคณิต เราสร้างสมการสำหรับแต่ละองค์ประกอบและเท่ากับจำนวนอะตอมในสารตั้งต้นกับจำนวนอะตอมในผลิตภัณฑ์ ดังนั้น:
สมการสมดุล:
คำถาม 12
ปรับสมดุลสมการด้านล่างโดยใช้วิธีการทดลอง
ตอบ:
สมการประกอบด้วยธาตุไฮโดรเจนและคลอรีน เราสร้างสมดุลขององค์ประกอบโดยการเพิ่มค่าสัมประสิทธิ์ 2 ข้างหน้าผลิตภัณฑ์
สมการไม่จำเป็นต้องมีความสมดุล เนื่องจากมีการปรับปริมาณอะตอมแล้ว
ฟอสฟอรัสมีอะตอมสองอะตอมในสารตั้งต้น ดังนั้นเพื่อให้สมดุลของธาตุนี้ เราจึงปรับปริมาณกรดฟอสฟอริกในผลิตภัณฑ์เป็น 2H3ฝุ่น4.
หลังจากนั้น เราสังเกตว่าไฮโดรเจนมี 6 อะตอมในผลิตภัณฑ์ เราปรับสมดุลปริมาณของธาตุนี้โดยเพิ่มค่าสัมประสิทธิ์ 3 ให้กับสารตั้งต้นที่มีไฮโดรเจนอยู่
ด้วยขั้นตอนก่อนหน้านี้ ปริมาณออกซิเจนได้รับการแก้ไข
เมื่อพิจารณาจากสมการจะพบว่าปริมาณไฮโดรเจนและโบรมีนในผลิตภัณฑ์เพิ่มขึ้นเป็นสองเท่า หากมีอยู่ในรีเอเจนต์ เราจึงเพิ่มค่าสัมประสิทธิ์ 2 ให้กับ HBr เพื่อทำให้ทั้งสองสมดุล องค์ประกอบ
คลอรีนมี 3 อะตอมในผลิตภัณฑ์และเพียง 1 อะตอมในสารตั้งต้น ดังนั้นเราจึงปรับสมดุลโดยใส่ค่าสัมประสิทธิ์ 3 ก่อน HCl
ไฮโดรเจนมี 3 อะตอมในตัวทำปฏิกิริยาและ 2 อะตอมในผลิตภัณฑ์ ในการปรับปริมาณเราแปลงดัชนี H2 ในสัมประสิทธิ์ เราคูณด้วย 3 ที่อยู่ใน HCl แล้ว ได้ผลลัพธ์เป็น 6HCl
เราปรับปริมาณคลอรีนในผลิตภัณฑ์ให้มี 6 อะตอมด้วย ได้ 2AlCl3.
อะลูมิเนียมมี 2 อะตอมในผลิตภัณฑ์ เราปรับปริมาณในตัวทำปฏิกิริยาเป็น 2Al
เราปรับสมดุลปริมาณไฮโดรเจนในผลิตภัณฑ์ถึง 3H2 และเราใส่จำนวน 6 อะตอมของธาตุนั้นให้พอดีในแต่ละเทอมของสมการ
ในสมการไนเตรตเรดิคัล (NO3-) มีดัชนี 2 ในผลิตภัณฑ์ เราแปลงดัชนีเป็นค่าสัมประสิทธิ์ในตัวทำปฏิกิริยาสำหรับ 2AgNO3.
จำเป็นต้องปรับปริมาณเงิน เนื่องจากตอนนี้มี 2 อะตอมในรีเอเจนต์ ดังนั้นเราจึงมี 2Ag อยู่ในผลิตภัณฑ์
ในสารตั้งต้น เรามีไฮโดรเจน 4 อะตอม และเพื่อให้องค์ประกอบนี้สมดุล เราเพิ่มค่าสัมประสิทธิ์ 2 ให้กับผลิตภัณฑ์ HCl
ตอนนี้คลอรีนมี 4 อะตอมในผลิตภัณฑ์ เราจึงปรับปริมาณในรีเอเจนต์เป็น 2Cl2.
เรามีไฮโดรเจน 6 อะตอมในสารตั้งต้น และเพื่อให้สมดุลของธาตุนี้ เราปรับปริมาณน้ำเป็น 3H2โอ.
เรามีคาร์บอนอะตอม 2 อะตอมในสารตั้งต้น และเพื่อให้สมดุลของธาตุนี้ เราปรับปริมาณคาร์บอนไดออกไซด์เป็น 2CO 22.
ออกซิเจนจำเป็นต้องมี 7 อะตอมในสารตั้งต้น และเพื่อให้สมดุลของธาตุนี้ เราปรับปริมาณของโมเลกุลออกซิเจนเป็น 3O2.
เมื่อพิจารณาจากสมการ ไนเตรตเรดิคัล (NO .)3-) มีดัชนี 2 ในผลิตภัณฑ์ เราแปลงดัชนีเป็นสัมประสิทธิ์ 2 ในรีเอเจนต์ AgNONO3.
เรามีอะตอมของเงิน 2 อะตอมในสารตั้งต้น และเพื่อให้สมดุลของธาตุนี้ เราปรับปริมาณของซิลเวอร์คลอไรด์ในผลิตภัณฑ์เป็น 2AgCl
เรามีแคลเซียม 3 อะตอมในผลิตภัณฑ์ และเพื่อให้สมดุลองค์ประกอบนี้ เราปรับปริมาณแคลเซียมไนเตรตในรีเอเจนต์เป็น 3Ca (NO3)2.
เราก็เหลือ 6 อนุมูลอิสระ3- ในสารตั้งต้นและเพื่อให้สมดุลของอนุมูลอิสระนี้ เราปรับปริมาณกรดไนตริกในผลิตภัณฑ์เป็น 6HNO3.
ตอนนี้เรามีไฮโดรเจน 6 อะตอมในผลิตภัณฑ์ และเพื่อให้สมดุลของธาตุนี้ เราปรับปริมาณกรดฟอสฟอริกในรีเอเจนต์เป็น 2H3ฝุ่น4.
เรียนรู้เพิ่มเติมเกี่ยวกับการคำนวณด้วยสมการเคมีได้ที่:
- สมดุลสมการเคมี
- ปริมาณสัมพันธ์
- การคำนวณปริมาณสัมพันธ์
- แบบฝึกหัดเรื่องปริมาณสัมพันธ์
- แบบฝึกหัดตารางธาตุ