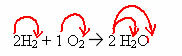ความสามารถในการละลายคือคุณสมบัติทางกายภาพของสารที่จะละลายหรือไม่ละลายในของเหลวที่กำหนด
ถูกเรียก ตัวละลาย, สารเคมีที่ละลายในสารอื่น อู๋ ตัวทำละลาย เป็นสารที่จะละลายตัวถูกละลายเพื่อสร้างผลิตภัณฑ์ใหม่
THE การละลายของสารเคมี เป็นกระบวนการกระจายตัวถูกละลายในตัวทำละลาย ทำให้เกิดสารละลายหรือของผสมที่เป็นเนื้อเดียวกัน
ตัวทำละลายสามารถจำแนกได้เป็น:
- ละลายน้ำได้: คือตัวถูกละลายที่ละลายในตัวทำละลาย
- ละลายได้เล็กน้อย: เป็นตัวทำละลายที่ละลายได้ยากในตัวทำละลาย
- ไม่ละลายน้ำ: คือตัวถูกละลายที่ไม่ละลายในตัวทำละลาย
หลักการทั่วไปในการละลายคือ: "ชอบละลายชอบ”. ซึ่งหมายความว่าตัวทำละลายมีขั้วมีแนวโน้มที่จะละลายในตัวทำละลายที่มีขั้ว เช่นเดียวกับสารที่ไม่มีขั้ว
ดูตัวอย่างบางส่วน:
- ไฮโดรคาร์บอน สารประกอบที่มีอยู่ในน้ำมันเบนซิน ไม่มีขั้วและมีความสามารถในการละลายน้ำได้น้อยซึ่งเป็นขั้ว
- แอลกอฮอล์ เช่น เอทานอลและเมทานอล มีขั้วเนื่องจากมีออกซิเจนอยู่ในสายโซ่คาร์บอน ดังนั้นจึงสามารถละลายได้ในน้ำ
- เกลือมีความสามารถในการละลายต่างกัน พวกเขาสามารถจำแนกได้เป็น: เกลือที่ละลายน้ำได้และเกลือที่ไม่ละลายน้ำในทางปฏิบัติ
ค่าสัมประสิทธิ์การละลาย
อู๋
ค่าสัมประสิทธิ์การละลาย (Cs) กำหนดความจุสูงสุดของตัวถูกละลายที่ละลายในปริมาณตัวทำละลายที่กำหนด ทั้งนี้ขึ้นอยู่กับสภาวะอุณหภูมิโดยสรุป ค่าสัมประสิทธิ์การละลายคือปริมาณของตัวถูกละลายที่จำเป็นในการทำให้อิ่มตัวปริมาณตัวทำละลายมาตรฐานในสภาวะที่กำหนด
ตัวอย่างเช่น พิจารณาสถานการณ์ต่อไปนี้:
ในแก้วน้ำเกลือ (NaCl) ในขั้นต้น เกลือจะหายไปในน้ำ
อย่างไรก็ตาม หากเติมเกลือมากขึ้น ในบางจุด เกลือจะเริ่มสะสมที่ก้นแก้ว
ทั้งนี้เนื่องจากน้ำซึ่งเป็นตัวทำละลายได้ถึงขีดจำกัดความสามารถในการละลายและความเข้มข้นสูงสุดแล้ว นี้เรียกอีกอย่างว่า จุดอิ่มตัว.
ตัวถูกละลายที่ยังคงอยู่ที่ด้านล่างของภาชนะและไม่ละลายเรียกว่าตัวก้นหรือตกตะกอน
เกี่ยวกับ จุดอิ่มตัว, โซลูชั่นแบ่งออกเป็นสามประเภท:
- สารละลายไม่อิ่มตัว: เมื่อปริมาณตัวถูกละลายน้อยกว่า Cs
- สารละลายอิ่มตัว: เมื่อปริมาณตัวถูกละลายเท่ากับ Cs มันคือขีดจำกัดความอิ่มตัว
- สารละลายอิ่มตัวยิ่งยวด: เมื่อปริมาณตัวถูกละลายมากกว่า Cs
ผลิตภัณฑ์ความสามารถในการละลาย
ดังที่เราได้เห็นแล้ว ความสามารถในการละลายได้แสดงถึงปริมาณของตัวถูกละลายที่ละลายในสารละลาย อู๋ ผลิตภัณฑ์ที่ละลายน้ำได้ (Kps) เป็นค่าคงที่สมดุลที่เกี่ยวข้องโดยตรงกับความสามารถในการละลาย
การคำนวณช่วยให้คุณสามารถระบุได้ว่าสารละลายมีความอิ่มตัว ไม่อิ่มตัว หรืออิ่มตัวด้วยการตกตะกอน การคำนวณนี้เกี่ยวข้องกับสมดุลการละลายและความเข้มข้นของไอออนในสารละลาย
ทั้งนี้เนื่องจากผลคูณของความสามารถในการละลายหมายถึงสมดุลการละลายของสารไอออนิก
เข้าใจมากขึ้นเกี่ยวกับ ตัวทำละลายและตัวทำละลาย.
เส้นกราฟความสามารถในการละลาย
ความสามารถในการละลายทางเคมีของสารภายใต้การเปลี่ยนแปลงของอุณหภูมิไม่เป็นเชิงเส้น ความแปรผันของความสามารถในการละลาย ตามฟังก์ชันของอุณหภูมิ เรียกว่าเส้นกราฟความสามารถในการละลาย
สารที่เป็นของแข็งส่วนใหญ่มีค่าสัมประสิทธิ์การละลายเพิ่มขึ้นตามอุณหภูมิที่เพิ่มขึ้น ดังนั้นความสามารถในการละลายของวัสดุแต่ละชนิดจึงเกิดขึ้นตามสัดส่วน ขึ้นอยู่กับอุณหภูมิ
สารแต่ละชนิดมีเส้นกราฟความสามารถในการละลายของตัวเองสำหรับตัวทำละลายชนิดใดชนิดหนึ่ง
ความแปรผันของความสามารถในการละลายถือเป็นเส้นตรงเมื่อไม่อยู่ภายใต้อิทธิพลของอุณหภูมิ หากต้องการทราบความแปรผัน จำเป็นต้องดูกราฟความสามารถในการละลาย
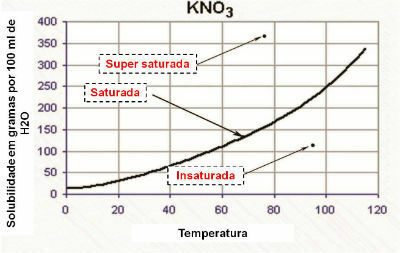
เส้นกราฟความสามารถในการละลาย
ในกราฟ กราฟความสามารถในการละลายแสดงให้เห็นว่าสารละลายคือ:
- อิ่มตัว: เมื่อจุดอยู่บนเส้นกราฟความสามารถในการละลาย
- ไม่อิ่มตัว: เมื่อจุดอยู่ต่ำกว่าเส้นกราฟความสามารถในการละลาย
- อิ่มตัวเป็นเนื้อเดียวกัน: เมื่อจุดอยู่เหนือเส้นกราฟความสามารถในการละลาย
อ่านเพิ่มเติมเกี่ยวกับ ความเข้มข้นของสารละลาย.
สูตรสัมประสิทธิ์การละลาย
สูตรคำนวณค่าสัมประสิทธิ์การละลายคือ
ซี = 100. ม1/m2
ที่ไหน:
Cs: ค่าสัมประสิทธิ์การละลาย
ม1: มวลของตัวถูกละลาย
ม2: มวลตัวทำละลาย
ต้องการทราบข้อมูลเพิ่มเติม? อ่าน เคมีภัณฑ์ และ การเจือจางของสารละลาย.
การออกกำลังกาย
1. (Fuvest-SP) นักเคมีอ่านคำแนะนำต่อไปนี้ในขั้นตอนที่อธิบายไว้ในคู่มือห้องปฏิบัติการของเขา:
"ละลายคลอไรด์ 5.0 กรัม ในน้ำ 100 มล. ที่อุณหภูมิห้อง..." .
ในบรรดาสารต่างๆ ข้างล่างนี้ มีกล่าวถึงข้อใดในข้อความบ้าง?
ก) Cl2.
ข) CCl4.
ค) NaClO
ง) NH4ค.
จ) AgCl
ง) NH4ค.
2. (UFRGS-RS) เกลือบางชนิดมีความสามารถในการละลายในน้ำเท่ากับ 135g/L ที่ 25°C โดยการละลายเกลือนี้อย่างสมบูรณ์ 150 กรัมในน้ำหนึ่งลิตร ที่อุณหภูมิ 40°C และทำให้ระบบเย็นลงอย่างช้าๆ เป็น 25°C จะได้ระบบที่เป็นเนื้อเดียวกันซึ่งสารละลายจะเป็น:
ก) เจือจาง
ข) เข้มข้น
c) ไม่อิ่มตัว
ง) อิ่มตัว
จ) อิ่มตัวยิ่งยวด
จ) อิ่มตัวยิ่งยวด
3. (Mackenzie-SP) ตัวอย่างทั่วไปของสารละลายอิ่มตัวยิ่งยวดคือ:
ส่วนน้ำแร่.
b) เซรั่มโฮมเมด
c) โซดาในภาชนะปิด
ง) แอลกอฮอล์ 46° GL
จ) น้ำส้มสายชู
c) โซดาในภาชนะปิด
4. (PUC-RJ) สังเกตรูปด้านล่างซึ่งแสดงถึงความสามารถในการละลายในหน่วยกรัมต่อ 100 กรัมของ H2O ของเกลืออนินทรีย์ 3 ตัวในช่วงอุณหภูมิที่กำหนด:
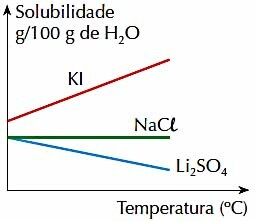
ตรวจสอบข้อความที่ถูกต้อง:
ก) ความสามารถในการละลายของเกลือทั้ง 3 ตัวจะเพิ่มขึ้นตามอุณหภูมิ
b) การเพิ่มขึ้นของอุณหภูมิเอื้อต่อการละลายของ Li2เท่านั้น4.
c) ความสามารถในการละลายของ KI มากกว่าความสามารถในการละลายของเกลืออื่นๆ ในช่วงอุณหภูมิที่แสดง
d) ความสามารถในการละลายของ NaCl จะแปรผันตามอุณหภูมิ
จ) ความสามารถในการละลายของเกลือ 2 ตัวลดลงตามอุณหภูมิ
c) ความสามารถในการละลายของ KI มากกว่าความสามารถในการละลายของเกลืออื่นๆ ในช่วงอุณหภูมิที่แสดง