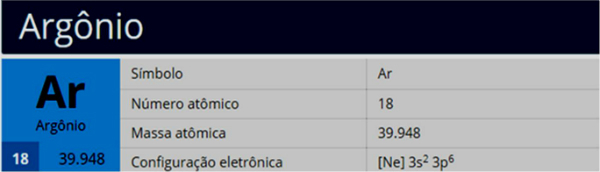
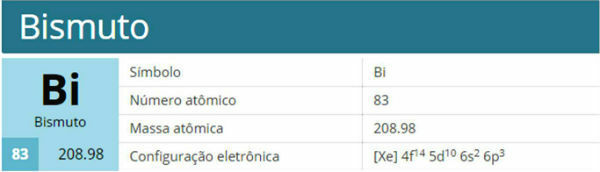
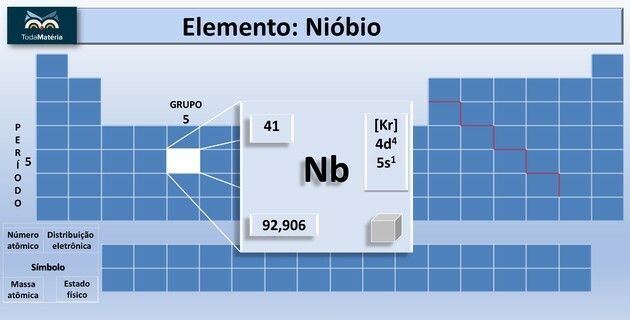
โมเลกุลเป็นชุดของอะตอมที่เหมือนกันหรือต่างกันที่เชื่อมต่อกันด้วยพันธะโควาเลนต์
สารเคมีเหล่านี้เป็นกลางทางไฟฟ้าและเป็นตัวแทนของหน่วยการก่อตัวของสาร
มีโมเลกุลอย่างง่าย เช่น ออกซิเจน (O2) ของอากาศที่เราหายใจเข้าไป อย่างไรก็ตาม ยังมีสารประกอบเชิงซ้อน เช่น บัคกี้บอล (อะตอมของคาร์บอน 60 อะตอมรวมกันเป็นทรงกลม) ซึ่งเป็นโมเลกุลที่ใหญ่ที่สุดเท่าที่เคยพบในอวกาศ
การศึกษาโมเลกุล
พันธะโควาเลนต์ในโมเลกุลสอดคล้องกับการใช้อิเล็กตรอนร่วมกัน โดยปกติระหว่างองค์ประกอบที่ไม่ใช่โลหะ
ดูโมเลกุลของน้ำเป็นตัวอย่างของสารประกอบอย่างง่าย
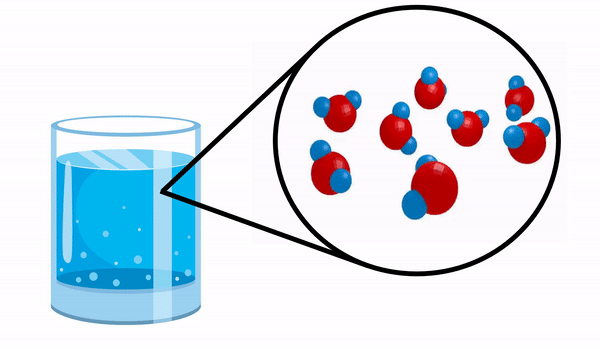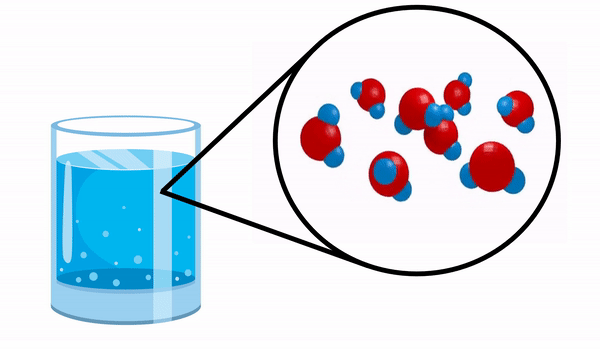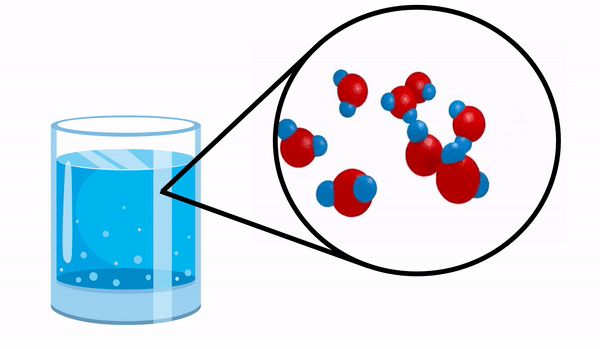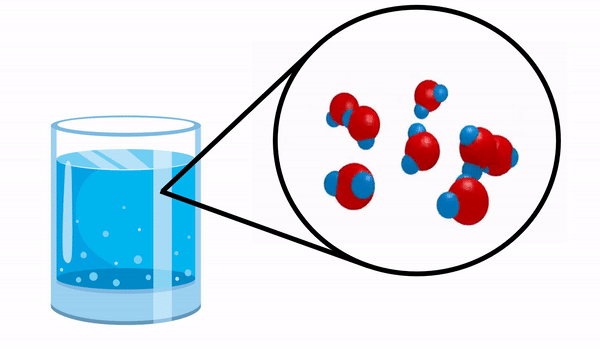
เมื่อเราสังเกตแก้วด้วย น้ำ เราไม่รู้ว่าสารนี้ประกอบด้วยโมเลกุล H หลายตัว2โอ. สูตรนี้บ่งชี้ว่าน้ำประกอบด้วย 3 อะตอม ได้แก่ ไฮโดรเจน 2 อะตอม และออกซิเจน 1 อะตอม ซึ่งใช้อิเล็กตรอนร่วมกัน
น้ำตาล ซึ่งเราใช้ทำน้ำผลไม้ให้หวานและทำเค้ก ก็ประกอบด้วยโมเลกุลเช่นกัน หน่วยสร้างน้ำตาลคือซูโครส

โมเลกุลนี้ซับซ้อนกว่ามาก เนื่องจากมี45 อะตอม เชื่อมต่อ ประกอบด้วยอะตอมของคาร์บอน 12 อะตอม ไฮโดรเจน 22 อะตอม และออกซิเจน 11 อะตอม
โมเลกุลเป็นโครงสร้างของมวลโมเลกุลที่รู้จัก แต่ก็มีโมเลกุลขนาดใหญ่เช่นกัน ซึ่งเป็น "โครงสร้างขนาดยักษ์" ที่ก่อตัวขึ้นจากอะตอมจำนวนมากจนองค์ประกอบของพวกมันไม่ได้กำหนดไว้ ตัวอย่างของประเภทนี้คือเพชร ซึ่งเป็นโมเลกุลขนาดใหญ่ที่เกิดจากอะตอมจำนวนมากของ
คาร์บอน ในเครือข่ายโควาเลนต์พันธะโควาเลนต์
พันธะเคมีโควาเลนต์ถูกสร้างขึ้นระหว่างสองอะตอมเมื่อพวกมันแบ่ง share อิเล็กตรอน ภายนอกมากขึ้น (ของความจุ) โมเลกุลสามารถมีพันธะได้สองประเภท:
พันธะโควาเลนต์โมเลกุล: คู่ของอิเล็กตรอนของอะตอมพันธะทั้งสองถูกใช้ร่วมกัน

พันธบัตรโควาเลนต์ (dative): อิเลคตรอนที่ใช้ร่วมกันมาจากอะตอมเดียวที่เกี่ยวข้อง
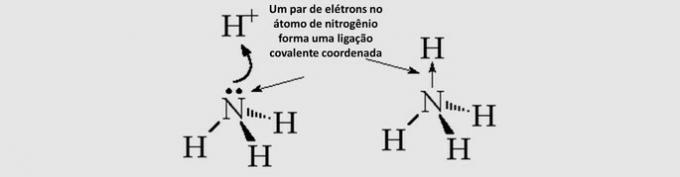
เรขาคณิตโมเลกุล
เมื่อโมเลกุลถูกสร้างขึ้น อะตอมจะถูกจัดตำแหน่งในลักษณะต่างๆ เพื่อให้การจัดเรียงเชิงพื้นที่มีเสถียรภาพมากขึ้น ดังนั้นคอมโพสิตจึงมีรูปทรงที่แตกต่างกัน
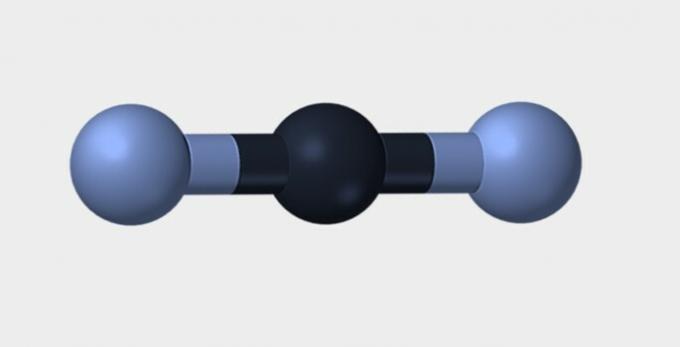
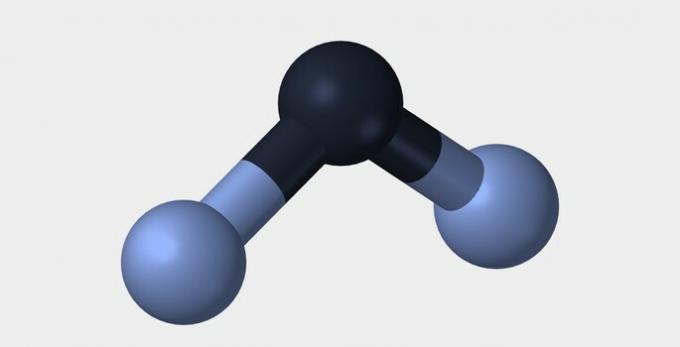
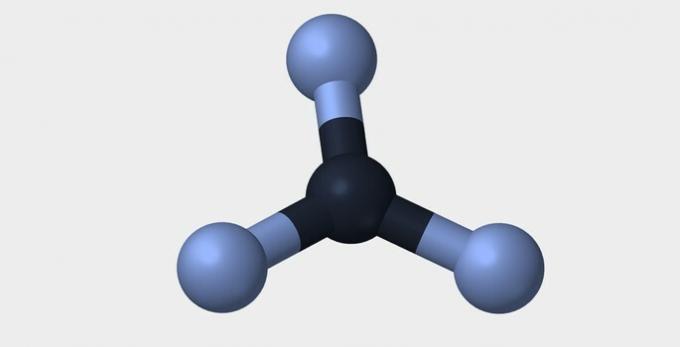
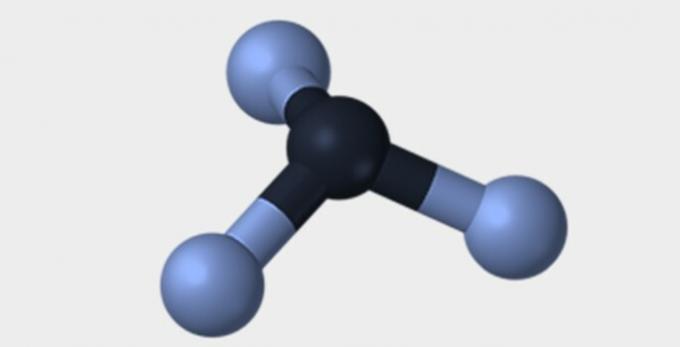
ต่อไปนี้คือรูปทรงเรขาคณิตบางส่วนที่โมเลกุลสามารถมีได้
| เรขาคณิตโมเลกุล | ||
|---|---|---|
| เชิงเส้น | เชิงมุม | สามเหลี่ยม |
 |
 |
 |
| เสี้ยม | จัตุรมุข | แปดด้าน |
 |
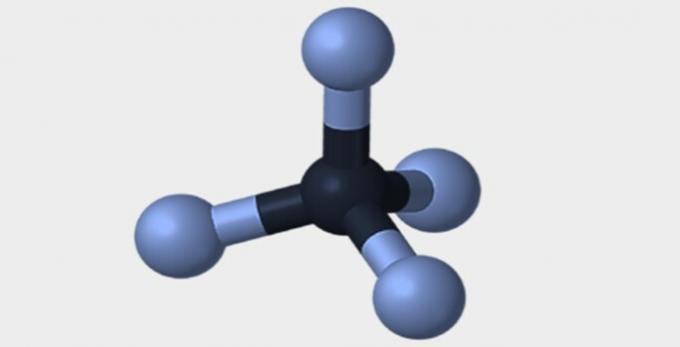 |
 |
โมเลกุลมีขั้วและไม่มีขั้ว
โมเลกุลถูกจำแนกตาม ขั้ว.
โมเลกุลไม่มีขั้ว: ไม่มีความแตกต่างในอิเล็กโตรเนกาติวีตี้ระหว่างอะตอม
| ไนโตรเจน (N2) | คาร์บอนไดออกไซด์ (CO2) |
|---|---|
 |
 |
ไนโตรเจน (N2) เป็นโมเลกุลที่ไม่มีขั้วเพราะมันถูกสร้างขึ้นโดยมัน องค์ประกอบทางเคมี ดังนั้นจึงไม่มีความแตกต่างในอิเล็กโตรเนกาติวีตี้ คาร์บอนไดออกไซด์ (CO2) ไม่มีขั้วเนื่องจากรูปทรงเชิงเส้น ซึ่งทำให้แรงดึงดูดของออกซิเจนโดยอิเล็กตรอนคงที่
โมเลกุลขั้ว: มีความแตกต่างของอิเล็กโตรเนกาติวีตี้ระหว่างอะตอมกับขั้วบวกและขั้วลบ
| น้ำ (H2อ) | แอมโมเนีย (NH3) |
|---|---|
 |
 |
ในทั้งสองตัวอย่าง เราจะเห็นว่าอะตอมกลาง ออกซิเจน และไนโตรเจน มีคู่อิเล็กตรอนที่ไม่คู่กันซึ่งก่อตัวเป็นเมฆอิเล็กตรอน เนื่องจากมีเมฆอิเล็กทรอนิกส์อยู่รอบๆ อะตอมกลางมากกว่าพันธะเคมีที่ก่อตัวขึ้น โมเลกุลจึงมีขั้ว
ตัวอย่างของโมเลกุล
| สาร | คุณสมบัติ | โมเลกุล | สูตร |
|---|---|---|---|
| ไฮโดรเจน | เชื้อเพลิงและมีอยู่มากมายในเปลือกโลก | 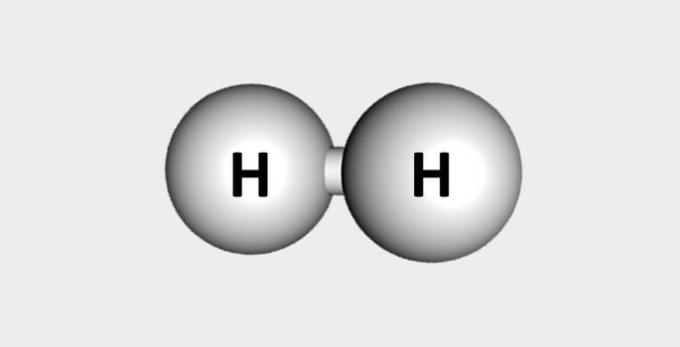 |
โฮ2 |
| ออกซิเจน | จำเป็นสำหรับการหายใจและมีส่วนร่วมในปฏิกิริยาเคมีต่างๆ | 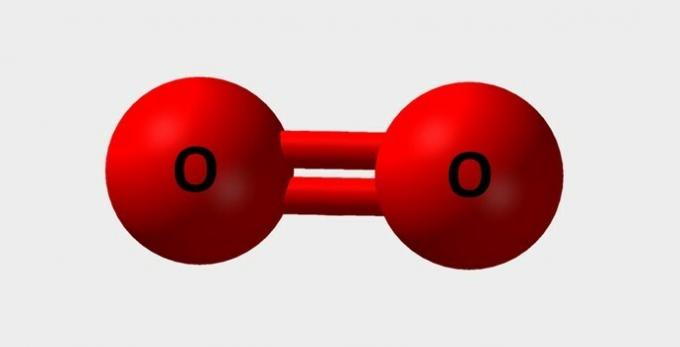 |
อู๋2 |
| กำมะถัน | ผงสีเหลืองใช้ทำสีย้อม | 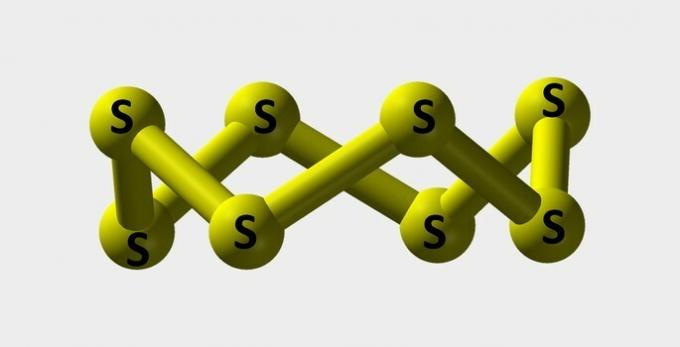 |
ส8 |
| คาร์บอนไดออกไซด์ | ใช้ในถังดับเพลิงและสารทำความเย็น | 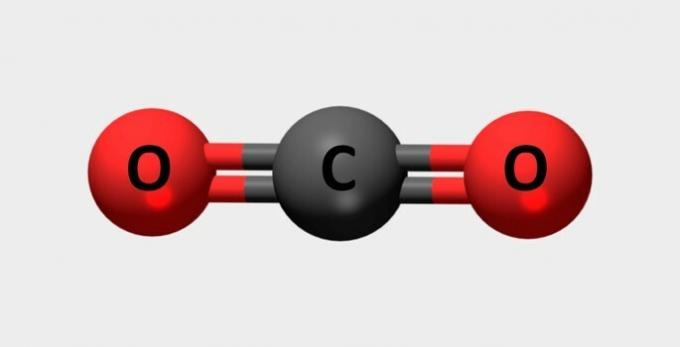 |
CO2 |
| เอทานอล | แอลกอฮอล์ทั่วไปใช้เป็นเชื้อเพลิงและในน้ำหอม | 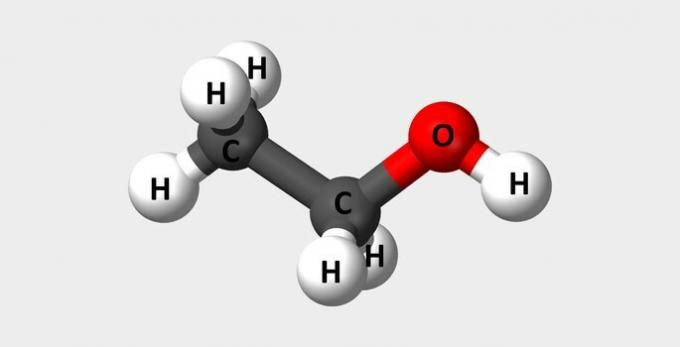 |
ค2โฮ6อู๋ |
อย่าลืมตรวจสอบข้อความเหล่านี้ในหัวข้อที่เกี่ยวข้องกับสิ่งที่คุณเพิ่งเรียนรู้:
- ชีวโมเลกุล
- สารประกอบอินทรีย์
- มวลโมเลกุล
- กฎออคเต็ต
- พันธะเคมี
- ขั้วเชื่อมต่อ
- กองกำลังระหว่างโมเลกุล