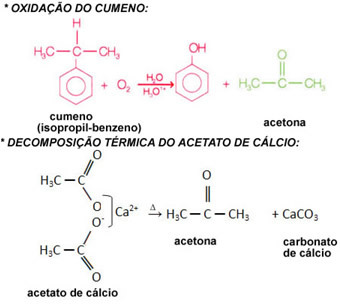
ไนโอเบียม (Nb) เป็นองค์ประกอบทางเคมีของเลขอะตอม 41 ที่อยู่ในกลุ่ม 5 ของตารางธาตุ
เป็นโลหะทรานซิชันที่มีอยู่ตามธรรมชาติในสถานะของแข็ง ซึ่งถูกค้นพบในปี 1801 โดยนักเคมีชาวอังกฤษ Charles Hatchett
แร่ธาตุที่มีไนโอเบียมเป็นของหายากในโลก แต่มีมากในบราซิล ซึ่งเป็นประเทศที่มีโลหะสำรองมากที่สุด
เนื่องจากคุณสมบัติ การนำไฟฟ้าสูงและทนต่อการกัดกร่อน องค์ประกอบนี้มีการใช้งานมากมายตั้งแต่การผลิตเหล็กไปจนถึงการผลิตจรวด
ต่อไป เราจะแนะนำองค์ประกอบทางเคมีนี้และลักษณะเฉพาะที่ทำให้มีความสำคัญมาก
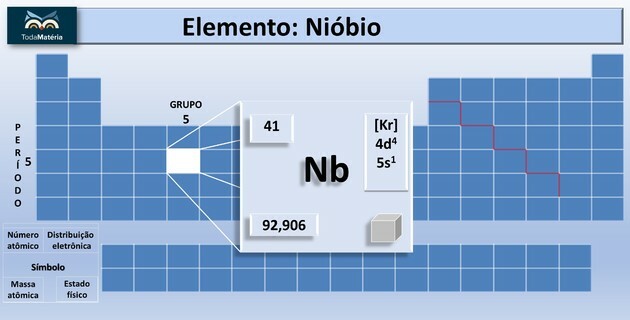
ไนโอเบียมคืออะไร?
ไนโอเบียมเป็นโลหะทนไฟ กล่าวคือ ทนต่อความร้อนและการสึกหรอได้ดีมาก
โลหะในกลุ่มนี้ได้แก่ ไนโอเบียม ทังสเตน โมลิบดีนัม แทนทาลัม และรีเนียม โดยไนโอเบียมจะเบาที่สุด
ไนโอเบียมเกิดขึ้นในธรรมชาติในแร่ธาตุ ซึ่งมักจะเชื่อมโยงกับองค์ประกอบอื่นๆ ซึ่งส่วนใหญ่เป็นแทนทาลัม เนื่องจากทั้งสองมีคุณสมบัติทางเคมีกายภาพที่คล้ายกันมาก
องค์ประกอบทางเคมีนี้จัดเป็นโลหะทรานซิชันในตารางธาตุ มีความสดใส มีความแข็งต่ำ มีความต้านทานไฟฟ้าไหลผ่านต่ำและทนต่อการกัดกร่อน
คุณสมบัติทางกายภาพของไนโอเบียม
| สภาพร่างกาย | แข็งที่อุณหภูมิห้อง |
|---|---|
| สีและรูปลักษณ์ | สีเทาเมทัลลิก |
| ความหนาแน่น | 8.570 ก./ซม.3 |
| จุดหลอมเหลว | 2468°C |
| จุดเดือด | 4742 °C |
| โครงสร้างผลึก | ลูกบาศก์ตรงกลางของร่างกาย - CCC |
การนำความร้อน |
54.2 วัตต์ m-1 K-1 |
คุณสมบัติทางเคมีของไนโอเบียม
| การจำแนกประเภท | โลหะทรานซิชัน |
|---|---|
| เลขอะตอม | 41 |
| บล็อก | d |
| กลุ่ม | 5 |
| เวลาที่แน่นอน | 5 |
| น้ำหนักอะตอม | 92,90638 u |
| รังสีปรมาณู | 1,429 Å |
| ไอออนทั่วไป | Nb5+ และ Nb3+ |
| อิเล็กโตรเนกาติวีตี้ | 1.6 Pauling |
ข้อได้เปรียบหลักของการใช้โลหะนี้คือปริมาณของธาตุนี้ในหน่วยกรัมเท่านั้นที่สามารถ ดัดแปลงตันเหล็ก ทำให้โลหะเบาขึ้น ทนต่อการกัดกร่อน และอื่นๆ มีประสิทธิภาพ
ไนโอเบียมพบได้ที่ไหน?
เมื่อเทียบกับสารอื่นๆ ที่มีอยู่ในธรรมชาติ ไนโอเบียมมีความเข้มข้นต่ำในสัดส่วน 24 ส่วนในล้านส่วน
โลหะนี้พบได้ในประเทศต่อไปนี้: บราซิล แคนาดา ออสเตรเลีย อียิปต์ สาธารณรัฐประชาธิปไตยคองโก กรีนแลนด์ รัสเซีย ฟินแลนด์ กาบอง และแทนซาเนีย
ไนโอเบียมในบราซิล
ในปี 1950 แหล่งแร่ไพโรคลอร์ที่ใหญ่ที่สุดซึ่งมีโลหะนี้ถูกค้นพบในบราซิลโดยนักธรณีวิทยาชาวบราซิล Djalma Guimarães
แร่จำนวนมากที่มีไนโอเบียมอยู่ในบราซิล ซึ่งเป็นผู้ผลิตรายใหญ่ที่สุดของโลก ซึ่งถือครองแร่โลหะสำรองมากกว่า 90%
เขตสงวนที่สำรวจตั้งอยู่ในรัฐ Minas Gerais, Amazonas, Goiás และ Rondônia
แร่ไนโอเบียม
ไนโอเบียมพบได้ในธรรมชาติโดยเชื่อมโยงกับองค์ประกอบทางเคมีอื่นๆ แร่ธาตุมากกว่า 90 ชนิดที่ประกอบด้วยไนโอเบียมและแทนทาลัมในธรรมชาติเป็นที่ทราบกันดีอยู่แล้ว
ในตารางด้านล่าง เราจะเห็นแร่บางชนิดที่มีไนโอเบียม ลักษณะสำคัญ และปริมาณไนโอเบียมที่มีอยู่ในวัสดุแต่ละชนิด
| โคลัมไบท์ แทนทาไลท์ | |
|---|---|
 | |
| องค์ประกอบ: | (เฟ, Mn)(Nb, ตา)2อู๋6 |
| ปริมาณไนโอเบียม (สูงสุด): | 76% ของ Nb2อู๋5 |
| คุณสมบัติ: |
|
| ไพโรคลอไรท์ | |
|---|---|
 | |
| องค์ประกอบ: | (ที่2,ที่นี่)2(Nb, Ti)(O, F)7 |
| ปริมาณไนโอเบียม (สูงสุด): | 71% ของ Nb2อู๋5 |
| คุณสมบัติ: |
|
| โลพาไรต์ | |
|---|---|
 | |
| องค์ประกอบ: | (ค, นา, ค)2(Ti, Nb)2อู๋6 |
| ปริมาณไนโอเบียม (สูงสุด): | 20% ของ Nb2อู๋5 |
| คุณสมบัติ: |
|
การสำรวจไนโอเบียม
แร่ไนโอเบียมได้รับการเปลี่ยนแปลงจนกว่าจะมีการสร้างผลิตภัณฑ์ที่จะวางตลาด
ขั้นตอนกระบวนการสามารถสรุปได้ดังนี้:
- การขุด
- ความเข้มข้นของไนโอเบียม
- การกลั่นไนโอเบียม
- ผลิตภัณฑ์ไนโอเบียม
การขุดเกิดขึ้นในบริเวณที่มีแร่สำรอง ซึ่งสกัดโดยใช้วัตถุระเบิดและขนส่งโดยสายพานไปยังจุดที่มีความเข้มข้น
ความเข้มข้นเกิดขึ้นจากการแตกตัวของแร่ การบดทำให้ผลึกแร่ละเอียดขึ้นมากและใช้ and การแยกแม่เหล็ก เศษเหล็กจะถูกลบออกจากแร่
ในการกลั่นไนโอเบียม กำมะถัน น้ำ ฟอสฟอรัส และตะกั่วจะถูกลบออก
หนึ่งในผลิตภัณฑ์ที่มีไนโอเบียมคือโลหะผสมเหล็กไนโอเบียมซึ่งผลิตขึ้นตามสมการต่อไปนี้:
กระบวนการนี้เรียกว่า aluminothermia ซึ่งแร่เข้มข้นถูกผสมในเครื่องปฏิกรณ์ด้วยเศษเหล็กหรือเหล็กออกไซด์
โลหะออกไซด์ทำปฏิกิริยากับอะลูมิเนียมภายใต้อุณหภูมิสูง ทำให้เกิดผลิตภัณฑ์ที่น่าสนใจ
ผลิตภัณฑ์ไนโอเบียมเชิงพาณิชย์มากที่สุดคือ:
- ไนโอเบียมเข้มข้น: ฐานที่มี 58% Nb2อู๋5.
- โลหะผสมเหล็ก-ไนโอเบียม: มีไนโอเบียม 65%
- ออกไซด์ที่มีความบริสุทธิ์สูง: ใช้ในการผลิตวัสดุพิเศษ
ไนโอเบียมมีไว้เพื่ออะไร?
คุณสมบัติของไนโอเบียมทำให้องค์ประกอบนี้เป็นที่ต้องการมากขึ้นและมีการใช้งานมากมาย
นับตั้งแต่การค้นพบในปี 1905 ได้มีการศึกษาการใช้ไนโอเบียม เมื่อนักเคมีชาวเยอรมัน แวร์เนอร์ ฟอน โบลตัน ผลิตธาตุในรูปแบบบริสุทธิ์
ยุค 50 แสดงถึงการค้นหาการใช้งานไนโอเบียมที่ยอดเยี่ยม จนกระทั่งถึงตอนนั้นยังไม่มีการผลิตในปริมาณมาก
ในช่วงเวลานี้ สงครามเย็นได้จุดประกายความสนใจในโลหะชนิดนี้เพื่อนำไปใช้ในส่วนประกอบด้านอวกาศ
ด้านล่างนี้คือรายการวิธีการใช้ไนโอเบียม
โลหะผสม

การเพิ่มไนโอเบียมในโลหะผสมจะเพิ่มความสามารถในการชุบแข็ง กล่าวคือ ความสามารถในการชุบแข็งเมื่อถูกความร้อนและเย็นลง ดังนั้น วัสดุที่มีไนโอเบียมสามารถผ่านกรรมวิธีทางความร้อนจำเพาะได้
ความสัมพันธ์ของไนโอเบียมกับคาร์บอนและไนโตรเจนส่งผลดีต่อคุณสมบัติทางกลของโลหะผสม เช่น ความแข็งแรงเชิงกลและความทนทานต่อการสึกหรอจากการเสียดสี
เอฟเฟกต์เหล่านี้มีประโยชน์เนื่องจากสามารถขยายการใช้งานในอุตสาหกรรมของโลหะผสมได้
ตัวอย่างเช่น เหล็กกล้าเป็นโลหะผสมที่เกิดจากเหล็กและคาร์บอน การเพิ่มไนโอเบียมในโลหะผสมนี้สามารถมีข้อดีสำหรับ:
- อุตสาหกรรมยานยนต์: ทำให้รถมีน้ำหนักเบาและทนต่อการชนกันมากขึ้น
- การก่อสร้าง: ปรับปรุงความสามารถในการเชื่อมของเหล็กและให้การอ่อนตัว
- อุตสาหกรรมท่อขนส่ง: ช่วยให้โครงสร้างผนังบางและเส้นผ่านศูนย์กลางใหญ่ขึ้น โดยไม่กระทบต่อความปลอดภัย
ซุปเปอร์อัลลอยด์

ซูเปอร์อัลลอยเป็นโลหะผสมที่มีความทนทานต่ออุณหภูมิสูงและความแข็งแรงทางกลสูง โลหะผสมที่มีไนโอเบียมทำให้วัสดุนี้มีประโยชน์ในการผลิตกังหันเครื่องบินหรือการผลิตพลังงาน
ข้อดีของการทำงานที่อุณหภูมิสูงทำให้ซูเปอร์อัลลอยประกอบด้วยเครื่องยนต์ไอพ่นประสิทธิภาพสูง
แม่เหล็กตัวนำยิ่งยวด

ความเป็นตัวนำยิ่งยวดของไนโอเบียมทำให้สารประกอบของไนโอเบียม-เจอร์เมเนียม ไนโอเบียม-สแกนเดียม และไนโอเบียม-ไททาเนียมถูกนำมาใช้ใน:
- สแกนเนอร์ของเครื่อง MRI
- เครื่องเร่งอนุภาค เช่น Large Hadron Collider
- การตรวจจับรังสีแม่เหล็กไฟฟ้าและการศึกษารังสีคอสมิกด้วยวัสดุที่มีไนโอเบียมไนไตรท์
ออกไซด์
การใช้งานอื่นๆ สำหรับไนโอเบียมจะอยู่ในรูปของออกไซด์ ซึ่งส่วนใหญ่เป็น Nb2อู๋5. การใช้งานหลักคือ:
- เลนส์สายตา
- ตัวเก็บประจุเซรามิก
- เซ็นเซอร์วัดค่า pH
- ชิ้นส่วนเครื่องยนต์
- เครื่องประดับ
ประวัติและการค้นพบไนโอเบียม
ในปี ค.ศ. 1734 แร่บางส่วนที่เป็นของสะสมส่วนตัวของ John Winthrop ถูกนำออกจากอเมริกาไปยังอังกฤษ และสิ่งของเหล่านี้เป็นส่วนหนึ่งของคอลเล็กชันของ British Museum ในลอนดอน
เมื่อเข้าร่วม Royal Society นักเคมีชาวอังกฤษ Charles Hatchett มุ่งเน้นไปที่การตรวจสอบองค์ประกอบของแร่ที่มีอยู่ในพิพิธภัณฑ์ นี่คือวิธีที่ในปี 1801 เขาแยกองค์ประกอบทางเคมีออกมาในรูปของออกไซด์ และตั้งชื่อมันว่า columbium และแร่ที่สกัดมันออกมาเป็น columbite
ในปี 1802 นักเคมีชาวสวีเดน Anders Gustaf Ekeberg ได้รายงานการค้นพบองค์ประกอบทางเคมีใหม่และตั้งชื่อมันว่าแทนทาลัม โดยอ้างอิงถึงลูกชายของ Zeus ในเทพนิยายกรีก
ในปี ค.ศ. 1809 นักเคมีและนักฟิสิกส์ชาวอังกฤษ วิลเลียม ไฮด์ วอลลาสตัน วิเคราะห์องค์ประกอบทั้งสองนี้และสังเกตว่าองค์ประกอบเหล่านี้มีลักษณะที่คล้ายคลึงกันมาก
ด้วยเหตุนี้ ตั้งแต่ปี ค.ศ. 1809 ถึง ค.ศ. 1846 โคลอมเบียมและแทนทาลัมจึงถือเป็นองค์ประกอบเดียวกัน
ต่อมา Heinrich Rose นักแร่วิทยาและนักเคมีชาวเยอรมัน ซึ่งกำลังตรวจสอบแร่ columbite ตั้งข้อสังเกตว่ามีแทนทาลัมด้วย
โรสพบว่ามีองค์ประกอบอื่นที่คล้ายกับแทนทาลัมและเรียกมันว่านีโอเบียสโดยอ้างอิงถึงนิโอเบ ธิดาของแทนทาลัสตามตำนานเทพเจ้ากรีก
ในปี 1864 Christian Bromstrand ชาวสวีเดนสามารถแยกไนโอเบียมออกจากตัวอย่างคลอไรด์ที่ถูกทำให้ร้อนในบรรยากาศไฮโดรเจน
ในปี 1950 สหภาพเคมีบริสุทธิ์และเคมีประยุกต์ (IUPAC) ได้อนุมัติไนโอเบียมเป็นชื่อทางการ แทนที่จะเป็น columbium เนื่องจากเป็นองค์ประกอบทางเคมีเดียวกัน
สรุปไนโอเบียม
องค์ประกอบทางเคมี: ไนโอเบียม | |||
|---|---|---|---|
| สัญลักษณ์ | Nb | ผู้ค้นพบ | Charles Hatchett |
| เลขอะตอม | 41 | มวลอะตอม | 92,906 u |
| กลุ่ม | 5 | เวลาที่แน่นอน | 5 |
| การจำแนกประเภท | โลหะทรานซิชัน | การกระจายทางอิเล็กทรอนิกส์ | [Kr]4วัน35s2 |
| คุณสมบัติ |
|
||
| แร่หลัก |
|
||
| ผลิตภัณฑ์หลัก |
|
||
| แอปพลิเคชั่น |
|
||
| อุบัติเหต | ในโลก |
|
|
| ในบราซิล |
|
แบบฝึกหัดและการสอบเข้า
1. (Enem/2018) ในเทพปกรณัมกรีก Niobia เป็นลูกสาวของ Tantalus ซึ่งเป็นตัวละครสองตัวที่รู้จักกันในเรื่องความทุกข์ทรมานของพวกเขา ธาตุเคมีที่มีเลขอะตอม (Z) เท่ากับ 41 มีคุณสมบัติทางเคมีและฟิสิกส์คล้ายกับธาตุที่มีเลขอะตอม 73 มากจนสับสน
ดังนั้น เพื่อเป็นเกียรติแก่อักขระสองตัวนี้ในเทพปกรณัมกรีก องค์ประกอบเหล่านี้จึงได้รับชื่อไนโอเบียม (Z = 41) และแทนทาลัม (Z = 73) องค์ประกอบทางเคมีทั้งสองนี้ได้รับความสำคัญทางเศรษฐกิจอย่างมากในด้านโลหะวิทยา ในการผลิต ตัวนำยิ่งยวดและในอุตสาหกรรมระดับไฮเอนด์อื่นๆ เนื่องจากคุณสมบัติทางเคมีและทางกายภาพ physical ร่วมกันทั้งสอง
คีน, เอส. ช้อนที่หายไป: และเรื่องจริงอื่นๆ เกี่ยวกับความบ้าคลั่ง ความรัก และความตายจากองค์ประกอบทางเคมี รีโอเดจาเนโร: Zahar, 2011 (ดัดแปลง).
ความสำคัญทางเศรษฐกิจและเทคโนโลยีขององค์ประกอบเหล่านี้เนื่องจากคุณสมบัติทางเคมีและทางกายภาพที่คล้ายคลึงกันนั้นเกิดจาก their
ก) มีอิเล็กตรอนในระดับย่อย f
b) เป็นองค์ประกอบของการเปลี่ยนแปลงภายใน
c) อยู่ในกลุ่มเดียวกันในตารางธาตุ
d) มีอิเล็กตรอนชั้นนอกสุดที่ระดับ 4 และ 5 ตามลำดับ
จ) อยู่ในตระกูลอัลคาไลน์เอิร์ธและอัลคาไลน์ตามลำดับ
ทางเลือกที่ถูกต้อง: c) อยู่ในกลุ่มเดียวกันในตารางธาตุ
ตารางธาตุแบ่งออกเป็น 18 กลุ่ม (ครอบครัว) โดยแต่ละกลุ่มจะรวบรวมองค์ประกอบทางเคมีที่มีคุณสมบัติคล้ายคลึงกัน
ความคล้ายคลึงกันเหล่านี้เกิดขึ้นเนื่องจากองค์ประกอบของกลุ่มมีจำนวนอิเล็กตรอนเท่ากันในเปลือกเวเลนซ์
การกระจายทางอิเล็กทรอนิกส์และการเพิ่มอิเล็กตรอนจากระดับย่อยที่มีพลังมากที่สุดไปยังระดับย่อยที่อยู่นอกสุด เราจะพบกลุ่มที่องค์ประกอบทั้งสองอยู่
| ไนโอเบียม | |
|
จำหน่าย อิเล็กทรอนิกส์ |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p65s2 4 วัน3 |
|
ผลรวมของ อิเล็กตรอน |
มีพลังมากขึ้น + ภายนอกมากขึ้น 4 วัน3 + 5 วินาที2 = 5 อิเล็กตรอน |
| กลุ่ม | 5 |
| แทนทาลัม | |
|
จำหน่าย อิเล็กทรอนิกส์ |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4 วัน10 5p66s2 4f145 วัน3 |
|
ผลรวมของ อิเล็กตรอน |
มีพลังมากขึ้น + ภายนอกมากขึ้น 5 วัน3 + 6s2 = 5 อิเล็กตรอน |
| กลุ่ม | 5 |
ธาตุไนโอเบียมและแทนทาลัม:
- อยู่ในกลุ่มเดียวกันในตารางธาตุ
- พวกมันมีอิเล็กตรอนชั้นนอกสุดที่ระดับ 5 และ 6 ตามลำดับ และอยู่ในคาบที่ 5 และ 6
- พวกมันมีอิเล็กตรอนในระดับย่อย d ดังนั้นจึงเป็นองค์ประกอบเฉพาะกาลภายนอก
2. (IFPE/2018) บราซิลเป็นผู้ผลิตไนโอเบียมรายใหญ่ที่สุดของโลก โดยคิดเป็นสัดส่วนมากกว่า 90% ของโลหะสำรองนี้ ไนโอเบียม สัญลักษณ์ Nb ใช้ในการผลิตเหล็กพิเศษ และเป็นโลหะที่ทนทานต่อการกัดกร่อนและอุณหภูมิสูงที่สุดชนิดหนึ่ง สารประกอบ Nb2อู๋5 เป็นสารตั้งต้นของโลหะผสมและสารประกอบไนโอเบียมเกือบทั้งหมด ทำเครื่องหมายทางเลือกด้วยมวลที่ต้องการของNb2อู๋5 เพื่อให้ได้ไนโอเบียม 465 กรัม ให้ไว้: Nb = 93 g/mol และ O = 16 g/mol
ก) 275 กรัม
ข) 330 กรัม
ค) 930 กรัม
ง) 465 กรัม
จ) 665 กรัม
ทางเลือกที่ถูกต้อง: จ) 665 ก.
สารประกอบตั้งต้นของไนโอเบียมคือ Nb ออกไซด์2อู๋5 และไนโอเบียมที่ใช้ในโลหะผสมอยู่ในรูปแบบธาตุ Nb
ดังนั้นเราจึงมีความสัมพันธ์เชิงปริมาณสัมพันธ์ต่อไปนี้:
1 โมลของ Nb2อู๋5 สร้าง Nb 2 โมลเนื่องจากไนโอเบียมออกไซด์ประกอบด้วย 2 อะตอมของโลหะนี้
ขั้นตอนที่ 1: คำนวณจำนวนโมลของไนโอเบียมที่ผลิตซึ่งสอดคล้องกับ 465 กรัม
ถ้าจากการคำนวณเราพบว่ามวลของไนโอเบียมเท่ากับ 5 โมล แสดงว่าปริมาณโมลของ Nb2อู๋5 ที่ใช้เป็นครึ่งหนึ่งของค่านี้เพราะ:
ขั้นตอนที่ 2: คำนวณมวลโมลาร์ของไนโอเบียมออกไซด์
ขั้นตอนที่ 3: คำนวณมวลของไนโอเบียมออกไซด์ที่สอดคล้องกับ 2.5 โมล
3. (UECE/2015) บราซิลถือครองไนโอเบียมสำรอง 98% ของโลก ซึ่งมีการใช้งานทางอุตสาหกรรมมากมาย เช่น ในการผลิตเครื่องประดับ รากฟันเทียมที่มีสารก่อภูมิแพ้สูง อิเล็กโทรเซรามิก แม่เหล็กตัวนำยิ่งยวด เครื่องเรโซแนนซ์แม่เหล็ก โลหะผสม เหรียญพิเศษ และในการผลิต เหล็ก. สำหรับไนโอเบียม ให้ทบทวนข้อความด้านล่างและทำเครื่องหมายทางเลือกที่แท้จริงเท่านั้น
ก) อิเล็กตรอนดิฟเฟอเรนเชียลอยู่ในเปลือกสุดท้าย
b) เป็นองค์ประกอบที่เป็นตัวแทน
c) อิเล็กโตรเนกาติวีตี้ต่ำกว่าวาเนเดียม
ง) เป็นช่วงที่สี่ของตารางธาตุ
ทางเลือกที่ถูกต้อง: ก) อิเล็กตรอนดิฟเฟอเรนเชียลอยู่ในเปลือกสุดท้าย
เมื่อทำการแจกแจงไนโอเบียมทางอิเล็กทรอนิกส์ จะเห็นได้ว่าอิเล็กตรอนดิฟเฟอเรนเชียลอยู่ในเปลือกสุดท้าย
เนื่องจากมีอิเล็กตรอนดิฟเฟอเรนเชียลในระดับย่อย d จึงเป็นองค์ประกอบทรานซิชันภายนอก
เนื่องจากระดับชั้นนอกสุดอยู่ในชั้นที่ห้า ไนโอเบียมจึงอยู่ในช่วงที่ห้าของตาราง
อิเล็กโตรเนกาติวีตี้เป็นคุณสมบัติที่เกี่ยวข้องกับความสามารถขององค์ประกอบในการดึงดูดอิเล็กตรอนและแตกต่างกันไปตาม according รัศมีอะตอม: ยิ่งรัศมีอะตอมเล็กลง แรงดึงดูดของอิเล็กตรอนก็จะยิ่งมากขึ้น ดังนั้น. ก็ยิ่งมากขึ้น อิเล็กโตรเนกาติวีตี้
เมื่อพิจารณาจากตารางที่มีค่าอิเล็กโตรเนกาติวีตี้จะเห็นว่าไนโอเบียมและวานาเดียมมีค่าใกล้เคียงกับ 1.6 Pauling
4. (UEA/2014) ไอโซโทปธรรมชาติของไนโอเบียมคือ 93หมายเหตุ จำนวนนิวตรอนในไอโซโทปนี้คือ
ก) 41.
ข) 52.
ค) 93.
ง) 134.
จ) 144.
ทางเลือกที่ถูกต้อง: b) 52.
ไอโซโทปเป็นอะตอมขององค์ประกอบทางเคมีที่มีเลขมวลต่างกัน
มวลอะตอมสอดคล้องกับผลรวมของโปรตอนและนิวตรอนของธาตุ
จำนวนโปรตอนแสดงถึงเลขอะตอมขององค์ประกอบทางเคมี และสำหรับไอโซโทปจะไม่เปลี่ยนแปลง
ดังนั้นการแปรผันมวลของไอโซโทปจึงเกิดขึ้นเนื่องจากจำนวนนิวตรอนต่างกัน
หากเลขอะตอมของไนโอเบียมคือ 41 การคำนวณจะกำหนดจำนวนนิวตรอน:
5. (IFMG/2015) องค์ประกอบทางเคมีไนโอเบียม Nb ได้รับการตั้งชื่อตามเทพธิดากรีก Niobe บราซิลเป็นผู้ผลิตโลหะรายใหญ่ที่สุดของโลก โดยคิดเป็น 75% ของการผลิต เนื่องจากความเสถียรทางความร้อนของโลหะผสม ไนโอเบียมจึงถูกนำมาใช้ในการผลิตโลหะผสมที่มีความแข็งแรงสูงเป็นพิเศษสำหรับเครื่องยนต์ อุปกรณ์ขับเคลื่อน และวัสดุตัวนำยิ่งยวดต่างๆ เมื่อสังเกตตำแหน่งของไนโอเบียมในตารางธาตุ ถูกต้องแล้ว กล่าวได้ว่า:
ก) ระดับย่อยที่มีพลังมากที่สุดของคุณจะเป็นระดับย่อย ง.
b) เป็นองค์ประกอบที่เป็นของตระกูลโลหะอัลคาไล
c) สร้างสารประกอบไอออนิกกับโลหะอื่นๆ
d) ไพเพอร์ของมันจะมีรัศมีอะตอมมากกว่าธาตุบริสุทธิ์
ทางเลือกที่ถูกต้อง: ก) ระดับย่อยที่มีพลังมากที่สุดของคุณจะเป็นระดับย่อย ง.
เมื่อดูที่ตารางธาตุ เราจะเห็นว่าไนโอเบียมมีลักษณะเป็นองค์ประกอบการเปลี่ยนแปลงภายนอก ซึ่งอยู่ในกลุ่มที่ 5 ของตารางธาตุ เนื่องจากระดับย่อยที่มีพลังมากที่สุดคือ d
เราอาจได้รับข้อมูลนี้โดยแจกจ่ายทางอิเล็กทรอนิกส์
เนื่องจากเป็นโลหะ องค์ประกอบนี้จึงทำให้โลหะเชื่อมต่อกับโลหะอื่นๆ เช่นเดียวกับในโลหะผสม เหล็กไนโอเบียมหรือพันธะโควาเลนต์ด้วยการใช้อิเล็กตรอนร่วมกันเช่นเดียวกับไนโอเบียมออกไซด์ Nb2อู๋5.
6. (UFSC/2003) Niobium ถูกค้นพบในปี 1801 โดย Charles Hatchett นักเคมีชาวอังกฤษ บราซิลถือครองการผลิตไนโอเบียมเข้มข้นประมาณ 93% ของโลก เงินฝากที่ใหญ่ที่สุดตั้งอยู่ในรัฐ Minas Gerais, Goiás และ Amazonas โลหะส่วนใหญ่ใช้ในการผลิตโลหะผสมเหล็ก-ไนโอเบียมและโลหะผสมที่ซับซ้อนมากขึ้น ซึ่งถูกนำมาใช้ในการสร้างกังหันขับเคลื่อนไอพ่น จรวด และยานอวกาศ ออกไซด์ของออกไซด์นี้ใช้ในการผลิตเลนส์แสงสำหรับแว่นตา กล้องถ่ายภาพ และอุปกรณ์เกี่ยวกับสายตาอื่นๆ ให้ไว้ (Z = 41) เกี่ยวกับไนโอเบียม ทำเครื่องหมายข้อเสนอที่ถูกต้อง
(01) ไนโอเบียมเมื่อสูญเสียอิเล็กตรอน 3 ตัวถือว่ามีการกำหนดค่าของคริปทอน
(02) ไนโอเบียมสามารถสร้างออกไซด์ของโลหะชนิด M ได้2อู๋5 ใน2อู๋3.
(04) สัญลักษณ์ทางเคมีของไนโอเบียมคือ Ni
(08) ไนโอเบียมเป็นโลหะทรานซิชัน
(16) โลหะผสมเหล็กไนโอเบียมเป็นตัวอย่างของสารละลายที่เป็นของแข็ง
ทางเลือกที่ถูกต้อง: 02 + 08 + 16 = 26
(01) ไม่ถูกต้อง
| องค์ประกอบ | การกระจายทางอิเล็กทรอนิกส์ |
| 36กรุ | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 |
|
41Nb 41Nb3+ |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4 วัน3 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 4p6 4 วัน2 |
(02) ถูกต้อง
พิจารณาเลขออกซิเดชัน 3+ และ 5+ สำหรับไนโอเบียม สามารถสร้างสารประกอบได้:
| ออกซิเดชันหมายเลข 5+ | ออกซิเดชันหมายเลข 3+ |
| Nb2อู๋5 | Nb2อู๋3 |
(04) ไม่ถูกต้อง
Ni เป็นสัญลักษณ์ของธาตุนิกเกิล สัญลักษณ์ของไนโอเบียมคือ Nb
(08) ถูกต้อง
ไนโอเบียมเป็นโลหะทรานซิชันภายนอกที่อยู่ในกลุ่ม 5 ของตารางธาตุ
(16) ถูกต้อง
สารละลายที่เป็นของแข็งสอดคล้องกับส่วนผสมของส่วนประกอบตั้งแต่สองชิ้นขึ้นไปในเฟสเดียวกัน ซึ่งเป็นของแข็งที่พบได้ทั่วไปในโลหะ
7. (UERJ/2013) ไนโอเบียมเป็นโลหะที่พบในแหล่งสะสมตามธรรมชาติ ส่วนใหญ่อยู่ในรูปของออกไซด์
ในเงินฝากที่มีไนโอเบียมที่มีเลขออกซิเดชัน +5 สูตรสำหรับออกไซด์เด่นของโลหะนี้สอดคล้องกับ:
ก) NbO5
ข) Nb5อู๋
ค) Nb5อู๋2
ง) Nb2อู๋5
ทางเลือกที่ถูกต้อง: d) Nb2อู๋5
ออกซิเจนสร้างพันธะสองพันธะและมีเลขออกซิเดชันคงที่ ซึ่งก็คือ 2
ดังนั้น ในการสร้างไนโอเบียมออกไซด์ ออกซิเจนจำเป็นต้องจับกับ 2 อะตอมของโลหะนี้
ไนโอเบียมมีสถานะออกซิเดชันต่างกัน ด้วยเลขออกซิเดชัน 3+ จะจับกับออกซิเจน 3 ตัว และด้วย Nox 5+ จะทำให้เกิดสารประกอบ: Nb2อู๋5 โดยที่อะตอมไนโอเบียม 2 อะตอมจับกับออกซิเจน 5 อะตอม
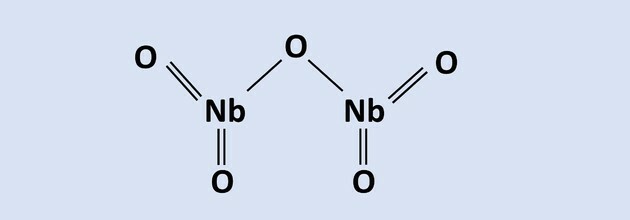
อ่านข้อความเพื่อตอบคำถามข้อ 8 ถึง 10
ไนโอเบียมเป็นโลหะที่มีความสำคัญทางเทคโนโลยีอย่างมากและมีแหล่งสำรองหลักของโลกอยู่ใน
บราซิล ในรูปของแร่ไพโรคลอร์ ประกอบด้วย Nb2อู๋5. ในกระบวนการหนึ่งของการแยกโลหะวิทยา จะใช้อลูมิโนเทอร์เมียต่อหน้าเฟออกไซด์2อู๋3ทำให้เกิดโลหะผสมของไนโอเบียมและเหล็กและอะลูมิเนียมออกไซด์เป็นผลพลอยได้ ปฏิกิริยาของกระบวนการนี้แสดงอยู่ในสมการ:
ในธรรมชาติ ไนโอเบียมปรากฏในรูปแบบของไอโซโทปไนโอเบียม-93 ที่เสถียร แต่รู้จักไอโซโทปสังเคราะห์ที่ไม่เสถียรหลายไอโซโทปซึ่งสลายตัวโดยการปล่อยรังสี หนึ่งในนั้นคือไนโอเบียม-95 ซึ่งสลายตัวเป็นองค์ประกอบโมลิบดีนัม-95
(Systems.dnpm.gov.br; เทคโนโลยี โลหะ. มาเตอร์ คนขุดแร่, เซาเปาโล, วี. 6 ไม่ 4 หน้า 185-191 เม.ย.-มิ.ย. 2010 และ G. Audi et al./Nuclear Physics A 729 (2003) 3–128. ดัดแปลง)
8. (FGV/2019) ในปฏิกิริยาอะลูมิโนเทอร์เมียเพื่อให้ได้โลหะผสมของไนโอเบียมและเหล็ก โดยพิจารณาจากปริมาณสารสัมพันธ์ที่นำเสนอในสมการสมดุล จำนวนอิเล็กตรอนทั้งหมดที่เกี่ยวข้องในกระบวนการคือ
ก) 6.
ข) 12.
ค) 18.
ง) 24.
จ) 36.
ทางเลือกที่ถูกต้อง: จ) 36.
ปฏิกิริยารีดอกซ์เกิดขึ้นกับการสูญเสียและรับอิเล็กตรอน
เมื่อองค์ประกอบลดลงจะได้รับอิเล็กตรอนและเมื่อองค์ประกอบถูกออกซิไดซ์จะสูญเสียอิเล็กตรอน
เมื่อองค์ประกอบลดลง ก็จะเป็นตัวออกซิไดซ์ ในขณะที่เมื่อองค์ประกอบออกซิไดซ์ ก็จะเป็นตัวรีดิวซ์
ด้วยวิธีนี้ จำนวนอิเล็กตรอนที่สูญเสียไปโดยองค์ประกอบหนึ่งและมอบให้กับอีกองค์ประกอบหนึ่งจึงเท่ากัน
| ธาตุ | NOX | ปฏิกิริยา | อิเล็กตรอน | |
| ไนโอเบียม |
+5 3Nb2อู๋5 |
0 6Nb |
ลดกระหน่ำ | 3.2.5 = 30 และ- กำไร |
| เหล็ก |
+3 ศรัทธา2อู๋3 |
0 2Fe |
ลดกระหน่ำ | 2.3 = 6 และ- กำไร |
| อลูมิเนียม |
0 12อัล |
+3 6Al2อู๋3 |
ออกซิเดชัน | 6.2.3 = 36 และ- สูญหาย |
ประจุอะลูมิเนียมบนผลิตภัณฑ์อะลูมิเนียมออกไซด์คือ 3+ นั่นคือ อะลูมิเนียมแต่ละตัวสูญเสียอิเล็กตรอนไป 3 ตัว
แต่ในผลิตภัณฑ์ เรามีอะลูมิเนียม 12 อะตอม ซึ่งทำให้จำนวนอิเล็กตรอนทั้งหมดที่เกี่ยวข้องในกระบวนการนี้:
12. 3 = 36 อิเล็กตรอน
9. (FGV/2019) ในการดำเนินการ aluminothermia สำหรับการผลิตไนโอเบียมและโลหะผสมเหล็กที่มีปริมาณสารสัมพันธ์ของ Nb2อู๋5 และเฟ2อู๋3 และการใช้อลูมิเนียมโลหะส่วนเกินทำให้เกิดอัล 6.12 ตัน2อู๋3. ผลรวมของปริมาณไนโอเบียมและธาตุเหล็กที่คาดว่าจะได้รับในการดำเนินการนี้เป็นโมลเป็น
ก) 6 × 104
ข) 6 × 106
ค) 8 × 103
ง) 8 × 104
จ) 8 × 106
ทางเลือกที่ถูกต้อง: ง) 8 × 104.
ขั้นตอนที่ 1: คำนวณมวลโมลาร์ของ Al2อู๋3
ขั้นตอนที่ 2: คำนวณจำนวนโมลของAl2อู๋3
ขั้นตอนที่ 3: ดำเนินการความสัมพันธ์ปริมาณสัมพันธ์
ในสมการทางเคมี เราจะเห็นว่ามีความสัมพันธ์กัน คือ ไนโอเบียม 6 โมล อลูมิเนียม 6 โมล และเหล็ก 2 โมล
โดยอัตราส่วนของจำนวนโมลที่เกิดขึ้น เรามี:
และผลรวมของปริมาณไนโอเบียมและธาตุเหล็กเป็นโมลคือ:
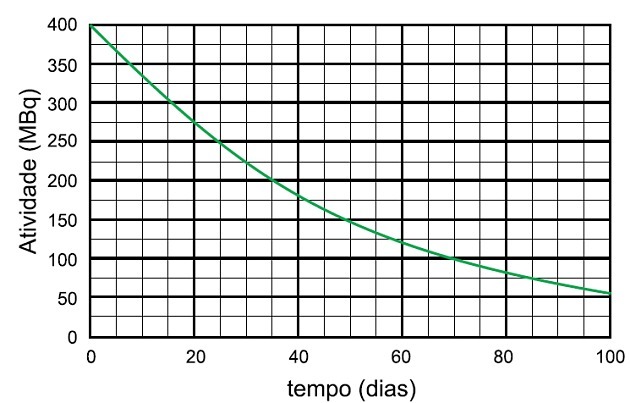
ในกระบวนการสลายตัวของไอโซโทปรังสีไนโอเบียม-95 เวลาที่ใช้สำหรับกิจกรรมของตัวอย่างนี้จะสลายตัวเป็น 25 MBq และชื่อของสปีชีส์ที่ปล่อยออกมาคือ
ก) 140 วันและนิวตรอน
b) 140 วันและโปรตอน
c) 120 วันและโปรตอน
ง) 120 วันและอนุภาค ß–.
จ) 140 วันและอนุภาค ß–.
ทางเลือกที่ถูกต้อง: จ) 140 วันและอนุภาค ß–.
ครึ่งชีวิตเป็นเวลาที่ใช้สำหรับตัวอย่างกัมมันตภาพรังสีเพื่อลดกิจกรรมลงครึ่งหนึ่ง
ในกราฟเราจะเห็นว่ากิจกรรมกัมมันตภาพรังสีเริ่มต้นที่ 400 MBq ดังนั้นครึ่งชีวิตคือเวลาที่กิจกรรมสลายตัวเป็น 200 MBq ซึ่งเท่ากับครึ่งหนึ่งของช่วงเริ่มต้น
เราวิเคราะห์ในกราฟว่าเวลานี้ 35 วัน
เพื่อให้กิจกรรมลดลงครึ่งหนึ่งอีกครั้ง อีก 35 วันผ่านไป และกิจกรรมเพิ่มจาก 200 MBq เป็น 100 MBq เมื่ออีก 35 วันผ่านไป นั่นคือจาก 400 เป็น 100 MBq ผ่านไป 70 วัน
สำหรับตัวอย่างที่จะสลายตัวได้มากถึง 25 MBq ต้องใช้เวลาครึ่งชีวิต 4 ครั้ง
ซึ่งสอดคล้องกับ:
4 x 35 วัน = 140 วัน
ในการสลายกัมมันตภาพรังสี การปล่อยอาจเป็นอัลฟา เบต้า หรือแกมมา
รังสีแกมมาเป็นคลื่นแม่เหล็กไฟฟ้า
การปล่อยแอลฟามีประจุบวกและลดลง 4 หน่วยในมวล และ 2 หน่วยในเลขอะตอมของธาตุที่สลายตัว เปลี่ยนเป็นธาตุอื่น
การปล่อยเบต้าเป็นอิเล็กตรอนความเร็วสูงที่เพิ่มเลขอะตอมของธาตุที่สลายตัวหนึ่งหน่วย เปลี่ยนเป็นองค์ประกอบอื่น
ไนโอเบียม-95 และโมลิบดีนัม-95 มีมวลเท่ากัน จึงเกิดการปล่อยเบต้าเนื่องจาก: