อู๋ แผนภาพเฟส เป็นกราฟที่ให้คุณกำหนดสถานะทางกายภาพของสาร ณ เวลาใดเวลาหนึ่ง โดยรู้อุณหภูมิและความดันของสารนั้น
การวัดในห้องปฏิบัติการใช้เพื่อสร้างแผนภาพเฟสของสารที่กำหนด
แผนภาพนี้แบ่งออกเป็นสามส่วน ซึ่งแสดงถึงสถานะของแข็ง ของเหลว และไอ
จุดบนเส้นที่คั่นภูมิภาคเหล่านี้บ่งบอกถึงค่าของอุณหภูมิและความดันที่สารสามารถอยู่ในสองสถานะ
แผนภาพเฟสมีองค์ประกอบดังต่อไปนี้:
- เส้นโค้งของ ฟิวชั่น: แยกพื้นที่ที่สอดคล้องกับสถานะของแข็งและของเหลว
- เส้นโค้งของ การทำให้กลายเป็นไอ: แยกพื้นที่ที่สอดคล้องกับเฟสของเหลวและไอ
- เส้นโค้งของ ระเหิด: แยกพื้นที่ที่สอดคล้องกับเฟสของแข็งและไอระเหย
- ทริปเปิ้ลพอยต์: จุดตัดของเส้นโค้งทั้งสาม (ฟิวชั่น การกลายเป็นไอ และการระเหิด) จุดนี้บ่งชี้ค่าอุณหภูมิและความดันที่สารสามารถอยู่ในสามสถานะพร้อมกันได้
- จุดวิกฤต: ระบุอุณหภูมิสูงสุดที่สารเป็นไอ จากจุดนั้นไป จะไม่สามารถแยกความแตกต่างระหว่างสถานะของเหลวและไอระเหยได้อีกต่อไป ที่อุณหภูมิสูงกว่าจุดวิกฤต สารจะกลายเป็นก๊าซ
ในรูปด้านล่าง เรานำเสนอการแสดงแผนภาพเฟส:

อ่านเพิ่มเติมได้ที่: การเปลี่ยนแปลงสภาพร่างกาย.
เส้นโค้งหลอมละลาย
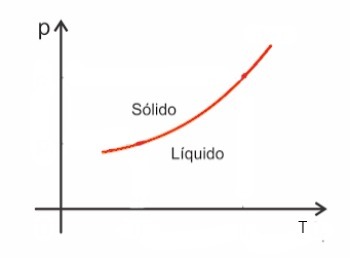
โดยทั่วไป สารจะมีปริมาตรเพิ่มขึ้นเมื่อเกิดการหลอมรวม และในทางกลับกัน ปริมาณจะลดลงเมื่อแข็งตัว ด้วยเหตุนี้ ความดันที่เพิ่มขึ้นทำให้จุดหลอมเหลวเพิ่มขึ้น (อุณหภูมิหลอมเหลว)
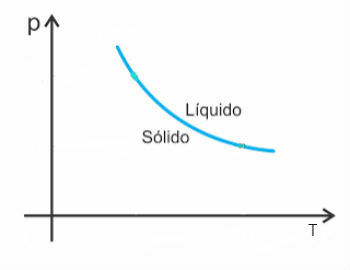
อย่างไรก็ตาม มีข้อยกเว้นบางประการในหมู่พวกเขา น้ำซึ่งในการหลอมละลายในปริมาตรลดลง ในกรณีนี้ ความดันที่เพิ่มขึ้นจะทำให้จุดหลอมเหลวลดลง
ดังนั้นเส้นโค้งการหลอมเหลวของสารเหล่านี้จะมีลักษณะดังนี้:
ตัวอย่าง
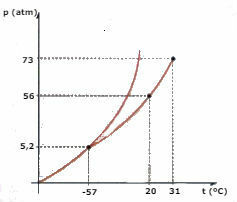
พิจารณาไดอะแกรมเฟส CO2 (คาร์บอนไดออกไซด์) แสดงด้านล่างและตอบคำถาม:
ก) CO. อยู่ในระยะใด2 , เมื่ออุณหภูมิของคุณอยู่ที่ -60 °C และความดันอยู่ที่ 50 atm?
b) CO. จำนวนหนึ่ง2 ของเหลวอยู่ภายใต้ความดัน 56 atm และถูกคุมขังในภาชนะ ถ้าของเหลวถูกทำให้ร้อนโดยรักษาความดันให้คงที่ ค่าอุณหภูมิที่จะกลายเป็นไอคืออะไร?
c) ค่าอุณหภูมิและความดันของจุดสามจุดของCO .เป็นเท่าใด2?
d) น้ำแข็งแห้งชิ้นหนึ่ง (CO2) อยู่ภายใต้แรงดัน 2 atm มันถูกให้ความร้อนโดยรักษาแรงดันคงที่ ในช่วงเวลาหนึ่งการเปลี่ยนแปลงเฟสเริ่มเกิดขึ้น การเปลี่ยนแปลงนี้ชื่ออะไร
ความละเอียด:
ก) เมื่อสังเกตจากแผนภาพ เราสรุปได้ว่า CO2 จะอยู่ในสถานะของแข็ง
b) การระเหยจะเกิดขึ้นเมื่ออุณหภูมิถึง 20 องศาเซลเซียส
ค) จุดสามจุดสอดคล้องกับจุดตัดของเส้นโค้งทั้งสามในกรณีของCO2, เมื่อมีอุณหภูมิ -57°C และความดัน 5.2 atm สถานะทางกายภาพทั้งสามสามารถอยู่ร่วมกันได้
d) การระเหิดจะเกิดขึ้น
หากต้องการเรียนรู้เพิ่มเติม ให้อ่านเพิ่มเติม:
- การแข็งตัว
- จุดหลอมเหลวและจุดเดือด
- การระเหย
- การควบแน่น
แก้ไขแบบฝึกหัด
1) ศัตรู - 2000
แม้กระทั่งทุกวันนี้ เป็นเรื่องธรรมดามากที่ผู้คนจะใช้ภาชนะดินเผา (โถหรือหม้อเซรามิกที่ไม่เคลือบ) เพื่อประหยัดน้ำที่อุณหภูมิต่ำกว่าสภาพแวดล้อม นี้เป็นเพราะ:
ก) ดินเหนียวแยกน้ำออกจากสิ่งแวดล้อม โดยรักษาอุณหภูมิให้ต่ำกว่าตัวมันเองเสมอ ราวกับว่ามันเป็นโฟม
ข) ดินเหนียวมีอำนาจในการ "แช่แข็ง" น้ำเนื่องจากองค์ประกอบทางเคมี ในปฏิกิริยาน้ำจะสูญเสียความร้อน
c) ดินเหนียวเป็นรูพรุนทำให้น้ำไหลผ่านได้ ส่วนหนึ่งของน้ำนี้ระเหย นำความร้อนจากมะรุมและน้ำที่เหลือซึ่งจะถูกทำให้เย็นลง
d) ดินเหนียวเป็นรูพรุนทำให้น้ำตกลงที่ด้านนอกของเหยือก น้ำภายนอกมักมีอุณหภูมิสูงกว่าภายในเสมอ
จ) มะรุมเป็นตู้เย็นธรรมชาติชนิดหนึ่ง ปล่อยสารดูดความชื้นที่ลดอุณหภูมิของน้ำตามธรรมชาติ
ทางเลือก ค: ดินเหนียวมีรูพรุนทำให้น้ำผ่านได้ ส่วนหนึ่งของน้ำนี้ระเหย นำความร้อนจากมะรุมและน้ำที่เหลือซึ่งจะถูกทำให้เย็นลง
2) Ita - 2013
พิจารณาแผนภาพเฟสสมมุติที่แสดงแผนผังในรูปต่อไปนี้:

จุด A, B, C, D และ E หมายถึงอะไร?
จุด A: จุดระเหิด
จุด B: จุดสามจุด
จุด C: จุดหลอมเหลว/จุดแข็งตัว
จุด D: จุดกลายเป็นไอ/จุดควบแน่น
จุด E: จุดวิกฤต
3) UECE - 2009
ดูแผนภาพเฟส PT ที่แสดงด้านล่าง สรุปได้ถูกต้องว่าสารที่ผ่านกระบวนการระเหิดนั้นเป็นไปตามวิถี:

ก) X หรือ Y
b) Y หรือ U
c) U หรือ V
ง) T หรือ X
ทางเลือก b: Y หรือ U


