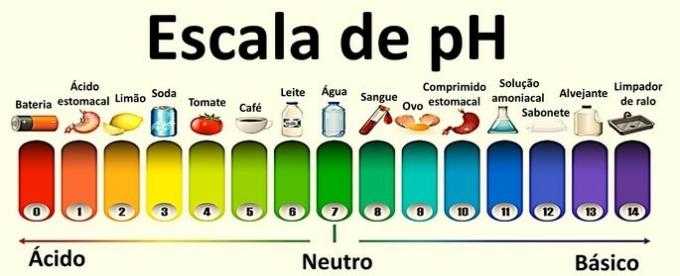
pH แสดงถึงศักย์ของไฮโดรเจนไอออนิก และ pOH คือศักย์ไฮดรอกซีไอออนิกของสารละลาย
เหล่านี้เป็นมาตราส่วนลอการิทึมที่ใช้ในการวัดลักษณะที่เป็นกรดและพื้นฐานของตัวอย่าง
ค่าที่ประกอบขึ้นจาก 0 ถึง 14 และได้รับจากสมดุลไอออนิกของน้ำ
สารละลายเป็นกลางมีค่า pH 7 ค่าที่ต่ำกว่า 7 จำแนกสารละลายเป็นกรด ในขณะที่หลังจาก 7 สารละลายจะเป็นพื้นฐาน
ด้วยค่า pH คุณสามารถค้นหาค่าที่สอดคล้องกันในระดับ pOH เพียงแค่ทำการลบ
สมดุลน้ำอิออน
โมเลกุลของน้ำมีความสามารถในการแตกตัวเป็นไอออนตามสมการ:
เรามีความสมดุลของไอออนิก เนื่องจากกระบวนการนี้สามารถย้อนกลับได้ และไอออนยังสามารถมารวมกันและก่อตัวเป็นโมเลกุลของน้ำได้อีกครั้ง
อีกวิธีในการแสดงให้เห็นถึงความสมดุลที่เกิดขึ้นคือผ่าน through การทำให้เป็นอัตโนมัติ.
โมเลกุลของน้ำสร้างไฮโดรเนียมไอออน (H3อู๋+) และไฮดรอกซิล (OH-) ผ่านการหยุดชะงักของโมเลกุลที่สอง
ผลิตภัณฑ์ไอออนิกของน้ำ (Kw)
ค่าคงตัวสำหรับสมดุลไอออนิกของน้ำคือ:
เนื่องจากน้ำเป็นของเหลวบริสุทธิ์ ความเข้มข้นของมันคือ 1 และไม่รบกวนค่าคงที่ ดังนั้นนิพจน์จะกลายเป็น:
อู๋ ผลิตภัณฑ์ไอออนิกของ น้ำ é .
นิพจน์นี้ได้รับสัญลักษณ์ Kw (W มาจากภาษาอังกฤษว่า น้ำ - น้ำ) และเช่นเดียวกับค่าคงที่สมดุล มันแปรผันตามอุณหภูมิ

การหาค่า pH และ pOH
ที่อุณหภูมิ 25 องศาเซลเซียส ผลิตภัณฑ์ไอออนิกของน้ำคือ:
ในการแตกตัวเป็นไอออนของน้ำบริสุทธิ์ H. 1 โมล3อู๋+ เกิดขึ้นจาก OH. 1 โมล- .
ในไม่ช้า
เนื่องจากค่าเหล่านี้ต่ำมาก จึงตัดสินใจใช้ค่าของโคโลการิทึม ซึ่งสอดคล้องกับลอการิทึมที่มีเครื่องหมายสลับกัน
การใช้โคโลการิทึมกับผลิตภัณฑ์ไอออนิกของน้ำ เราต้อง:
เราสามารถสังเกตได้ว่า: ถ้าเรารู้ค่า pH ของสารละลาย สามารถหาค่า pOH ได้โดยการลบค่าแรกออกจาก 14
ความเป็นกรดและความเป็นด่างของสารละลาย
สารละลายเป็นกลาง: ความเข้มข้นของไฮโดรเนียมไอออนเท่ากับไฮดรอกซิล
| [ห้3อู๋+] = 1,0. 10-7 นางสาว | pH = 7 |
| [โอ้-] = 1,0. 10-7 นางสาว | pOH = 7 |
ตัวอย่าง: น้ำบริสุทธิ์
สารละลายกรด: ความเข้มข้นของไฮโดรเนียมไอออนมากกว่าไฮดรอกซิล
| [ห้3อู๋+] |
pH |
| [โอ้-] |
pOH |
ตัวอย่าง: โซดา มะนาว และมะเขือเทศ
สารละลายพื้นฐาน: ความเข้มข้นของไฮดรอกซิลมากกว่าความเข้มข้นของไฮโดรเนียมไอออน
| [ห้3อู๋+] |
pH |
| [โอ้-] |
pOH |
ตัวอย่าง: ไข่ สบู่ และสารฟอกขาว
การคำนวณค่า pH
แนวคิดของศักยภาพไฮโดรเจนถูกสร้างขึ้นโดยนักเคมีชาวเดนมาร์ก Peter Lauritz Sorensen (1868-1939) เพื่อแสดงความเป็นกรดของสารละลายผ่านความเข้มข้นของ H+.
ดูตารางด้านล่างที่แสดงการแตกตัวเป็นไอออนของa กรด:
| โมลาริตีเบื้องต้น | 0,020 | 0 | 0 |
| ไอออไนซ์ | 0,001 | 0,001 | 0,001 |
| โมลาริตีสมดุล | 0,019 | 0,001 | 0,001 |
ในตัวอย่างจะมีความเข้มข้นของไอออน H+ é 0,001. ดังนั้น pH ของสารละลายคือ:
[ห้+] = 0,001 = 10-3
pH = - บันทึก 10-3 = 3
เนื่องจาก pH ของสารละลายน้อยกว่า 7 สารละลายนี้จึงมีสภาพเป็นกรด
สรุปเกี่ยวกับ pH และ pOH
| คำจำกัดความ | pH: ศักยภาพของไฮโดรเจนไอออนิกของสารละลาย | |
|---|---|---|
| pOH: ศักยภาพของไฮดรอกซิไลโอนิกของสารละลาย | ||
| สูตรทั่วไป | pH + pOH = 14 | |
| โซลูชั่น | เป็นกลาง | pH = pOH = 7 |
| กรด |
pH pOH > 7 |
|
| พื้นฐาน |
pOH pH > 7 |
|
| การคำนวณค่า pH | pH = - บันทึก [H+] | |
| การคำนวณ pOH | pOH = -log[OH-] |
แบบฝึกหัดเกี่ยวกับ pH และ pOH
1. (FMTM) ค่า pH ของน้ำย่อยซึ่งเป็นสารละลายของกรดไฮโดรคลอริก (HCℓ) อยู่ที่ประมาณ 2 ดังนั้นมวลเป็นกรัมของHCℓที่มีอยู่ในน้ำย่อยแต่ละลิตรคือ
ข้อมูล: มวลโมลาร์ (g/mol) H = 1, Cℓ = 35.5
ก) 7.3 · 10-2
ข) 3.65 · 10-1
ค) 10-2
ง) 2
จ) 10
ทางเลือกที่ถูกต้อง: b) 3.65 · 10-1.
ขั้นตอนที่ 1 คำนวณความเข้มข้นของไอออน H+.
ขั้นตอนที่ 2: คำนวณมวลโมลาร์ของ HCl
ขั้นตอนที่ 3: คำนวณมวลของกรดไฮโดรคลอริกในน้ำย่อยแต่ละลิตร
2. (UEMG) ผลิตภัณฑ์ทำความสะอาดหลายชนิดมีแอมโมเนียอยู่ในตัว ฉลากของผลิตภัณฑ์เหล่านี้ระบุค่า pH = 11 ซึ่งหมายความว่าความเข้มข้นของไฮดรอกโซเนียมไพเพอร์และไฮดรอกซิลแอนไอออนในผลิตภัณฑ์นี้ตามลำดับ:
ถึง 1 10-3 และ 1 10-11
ข) 1. 10-11 และ 1 10-7
ค) 1. 10-11 และ 1 10-3
ง) 1. 10-11 และ 1 10-11
ทางเลือกที่ถูกต้อง: c) 1. 10-11 และ 1 10-3.
ก) ผิด ความเข้มข้นเหล่านี้สอดคล้องกับสารละลาย pH = 3
ข) ผิด แม้ว่าความเข้มข้นของ H+ แสดงว่า pH ของสารละลายเท่ากับ 11 ความเข้มข้นของ OH ไอออน- ผิดตามที่ควรจะเป็น 3 เนื่องจาก: pOH = 14 - pH
ค) ถูกต้อง pH = 11 และ pOH = 3 เนื่องจาก pH + pOH = 14
ง) ผิด แม้ว่าความเข้มข้นของ H+ แสดงว่า pH ของสารละลายเท่ากับ 11 ความเข้มข้นของ OH ไอออน- ผิดตามที่ควรจะเป็น 3 เนื่องจาก: pOH = 14 - pH
ก) 0.1 โมล/ลิตร NaOH
ข) NaCl 0.5 โมล/ลิตร
ค) H2เท่านั้น4 1.0 โมล/ลิตร
ง) 1.0 โมล/ลิตร HCl
จ) 0.2 โมล/ลิตร KOH
ทางเลือกที่ถูกต้อง: จ) KOH 0.2 โมล/ลิตร
ก) ผิด สารละลายเป็นเบสพื้นฐานเนื่องจาก pH มากกว่า 7 แต่ไม่มี pH ที่สูงกว่าของทางเลือกอื่น
ข) ผิด NaCl เป็นเกลือเนื่องจากเป็นผลจากปฏิกิริยากรดและด่างอย่างแรง ดังนั้น pH ของมันจึงเป็นกลาง
ค) ผิด กรดซัลฟิวริกเป็นกรดแก่ ดังนั้น pH ของกรดจึงต่ำ
ง) ผิด กรดไฮโดรคลอริกเป็นกรดแก่ ดังนั้น pH ของกรดจึงต่ำ
จ) ถูกต้อง สารละลายเป็นเบสพื้นฐานเนื่องจาก pH มากกว่า 7