ไอโซเมอริซึม เป็นปรากฏการณ์ทางธรรมชาติที่สารต่างๆ (ในแง่ของคุณสมบัติทางเคมีและกายภาพ) มีสูตรโมเลกุลเหมือนกันทุกประการ ดังตัวอย่างต่อไปนี้
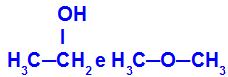
สารต่าง ๆ ที่มีสูตรโมเลกุลเหมือนกัน
เอทานอล (ซ้าย) มีสูตรโมเลกุล C2โฮ6O ซึ่งเกิดขึ้นกับเมทอกซีอีเทนด้วย (ขวา) ดังนั้นจึงเป็นไอโซเมอร์
ประเภทของไอโซเมอริซึม
→ ไอโซเมอร์แบน
เป็นประเภทของไอโซเมอร์ที่ศึกษาความแตกต่างเชิงโครงสร้างระหว่างไอโซเมอร์
ก) อาชีพ
เป็นประเภทของไอโซเมอร์แบบแบนซึ่งความแตกต่างระหว่างสารขึ้นอยู่กับความแตกต่างระหว่างหน้าที่ของสารอินทรีย์ที่มีอยู่ ดูตัวอย่างบางส่วน:
โพรพาโนนและโพรเพน:
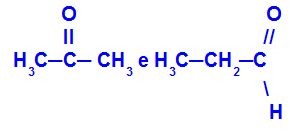
ไอโซเมอร์ที่อยู่ในหน้าที่ต่างกัน
โพรพาโนน (ซ้าย) อยู่ในกลุ่มคีโตน และโพรพานัล (ขวา) อยู่ในกลุ่มอัลดีไฮด์
ข) คุก
เป็นประเภทของไอโซเมอร์แบบแบนซึ่งความแตกต่างระหว่างสารขึ้นอยู่กับความแตกต่างระหว่างสายโซ่ที่มีอยู่ ดูตัวอย่าง:
2-เมทิล-โพรเพนและบิวเทน
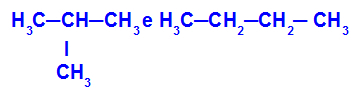
ไอโซเมอร์ที่มีสายโซ่ที่มีการจำแนกประเภทต่างกัน
ในตัวอย่าง เราจะเห็นว่า 2-เมทิล-โพรเพน (ด้านซ้าย) มีสายโซ่แยก และบิวเทน (ด้านขวา) มีสายโซ่ปกติ
ค) ตำแหน่ง
เป็นประเภทของไอโซเมอร์แบบแบนซึ่งความแตกต่างระหว่างสารขึ้นอยู่กับความแตกต่างในตำแหน่งของส่วนประกอบที่มีอยู่ในโซ่ ดูตัวอย่าง:
1-คลอโรโพรเพนและ 2-คลอโรโพรเพน
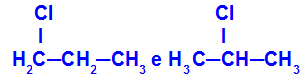
ไอโซเมอร์ที่มีส่วนประกอบอยู่ที่ตำแหน่งต่างๆ ในโซ่
ในตัวอย่าง เราจะเห็นว่า 1-คลอโร-โพรเพน (ด้านซ้าย) มีคลอรีนอยู่ที่คาร์บอน 1 และ 2-คลอโร-โพรเพน (ด้านขวา) มีคลอรีนอยู่ที่คาร์บอน 2
ง) Metameria หรือการชดเชย
บันทึก: Isomerism ใช้ได้เฉพาะกับสตริงที่ต่างกัน
เป็นประเภทของไอโซเมอร์แบบแบนซึ่งความแตกต่างระหว่างสารขึ้นอยู่กับความแตกต่างในตำแหน่งของเฮเทอโรอะตอมที่อยู่ในสายโซ่ ดูตัวอย่าง:
ตัวอย่าง: เมทอกซีโพรเพนและอีทอกซีอีเทน
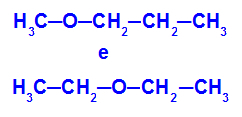
ไอโซเมอร์ที่มีเฮเทอโรอะตอมที่ตำแหน่งต่างๆ ในสายโซ่
ในตัวอย่าง เราจะเห็นได้ว่าในเมทอกซีโพรเพน (ซ้าย) ออกซิเจนมีอนุมูลที่มีคาร์บอนหนึ่งด้านและอีกสามคาร์บอนอยู่อีกด้านหนึ่ง ในเอทอกซีอีเทน (ขวา) ออกซิเจนมีอนุมูลที่มีคาร์บอน 2 ตัวอยู่ด้านหนึ่งและอีก 2 คาร์บอนอยู่อีกด้านหนึ่ง
และ)เทาโทเมอรี
เป็นกรณีเฉพาะของไอโซเมอร์ของฟังก์ชันระนาบและเกิดขึ้นในฟังก์ชันอินทรีย์เพียงสามฟังก์ชันเท่านั้น:
อัลดีไฮด์
คีโตน
Enol
isomerism ประเภทนี้ทำงานบนความจริงที่ว่ามีความสมดุลทางเคมีระหว่าง enol กับ aldehyde และระหว่าง enol และ ketone นั่นคือส่วนประกอบเหล่านี้จะถูกแปลงเป็นกันและกันอย่างต่อเนื่อง ดูตัวอย่าง:
Prop-2-en-1-ol และโพรพาโนน
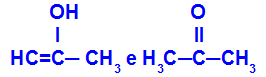
ไอโซเมอร์ที่อยู่ในหน้าที่ต่างกัน
ในตัวอย่าง เราจะเห็นว่า Prop-2-en-1-ol (ทางด้านซ้าย) อยู่ในกลุ่มของ enols และโพรพาโนน (ทางด้านขวา) อยู่ในกลุ่มของคีโตน ดังนั้นพวกมันจึงเป็นไอโซเมอร์ของเทาโทเมอรี
→ อวกาศ Isomerism
เป็นประเภทของ isomerism ที่กำหนดโดยการวิเคราะห์เชิงพื้นที่ของโมเลกุล
ก) ไอโซเมอร์เรขาคณิต
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
เป็นประเภทของไอโซเมอร์เชิงพื้นที่ที่เกิดขึ้นเมื่อสารมีโมเลกุลที่มีลักษณะดังต่อไปนี้:
โซ่ปิดที่มีคาร์บอนสองตัวที่มีลิแกนด์ต่างกันสองตัว ดังตัวอย่างด้านล่าง:

โครงสร้างปิดด้วยไอโซเมอร์เชิงเรขาคณิต
สายโซ่เปิดที่มีพันธะคู่ระหว่างคาร์บอน และในแต่ละคาร์บอนของพันธะคู่ มีลิแกนด์ที่แตกต่างกันสองตัว ดังในตัวอย่างด้านล่าง:
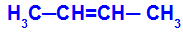
โครงสร้างแบบเปิดที่มีไอโซเมอร์เชิงเรขาคณิต
เรขาคณิต isomerism แบ่งออกเป็นสองกลุ่ม:
1โอ กลุ่ม: cis-trans
มันเกิดขึ้นเมื่อลิแกนด์สองอันของคาร์บอนหนึ่งอันมีค่าเท่ากับสองลิแกนด์ของคาร์บอนอีกอันอย่างเคร่งครัด ไม่ว่าจะอยู่ในโครงสร้างเปิดหรือในโครงสร้างปิด
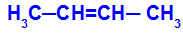
สายโซ่ของสารที่มีซิส-ทรานส์ไอโซเมอร์ริซึม
ไอโซเมอร์จะเรียกว่า cis เมื่อลิแกนด์เดียวกันอยู่ในระนาบเดียวกัน

ตัวอย่างของซิสไอโซเมอร์
ไอโซเมอร์จะเรียกว่าทรานส์เมื่อลิแกนด์ต่างกันอยู่ในระนาบเดียวกัน

ตัวอย่างของทรานส์ไอโซเมอร์
2โอ กลุ่ม: E-Z
มันเกิดขึ้นเมื่อลิแกนด์สองอันของคาร์บอนหนึ่งอันต่างกันเมื่อเทียบกับลิแกนด์สองอันของคาร์บอนอีกอัน ไม่ว่าจะในโครงสร้างเปิดหรือในโครงสร้างปิด

สายโซ่ของสารที่มี E-Z isomerism
ไอโซเมอร์จะเรียกว่า E เมื่อลิแกนด์ที่มีเลขอะตอมสูงสุดอยู่ในระนาบตรงข้าม ในตัวอย่างด้านล่าง คาร์บอนทางด้านซ้ายมี Br ที่มีเลขอะตอมสูงสุด (35) และอีกอันมีออกซิเจน (8)
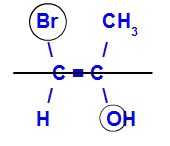
ตัวอย่างของ E-isomer
ไอโซเมอร์จะเรียกว่า Z เมื่อลิแกนด์ที่มีเลขอะตอมสูงสุดอยู่ในระนาบเดียวกัน ในตัวอย่างด้านล่าง คาร์บอนทางด้านซ้ายมี Br ที่มีเลขอะตอมสูงสุด (35) และอีกอันมีออกซิเจน (8)

ตัวอย่างของ Z-isomer
ข) ไอโซเมอร์ออปติคอล
เป็นประเภทของไอโซเมอร์เชิงพื้นที่ที่เกิดขึ้นเฉพาะเมื่อสารมีโมเลกุลด้วย ถ่านคาร์บอน (ซึ่งมีสี่แกนด์ที่แตกต่างกัน) ในโครงสร้าง โมเลกุลที่มี chiral carbon มีความสามารถในการโพลาไรซ์และหักเหแสงดังนี้:
ไปทางขวา (ไอโซเมอร์ขวามือ)
ไปทางซ้าย (ไอโซเมอร์ levorotatory)
สารประกอบที่มีกิจกรรมเกี่ยวกับการมองเห็นมักจะมี ไอโซเมอร์ที่ใช้งานอยู่ (เรียกว่าออปติคัลแอนติพอดส์) และไอโซเมอร์ที่ไม่ใช้งาน (ส่วนผสมระหว่างไอโซเมอร์ที่ออกฤทธิ์สองตัว ของผสมที่เรียกว่าราซิมิก)
เราสามารถใช้สูตรต่อไปนี้เพื่อกำหนดจำนวนไอโซเมอร์ที่ออกฤทธิ์ (IOA) และไอโซเมอร์ที่ไม่ใช้งาน (IOI) ของสารประกอบที่มีไครัลคาร์บอน:
IOA = 2ไม่
IOI = 2ไม่
2
ด้านล่างนี้เป็นตัวอย่างของสารประกอบที่มีไอโซเมอร์เชิงเรขาคณิต:
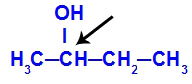
คาร์บอน Chiral มีอยู่ใน butan-2-ol
โครงสร้างของ butan-2-ol มีแกนด์ดังต่อไปนี้:
เมทิล (CH3)
เอทิล (CH3-CH2)
ไฮโดรเจน (H)
ไฮดรอกซิล (OH)
เนื่องจากมีคาร์บอน chiral เพียงตัวเดียว ดังนั้น butan-2-ol มี:
ไอโซเมอร์ที่ใช้งาน:
IOA = 21
IOA = 2
ไอโซเมอร์ที่ไม่ใช้งาน:
IOI = 21
2
IOI = 2
2
IOI = 1
By Me. Diogo Lopes Dias
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "ไอโซเมอริซึมคืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.


