คาร์บอเนตเป็นสารประกอบอนินทรีย์ที่เกิดจากพันธะไอออนิกของโลหะหรือกึ่งโลหะที่มีประจุลบคาร์บอเนต CO32-.
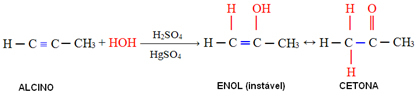
คาร์บอนเป็นเตตระวาเลนต์ กล่าวคือ มีอิเล็กตรอนสี่ตัวในเปลือกเวเลนซ์ และมันสามารถทำให้พันธะโควาเลนต์ทั้งสี่มีความเสถียร ในขณะที่ออกซิเจนเป็นไบวาเลนต์ มีอิเล็กตรอน 6 ตัวในเปลือกวาเลนซ์ และสามารถทำให้เกิดพันธะสองพันธะให้คงที่ได้ โดยมี 8 อิเล็กตรอน อิเล็กตรอน ดังนั้นจึงมีแนวโน้มสูงที่คาร์บอนจะจับกับออกซิเจนสองอะตอม ซึ่งทั้งหมดมีความเสถียร (O ═ C ═ โอ → CO2).
แต่ออกซิเจนอื่นๆ สามารถรวมตัวกับคาร์บอนได้ เนื่องจากอัตราส่วนของรัศมีไอออนทำให้เกิดจำนวนการประสานงานเท่ากับ 3 ทำให้เกิดโครงสร้าง รูปสามเหลี่ยมที่มีคาร์บอนอยู่ตรงกลาง ทำให้เกิดพันธะคู่กับอะตอมออกซิเจนตัวใดตัวหนึ่ง และพันธะเดี่ยวสองพันธะกับอีกสองตัวที่เหลือ ออกซิเจน ผลที่ได้คืออิเล็กตรอนเกินสองตัว เนื่องจากออกซิเจนสองตัวนี้ไม่เสถียร ต้องรับอิเล็กตรอนอย่างละตัว:
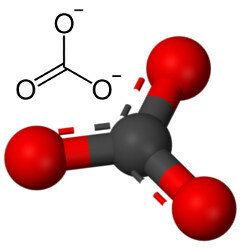
แอนไอออนของคาร์บอเนตนั้นเกิดจากพันธะโควาเลนต์ แต่สารประกอบของมันคือเกลืออนินทรีย์และแร่ธาตุ เรียกว่าคาร์บอเนตเป็นไอออนิกเนื่องจากอนุมูลนี้รับอิเล็กตรอนสองตัวจากโลหะหรือเซมิเมทัลบางส่วนก่อตัวเป็น พันธะไอออนิก
สารประกอบเหล่านี้ไม่ละลายในน้ำ ยกเว้นแอมโมเนียมคาร์บอเนต ((NH4)2CO3) และคาร์บอเนตที่เกิดขึ้นจากโลหะอัลคาไล (องค์ประกอบของตระกูล 1: Li, Na, K, Rb, Cs และ Fr) เกือบทั้งหมดเป็นของแข็งสีขาว ดังแสดงในภาพด้านล่าง:

ตัวอย่างที่พบบ่อยที่สุดและสำคัญที่สุดสองตัวอย่างในชีวิตประจำวันของคาร์บอเนตคือโซเดียมคาร์บอเนต (Na2CO3) และแคลเซียมคาร์บอเนต (CaCO3). ในกรณีแรก โซเดียมอยู่ในตระกูล 1 โดยมีอิเล็กตรอนอยู่ในเปลือกเวเลนซ์และมีแนวโน้มที่จะสูญเสียอิเล็กตรอนนี้เพื่อให้มีความเสถียร เนื่องจากคาร์บอเนตแอนไอออนต้องการรับอิเล็กตรอนสองตัว มันจึงจับกับโซเดียมสองอะตอม:
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)

โซดาแอชเป็นที่รู้จักกันดีในชื่อโซดาหรือโซดา ซึ่งใช้ในการผลิตสบู่ สีย้อม ยา กระดาษ และในการบำบัดน้ำในสระว่ายน้ำ แต่การใช้งานหลักคือการใช้แคลเซียมคาร์บอเนตและทรายในการผลิตแก้ว
แคลเซียมเป็นแฟมิลี 2 มีแนวโน้มที่จะสูญเสียอิเล็กตรอนสองตัว ดังนั้น อะตอมของแคลเซียมจึงจับกับคาร์บอเนตเรดิคัล:

แคลเซียมคาร์บอเนตมีอยู่ในหินปูนและหินอ่อน ที่ หินงอกหินย้อย ที่มีอยู่ในถ้ำประกอบด้วยคาร์บอเนตนี้ เปลือกหอย แนวปะการัง และเปลือกไข่ด้วย เมื่อเราล้างผนัง ลำต้นของต้นไม้ และสถานที่อื่นๆ เรากำลังใช้แคลเซียมไฮดรอกไซด์ (Ca(OH)2) ซึ่งเมื่อเวลาผ่านไปจะทำปฏิกิริยากับคาร์บอนไดออกไซด์ในบรรยากาศเพื่อสร้างแคลเซียมคาร์บอเนต

คาร์บอเนตมีอยู่ทั่วไปบนพื้นผิวโลก เช่นเดียวกับในกรณีของแร่ธาตุ ผลึกเรติคูลัมของมันสามารถจัดเรียงตัวเองใหม่ในอวกาศได้สองวิธี: ออร์โธฮอมบิก (เช่นเดียวกับแร่อะราโกไนต์ที่แสดงด้านบนพร้อมกับสูตรแคลเซียมคาร์บอเนต) และ รูปสี่เหลี่ยมขนมเปียกปูนหรือตรีโกณมิติ เช่นเดียวกับแคลไซต์ (แร่ธาตุอื่นที่ประกอบด้วยแคลเซียมคาร์บอเนต)
คาร์บอเนตทำปฏิกิริยาต่อหน้ากรด ปล่อยCO2ซึ่งมองเห็นได้ง่ายผ่านความฟุ่มเฟือย
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "คาร์บอเนต"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/carbonatos.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี

โซเดียมคาร์บอเนต วิธี Leblanc วิธี Ernest Solvay โซดาแอช โซดา การผลิตแก้วทั่วไป การบำบัดน้ำในสระว่ายน้ำ การควบคุม pH ของน้ำ การบำบัดสิ่งทอ สารเติมแต่งอาหาร
เคมี

เกลือในชีวิตประจำวัน แคลเซียมคาร์บอเนต โซเดียมคลอไรด์ โซเดียมฟลูออไรด์ โพแทสเซียมไนเตรต โซเดียมไนเตรต โซเดียม, โซเดียมคาร์บอเนต, โซเดียมไบคาร์บอเนต, โซเดียมไบคาร์บอเนต, โซเดียมซัลไฟต์, ดินประสิว, โซดา.