การศึกษาความเข้มแข็งของ กรด มีความสำคัญมากในการกำหนดความสามารถของสารละลายที่เป็นกรดในการนำกระแสไฟฟ้า เนื่องจากเกี่ยวข้องกับปริมาณไอออนที่สารนี้ผลิตเมื่อสัมผัสกับน้ำ (ไอออไนซ์). เมื่อกรดแรงเกินไป จะผลิตไฮโดรเนียมไอออนบวกมากเกินไป (H3โอ+) และแอนไอออนจำนวนมาก (X-). ดูสมการไอออไนซ์ของกรดไฮโดรโบรมิก:
HBr + H2O → H3โอ+ + บรา-
เมื่อแตกตัวเป็นไอออน ไฮโดรเจนที่มีอยู่ในโมเลกุลกรดจะทำปฏิกิริยากับโมเลกุลของน้ำและเกิดไฮโดรเนียม แต่สำหรับเหตุการณ์นี้ที่จะเกิดขึ้น อะตอมไฮโดรเจนจะต้องสามารถแตกตัวเป็นไอออนได้ ไฮโดรเจนที่แตกตัวเป็นไอออนคือสามารถสร้างไฮโดรเนียมไอออนบวกได้. ในการตรวจสอบว่าไฮโดรเจนสามารถแตกตัวเป็นไอออนได้หรือไม่ เราพิจารณาการจำแนกกรดเป็นไฮดราซิด (ไม่มีออกซิเจนในองค์ประกอบ) หรือออกซีกรด (มีออกซิเจนในองค์ประกอบ)
ก) ยาฆ่าแมลง
ไฮโดรเจนทั้งหมดในไฮดราซิดถือเป็นไอออนไนซ์ได้
ตัวอย่าง:
- HCl: ไฮโดรเจนที่แตกตัวเป็นไอออนได้ จึงผลิตไฮโดรเนียม
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
- โฮ2S: ไฮโดรเจนที่แตกตัวเป็นไอออนได้ 2 ตัว จากนั้นจึงผลิตไฮโดรเจน 2 ตัว
ข) Oxyacid
ในกรดออกซีกรด เฉพาะไฮโดรเจนที่ถูกผูกมัดกับอะตอมออกซิเจนในโมเลกุลเท่านั้นที่ถือว่าแตกตัวเป็นไอออนได้
สำหรับสิ่งนี้จำเป็นต้องสร้างสูตรโครงสร้าง ดูตัวอย่างบางส่วน:โฮ3ฝุ่น4 (กรดฟอสฟอริก)
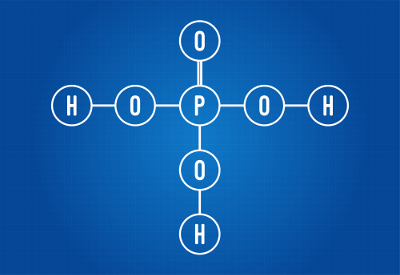
สูตรโครงสร้างของกรดฟอสฟอริก
เราจะเห็นได้ว่าในโครงสร้างของกรดฟอสฟอริก มีไฮโดรเจนสามตัวจับกับออกซิเจน จึงมีไฮโดรเจนที่แตกตัวเป็นไอออนได้สามตัว สมการไอออไนซ์จะเป็น:
โฮ3ฝุ่น4 + 3 ชั่วโมง2O → 3 ชั่วโมง3โอ+ + ป4-3
โฮ2เท่านั้น4 (กรดซัลฟูริก)
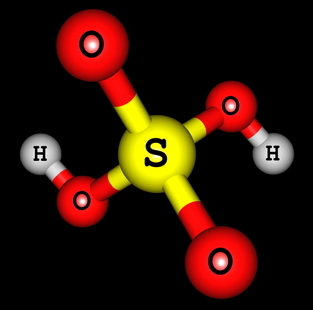
สูตรโครงสร้างของกรดซัลฟิวริก
เราจะเห็นได้ว่าในโครงสร้างของกรดซัลฟิวริก มีไฮโดรเจนอยู่สองตัวจับกับออกซิเจน จึงมีไฮโดรเจนที่แตกตัวเป็นไอออนได้สองตัว สมการไอออไนซ์จะเป็น:
โฮ2เท่านั้น4 + 2 ชั่วโมง2O → 2 H3โอ+ + OS4-2
By Me. ดิโอโก้ โลเปส ดิอาส
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "ไฮโดรเจนที่แตกตัวเป็นไอออน"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี

การแยกตัวและการแตกตัวเป็นไอออน, Volta นักวิทยาศาสตร์ชาวอิตาลี, กระแสไฟฟ้า, นักเคมีกายภาพชาวสวีเดน Svant August Arrhenius, ทฤษฎีของ อาร์เรเนียส, ไอออนบวก, ไพเพอร์, ไอออนลบ, แอนไอออน, โซดาไฟ, เกลือแกง, โมเลกุลมีขั้ว, การแยกตัวออกจากกัน อิออน,