ในข้อความ "ชื่อเรื่องหรือร้อยละมวล” เราเห็นวิธีการคำนวณอัตราส่วนระหว่างมวลของตัวถูกละลายกับมวลของสารละลายสำหรับสารละลายที่เป็นของแข็ง ของเหลว และก๊าซ อย่างไรก็ตาม ในข้อความนี้ เราจะเห็นว่ายังเป็นไปได้ที่จะคำนวณไทเทอร์ในแง่ของปริมาตร สำหรับสารละลายที่มีส่วนประกอบที่เป็นของเหลวหรือก๊าซ

ชื่อเรื่องในปริมาณสามารถคำนวณได้โดยนิพจน์:
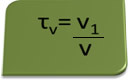
พิจารณาเป็นตัวอย่าง สารละลายเอทิลแอลกอฮอล์ที่ใช้เป็นน้ำยาฆ่าเชื้อและยาฆ่าเชื้อ ซึ่งก็คือ เตรียมโดยการเติมแอลกอฮอล์บริสุทธิ์ 70 มล. ลงในน้ำให้เพียงพอเพื่อให้ได้ปริมาตร 100 มล สารละลาย. ดังนั้นเราจึงมี:
τ = 70 มล. = 0,7
100มล.
เราสามารถแสดงชื่อเป็นเปอร์เซ็นต์ได้ เพียงแค่คูณผลลัพธ์ด้วย 100% ดังนั้น ในกรณีนี้ เรามีสารละลายเอทิลแอลกอฮอล์ 70% ซึ่งหมายความว่าจากทุกๆ 100 หน่วยปริมาตรของสารละลาย 70 หน่วยปริมาตรเป็นแอลกอฮอล์
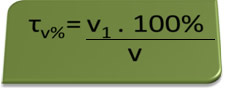
ในกรณีด้านล่าง เรามีสารละลายเอทิลแอลกอฮอล์ 70% ในปริมาตรสารละลาย 250 มล. ซึ่งหมายความว่า 175 มล. เป็นแอลกอฮอล์ตามการคำนวณ:
100 มล. แอลกอฮอล์ 70 มล.
250 มล. x
x = 70. 250
100
X = แอลกอฮอล์ 175 มล.

อย่างไรก็ตาม เราไม่สามารถพูดได้ว่าในกรณีนี้ เรามีน้ำ 75 มล. (250-175) ซึ่งแตกต่างจากการไทเทรตมวล ซึ่งเราสามารถเพิ่มมวลของตัวทำละลายให้กับมวลของตัวถูกละลายเพื่อค้นหามวลของสารละลาย ซึ่งไม่สามารถทำได้เมื่อเทียบกับไทเทอร์ของปริมาตร

อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
ซึ่งหมายความว่าปริมาตรของสารละลายไม่เท่ากับผลรวมของปริมาตรตัวทำละลายและปริมาตรของตัวถูกละลาย (แม้ว่าบ่อยครั้งจะถือว่าความแตกต่างนั้นเล็กน้อยก็ตาม) นี่เป็นเพราะแรงระหว่างโมเลกุลที่มีอยู่ในของเหลวเหล่านี้มีอิทธิพลต่อปริมาตรสุดท้าย
ในกรณีของสารละลายดังกล่าวของเอทิลแอลกอฮอล์ เช่น เมื่อเราผสมแอลกอฮอล์กับน้ำ จะเกิดการหดตัวของปริมาตรรวมของสารละลาย นั่นคือปริมาตรสุดท้ายจะน้อยกว่าถ้าเราเติมแอลกอฮอล์และน้ำเพียงอย่างเดียว เนื่องจากโมเลกุลแอลกอฮอล์สร้างพันธะหรือพันธะไฮโดรเจนกับโมเลกุลของน้ำ ทำให้ช่องว่างระหว่างพวกมันลดลง
ดังนั้น ในกรณีนี้และกรณีอื่นๆ ปริมาตรของสารละลายจะต้องถูกวัดโดยการทดลองเมื่อไม่ได้ระบุไว้ในแบบฝึกหัด
เปอร์เซ็นต์โดยปริมาตรใช้กันอย่างแพร่หลายในกรณีของเครื่องดื่มแอลกอฮอล์และแอลกอฮอล์เชิงพาณิชย์ตามที่กล่าวไว้ข้างต้น ดูการใช้งานที่สำคัญสองประการของการคำนวณนี้:
- เครื่องช่วยหายใจ: เครื่องวิเคราะห์ลมหายใจจะวัดความเข้มข้นของเอทิลแอลกอฮอล์ในเลือด และในบราซิล ห้ามมิให้ผู้ใดขับรถประเภทใดก็ตามที่มีปริมาณแอลกอฮอล์ในเลือดเท่ากับหรือสูงกว่า 0.1% ในปริมาตร บุคคลที่มีปริมาณแอลกอฮอล์นี้มีแอลกอฮอล์ 1 มล. สำหรับเลือดแต่ละลิตรดังที่แสดงโดยการคำนวณต่อไปนี้:
τวี%=วี1. 100%
วี
0,1 % = วี1. 100%
1L
วี1 = 0,1% → วี1 = 0.001 ลิตร = 1 มล.
100%

- ปริมาณเอทานอลในน้ำมันเบนซิน: ในบราซิล น้ำมันเบนซินถูกควบคุมโดยการเพิ่มเอทานอล แต่ปริมาณเอทานอลในน้ำมันเบนซินต้องไม่เกิน 24% โดยปริมาตรของแอลกอฮอล์ปราศจากน้ำ (เนื่องจากน้ำมันเบนซินต้องปราศจากน้ำ) ยิ่งเติมเอทานอลลงในน้ำมันเบนซินมาก สีของเชื้อเพลิงก็จะยิ่งจางลงและความหนาแน่นของน้ำมันก็จะมากขึ้น
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ชื่อปริมาณของสารละลายเคมี"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
เคมี

วิธีการทำงานของ Breathalyzer, ความเข้มข้นของแอลกอฮอล์, เครื่องวิเคราะห์ลมหายใจ, ปฏิกิริยาที่เกี่ยวข้องกับเอทิลแอลกอฮอล์, ประเภทของ เครื่องช่วยหายใจ, โพแทสเซียมไดโครเมต, เซลล์เชื้อเพลิง, ตัวเร่งปฏิกิริยา, การปล่อยอิเล็กตรอน, กรดอะซิติก, ไฮโดรเจน คอนเซ