เมื่อเราส่งองค์ประกอบต่างๆ ให้กับการกระทำของเปลวไฟ เราจะสังเกตเห็นว่าแต่ละองค์ประกอบปล่อยสีที่ต่างกันออกไป ตัวอย่างเช่น ถ้าเราเผาสตรอนเทียม โซเดียม และเกลือทองแดง เราจะเห็นสีแดง เหลืองเข้ม และเขียวตามลำดับ ดังแสดงในรูปต่อไปนี้:

ถ้าแสงจากเปลวไฟเหล่านี้ตกกระทบปริซึม a สเปกตรัมไม่ต่อเนื่องกล่าวคือจะสังเกตเห็นเส้นสีสว่างเพียงไม่กี่เส้นเท่านั้นที่กระจายไปทั่วบริเวณที่ไม่มีแสง สำหรับแต่ละองค์ประกอบเราจะมีสเปกตรัมที่แตกต่างกัน

สเปกตรัมประเภทนี้เรียกว่า สเปกตรัมการแผ่รังสีเนื่องจากออกโดยองค์ประกอบบางอย่างและใช้เพื่อระบุ
เป็นไปได้ที่จะได้สเปกตรัมในลักษณะนี้โดยใช้ลำแสงที่ผลิตในท่อปล่อยไฟฟ้าที่ระดับสูง อุณหภูมิและความดันต่ำ ซึ่งประกอบด้วยก๊าซจากธาตุบางชนิด เช่น ไฮโดรเจน หรือก๊าซมีตระกูล ร้อง:

โดยการส่งผ่านรังสีแม่เหล็กไฟฟ้า (แสง) ที่ผลิตผ่านปริซึม จะได้สเปกตรัมการแผ่รังสีของแต่ละองค์ประกอบเหล่านี้
ก่อนหน้านี้ คิดว่าสเปกตรัมแสงอาทิตย์ที่บรรลุได้นั้นต่อเนื่องโดยสิ้นเชิง แต่นักวิทยาศาสตร์ชาวอังกฤษ วิลเลียม ไฮด์ วอลลาสตัน พบว่าโดย การทำงานกับลำแสงที่แคบมาก มีร่องประมาณ 0.01 มม. คุณจะเห็นว่าสเปกตรัมของดวงอาทิตย์มีเส้นสีดำอยู่เจ็ดเส้น เกี่ยวกับมัน. ต่อมา หนุ่มๆ
โจเซฟ ฟรอนโฮเฟอร์ (พ.ศ. 2330-1826) โดยใช้ปริซึมและตะแกรงเลี้ยวเบน พบว่าสเปกตรัมของดวงอาทิตย์มีเส้นสีดำทับอยู่หลายพันเส้นหลังจากนั้นไม่นานร่างกาย the กุสตาฟ โรเบิร์ต เคิร์ชฮอฟฟ์ เขาสังเกตเห็นว่าจุดสีเหลืองที่เกิดจากสเปกตรัมโซเดียมนั้นอยู่ในตำแหน่งเดียวกับเส้นสีดำสองเส้นในสเปกตรัมของดวงอาทิตย์ เขาและนักเคมี โรเบิร์ต วิลเฮล์ม บุนเซ่น ทำการทดลองหลายครั้งและสังเกตว่าถ้าแสงสีขาวจากเตา Bunsen เช่นแสงแดดส่องผ่านแสงสีเหลืองที่ปล่อยออกมาจากโซเดียมและปริซึมถูกข้ามเพื่อสร้างสเปกตรัม ผลที่ได้จะเป็นสเปกตรัมสุริยะต่อเนื่องในสีรุ้ง แต่มีเส้นสีดำ (เรียกว่าเส้น D โดย Fraunhofer) ในตำแหน่งเดียวกับเส้นสีเหลืองในสเปกตรัมโซเดียม
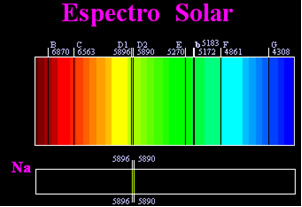
ดวงอาทิตย์เปล่งแสงทุกสี ตั้งแต่สีแดงไปจนถึงสีม่วง อย่างไรก็ตาม เมื่อผ่านชั้นบรรยากาศของโลก ก๊าซที่มีอยู่จะดูดซับแสงของดวงอาทิตย์ตามสีที่ปล่อยออกมา
สเปกตรัมประเภทนี้เรียกว่า สเปกตรัมการดูดซึม absorption.
จากข้อสังเกตเหล่านี้ เคิร์ชอฟฟ์ สร้างสาม กฎหมาย สเปกโตรสโคปี ได้แก่
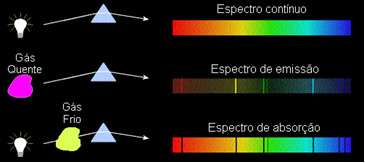
1) ร่างกาย ทึบแสง ร้อนในสถานะทางกายภาพสามอย่างใด ๆ ปล่อยคลื่นความถี่ ต่อเนื่อง.
2) แก๊ส โปร่งใส – เหมือนกับก๊าซมีตระกูลที่เราเห็นด้านบน – ทำให้เกิด a สเปกตรัมการแผ่รังสีด้วยรูปลักษณ์ของ with เส้น สดใส จำนวนและตำแหน่งของเส้นเหล่านี้จะถูกกำหนดโดยองค์ประกอบทางเคมีที่มีอยู่ในก๊าซ
3) ถ้า สเปกตรัมต่อเนื่องผ่านแก๊ส ที่อุณหภูมิต่ำสุด ก๊าซเย็นทำให้เกิด เส้นดำ, นั่นคือ, a สเปกตรัมการดูดซึม. นี่คือสิ่งที่เกิดขึ้นกับสเปกตรัมของแสงอาทิตย์ที่ส่องผ่านก๊าซโซเดียม ในกรณีนี้ จำนวนและตำแหน่งของเส้นในสเปกตรัมการดูดกลืนจะขึ้นอยู่กับองค์ประกอบทางเคมีที่มีอยู่ในก๊าซด้วย
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm

