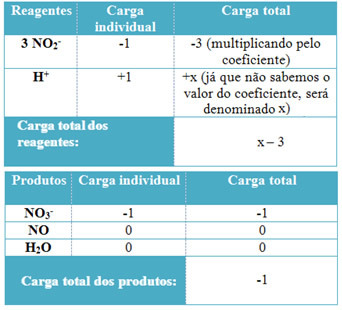
Једно реверзибилна реакција јавља се када је могуће производе претворити назад у реактанте. Оваква реакција долази хемијска равнотежа када је брзина развоја директне реакције, односно реакције са потрошњом реагенса и формирањем производи се дешавају истом брзином као и обрнута реакција - стварање реактаната и потрошња производа.
Ове врсте уравнотежених реакција се често виде у свакодневном животу. Пример је шта се дешава у пећинама, при формирању такозваних сталактита и сталагмита.
Подземне воде су под великим притиском, па садрже велике количине угљен-диоксида (ЦО2 (г)) растворен у њему. При проласку кроз тла која садрже кречњак (ЦаЦО3 (с)), овај карбонат се раствара и настају пећине, према доњој реакцији:
ЦаЦО3 (с) + ЦО2 (г) + Х2О.(1) → Ца2+(овде) + 2 ХЦО-3 (ак)
Међутим, јони карбоната и калцијума могу да реагују, поново се таложећи као калцијум-карбонат. То показује реакција:
Ево2+(овде) + 2 ХЦО-3 (ак)→ ЦаЦО3 (с) + ЦО2 (г) + Х2О.(1)
Не заустављај се сада... После оглашавања има још;)
Као што сте можда приметили, једна реакција је управо супротна другој: реактанти постају производи, а производи реактанти. Дакле, ову реакцију можемо представити у равнотежи на следећи начин:
ЦаЦО3 (с) + ЦО2 (ак) + Х2О.(1) Ево2+(овде) + 2 ХЦО-3 (ак)
Ево2+(овде) + 2 ХЦО-3 (ак)
Полако и континуирано одлагање карбоната из минерализованих капљица са крова пећина се спушта, вода им испарава и долази до ослобађања ЦО2. Тако да се хемијска равнотежа помера у супротном смеру (формирања реактаната), отуда и ЦаЦО3 (с) се формира, односно сталактити на крову пећина. При паду, кап је и даље растворио карбонат, који се таложи на дну пећине, формирајући сталагмити.
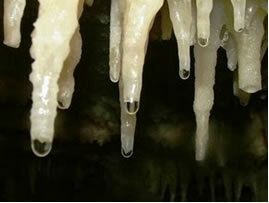
Вода са кречњаком који капље за стварање сталактита и сталагмита
Јеннифер Фогаца
Дипломирао хемију
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ФОГАЊА, Јеннифер Роцха Варгас. „Хемијска равнотежа у пећинама“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/equilibrio-quimico-nas-cavernas.htm. Приступљено 28. јуна 2021.