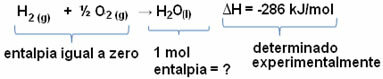
Хемијска једначина се подразумева као опис хемијских процеса, у којима су приказани реактанти и производи који учествују у реакцији:
Ц + О2→ ЦО2
Реагенси за производе
Да би дошло до хемијске везе, мора доћи до прекида постојећих веза у реактантима и стварања нових веза у производима. Овај процес укључује проучавање енергетских варијација реакција.
Снабдевање енергијом омогућава прекид везивања реактаната (ендотермни процес), док је стварање веза у производу егзотермичан процес јер се енергија ослобађа.
Енергија везивања је она која се ослобађа при формирању производа и нумерички је једнака енергији апсорбованој при прекиду ове везе, па је енергија везивања дефинисана за прекидање веза.
Укратко: Енергија везе је енергија апсорбована прекидом 1 мола веза, у гасовитом стању, на 25 ° Ц и 1 атм.
Погледајте сада пример како добити енергију везивања реакција:
ХЦл (г) → Х (г) + Цл (г) ∆Х = + 103,0 Кцал / мол
Не заустављај се сада... После оглашавања има још;)
Горња једначина показује да за прекидање веза у 1 молу молекула ХЦл (г) и формирању 1 мола ХЦл атома Потребно је Х (г) и 1 мол атома Цл (г), 103,0 Кцал, односно енергија везивања ХЦл (г) = + 103,0 Кцал / мол.
Стабилност везе: што је већа енергија везе, то је веза стабилнија. Пример:
Ако су дате следеће енергије везивања:
Х.2О (1) → Х.2 (г) + О (г) ∆Х = + 110,6 Кцал / мол
ХБр (г) → Х (г) + Бр (г) ∆Х = + 88,0 Кцал / мол
Која би била најстабилнија веза, она присутна у ХБр или у Х.2О?
Енергија везивања воде (Х.2О) има већу вредност од ХБр, па има већу стабилност.
Написала Лириа Алвес
Дипломирао хемију
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
СОУЗА, Лириа Алвес де. „Енергија везивања у хемијским једначинама“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/energia-ligacao-equacoes-quimicas.htm. Приступљено 28. јуна 2021.