Základňa je anorganická látka ktorú podľa švédskeho chemika Svante Arrheniuskeď je vo vode, trpí fenoménom iónová disociácia, v ktorom je vydanie ióny: katión (Y+) a hydroxidový anión (OH.)-).

Všeobecný vzorec Arrheniovej bázy
skupina Y a základňa môže to byť akýkoľvek kov alebo aj amónna skupina (NH4+), ktoré sa uvoľňujú vo vode ako katióny počas disociácie, ako je zrejmé z rovnice, ktorá predstavuje proces:
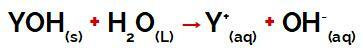
Rovnica predstavujúca disociáciu bázy
Ďalej uvádzame niektoré veľmi dôležité informácie týkajúce sa klasifikácie a nomenklatúry základne.
1) Klasifikácia týkajúce sa rozpustnosť zásad(schopnosť rozpustiť vo vode)
Bázy rozpustný: majú v kompozícii alkalický kov alebo amoniak;
Bázy ťažko rozpustný: mať kov alkalických zemín v zložení. Príklad: hydroxid horečnatý, široko používaný ako antacidum a preháňadlo;
základy prakticky nerozpustný: mať v zložení akýkoľvek iný kov. Príklad: hydroxid hlinitý, široko používaný ako antacidum.
2) Klasifikácia týkajúce sa základná sila(schopnosť disociovať vo vode)
Bázy silný: majú v zložení alkalické kovy alebo kovy alkalických zemín, s výnimkou horčíka;
Bázy slabý: mať v zložení akýkoľvek iný kov.
3) Základná nomenklatúra
Ak chcete pomenovať základňu, postupujte podľa pravidla pomenovania uvedeného nižšie:
Hydroxid + de + názov kovu alebo amónia
Príklad: Ca (OH)2 → hydroxid vápenatý
Ak má báza chemický prvok, ktorý nepatrí do čeľade IA, IIA alebo IIIA (a to nie je striebro alebo zinok), musíme pred menom prvku uviesť rímskymi číslicami, počet hydroxylové skupiny:
Príklad: Ti (OH)4 → hydroxid titaničitý IV
Podľa mňa. Diogo Lopes
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-base.htm
