Uvidíme v tomto texte ako a tabuľka zmena fyzikálneho stavu k hocijakej čistá substancia, ako interpretovať tento typ diagramu a ako je znázornený graf zmesí.
Za týmto účelom zvážme príklad vody. Predstavte si, že vezmeme pohár ľadu pri teplote –10 ° C a začneme proces ohrievania pod tlakom 1 atm. Keď teplota stúpa z -10 ° C na -9 ° C do -8 ° C atď., Ľad zostane v pevnom stave, kým nedosiahne teplotu 0 ° C.
V tomto okamihu sa začne meniť na tekuté skupenstvo, to znamená, že začne prebiehať fúzia. Teplota sa nebude ďalej zvyšovať ako predtým, ale zostane konštantná na 0 ° C, kým sa všetok ľad neroztopí:

Po roztopení celej tuhej látky sa teplota systému bude naďalej zvyšovať až do dosiahnutia teploty 100 ° C. Pri tejto teplote sa voda, ktorá bola v kvapalnom skupenstve, začne meniť na parné, to znamená, že bude vrieť.
Rovnako ako sa to stalo v fúzny bod, pri teplote varu tiež nebude konštantná, kým sa všetka kvapalina nezmení na paru. Potom, ak budeme systém neustále zahrievať, bude teplota naďalej stúpať:
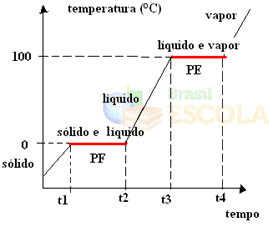
Pripravený! Toto je graf alebo diagram, ktorý predstavuje zmenu fyzikálneho stavu vody alebo jej vykurovacej krivky. Keby to bol inverzný proces, mali by sme nasledujúcu krivku vodného ochladenia:
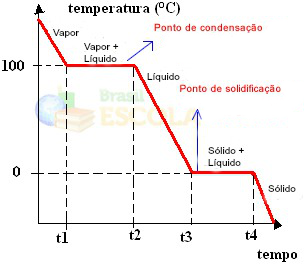
Veľmi dôležitým aspektom týchto grafov je, že sú tvorené dvoma úrovňami, to znamená, že existujú dva body, kde teplota na chvíľu zostáva konštantná. K tomu vždy dochádza pri zmene stavu čistej látky. Rozdiel je iba v hodnotách topenia a varu.
Napríklad kyslík nie je na rozdiel od vody kvapalina, ale plyn pri izbovej teplote (asi 20 ° C). Je to preto, lebo jeho teplota topenia na úrovni mora je -223,0 ° C a jeho teplota varu je -183,0 ° C. Pozrite si graf zmien fyzického stavu:

Spoločná kombinácia grafiky
Ak zmes zahrievame alebo ochladzujeme, teplota topenia a teplota varu nebudú mať určené a konštantné hodnoty, to znamená, že sa nevytvoria dve úrovne pozorované v grafoch vyššie.
Zmeny fyzikálnych stavov nastanú skôr v teplotných rozsahoch ako v pevnom množstve. Napríklad teplota topenia začína pri danej teplote a končí pri inej teplote a to isté sa stane s teplotou varu, ako je znázornené v nasledujúcom grafe:
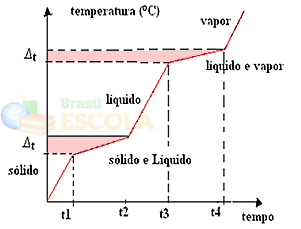
Dve výnimky sú eutektické a azeotropické zmesi. Zistite, čo sa s nimi stane:
a) Eutektická zmes
Eutektická zmes sa počas fúzie správa, akoby išlo o čistú látku, to znamená, že v tom okamihu zostáva teplota konštantná od začiatku do konca zmeny stavu agregácie.

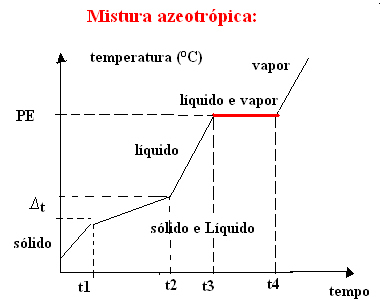
b) azeotropická zmes
Azeotropická zmes sa počas varu správa ako čistá látka, to znamená, že v tomto okamihu zostáva teplota konštantná od začiatku do konca zmeny stavu agregácie.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm

