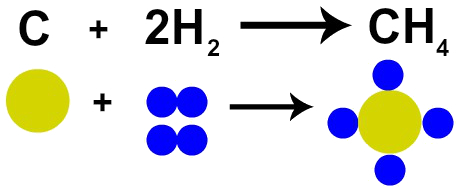
Teória hybridizácie sa ukázala ako doplnok k Teória oktetu, ktorá dokázala vysvetliť štruktúru väčšieho počtu molekúl vrátane molekúl tvorených bórom (B).
Tento prvok má päť základných elektrónov s nasledujúcou elektronickou konfiguráciou:
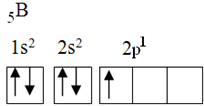
Podľa teórie oktetu mohol bór vytvoriť iba jednu kovalentnú väzbu, pretože má iba jednu neúplnú atómovú obežnú dráhu. Experimentálne je však potrebné poznamenať, že tento prvok vytvára zlúčeniny, v ktorých vykonáva viac ako jednu väzbu.
Príkladom je fluorid boritý (BF3). Ako je uvedené nižšie, bór vytvára tri kovalentné väzby s fluórom a delí sa o tri páry elektróny a so šiestimi elektrónmi v poslednom plášti (valenčná vrstva), to znamená výnimku z pravidla oktet.
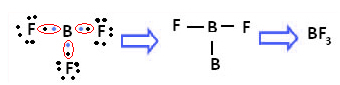
Vysvetľuje to hybridizačný jav, ktorý sa vyskytuje s bórom. Ukázalo sa, že elektrón z podúrovne 2s absorbuje energiu a prechádza do excitovaného stavu, v ktorom skočí na prázdnu obežnú dráhu podúrovne 2p. Tak vzniknú tri neúplné orbitaly, ktoré môžu teraz vytvárať tri kovalentné väzby:
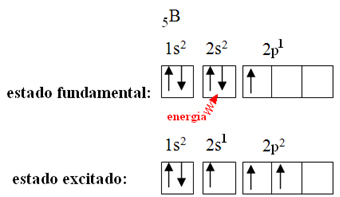
Väzby vytvorené v fluoride boritom sú však všetky rovnaké, ale ak sa pozrieme vyššie, existujú dve väzby rôzne, pretože jeden z nich by bol vyrobený pomocou orbitálu s a ďalšie dva cez orbitál tohto typu. typ p. Tu nastáva hybridizácia, to znamená, že neúplné orbitaly sa spájajú a vznikajú tri
hybridné orbitaly alebo hybridizovaný, ktoré sú rovnaké a odlišné od originálov: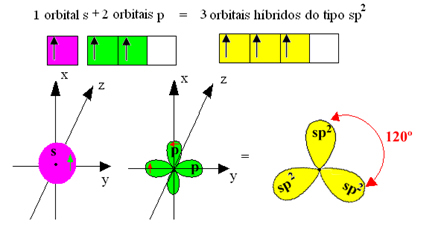
Pretože tieto hybridné orbitaly pozostávajú z jedného s orbitálu a dvoch p orbitálov, táto hybridizácia sa nazýva sp² hybridizácia.
Fluór, ktorý sa viaže na bór, má deväť elektrónov. Jeho elektronická distribúcia a orbitaly sú uvedené nižšie:
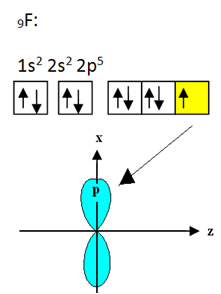
Upozorňujeme, že každý atóm fluóru môže tvoriť iba jednu kovalentnú väzbu a orbitál, ktorý túto väzbu vytvára, je typu p. Nižšie teda sledujte, ako sa formujú orbitaly pri vytváraní spojení, ktoré tvoria BF3 a uvidíte, ako sú odkazy identické σp-sp2:
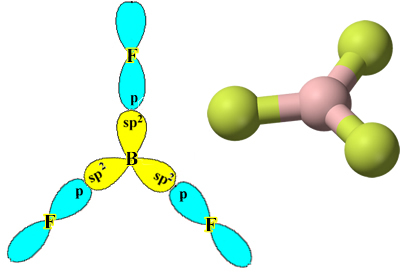
To sa stáva aj pri iných prvkoch, viď napríklad text „Hybridizácia berýlia”.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm