THE batérie je systém, kde prebieha oxidačno-redukčná reakcia. V tomto zariadení sa chemická energia vznikajúca pri spontánnej reakcii premieňa na elektrickú energiu.
Oxidačné a redukčné reakcie prebiehajú v bunke súčasne. Keď jeden druh podlieha oxidácii, daruje elektróny druhému druhu, ktorý po ich prijatí podlieha redukcii.
Preto ten, ktorý prechádza oxidáciou, je redukčným činidlom a ten, ktorý prechádza redukciou, je oxidačným činidlom.
THE oxidácia nastáva, keď druh stratí elektróny a stane sa katiónom: A → A+ + a-.
THE zníženie nastáva, keď druh získa elektróny a stane sa elektricky neutrálnym: B+ + a- → B.
V chemických rovniciach toto prenos elektrónov sa prejavuje zmenou oxidačného čísla (nox).
Vo vnútri článkov dochádza k redukčným reakciám a elektrický prúd vzniká migráciou elektrónov zo záporného na kladný pól.

Ako funguje zásobník?
Jeden redoxná reakcia môže byť všeobecne vyjadrená rovnicou:
A + B+ → A+ + B
Kde,
A: látka, ktorá je oxidovaná, stráca elektróny, zvyšuje svoju hodnotu a je redukčným činidlom.
B: látka, ktorá podlieha redukcii, získava elektróny, znižuje oxidáciu a je oxidačným činidlom.
Pozrite sa na nasledujúcom obrázku, ako možno tento proces znázorniť.
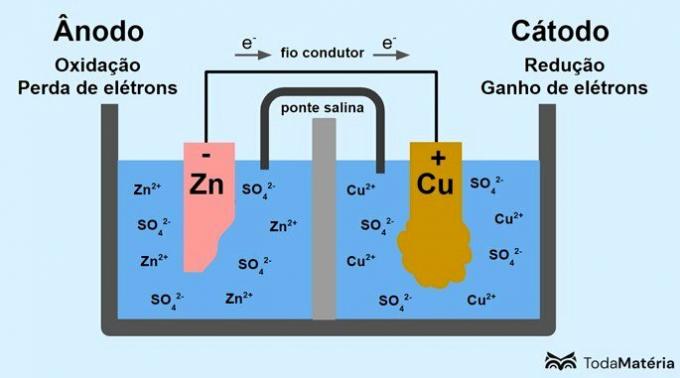
Systém rozdelený na dve poločlánky a tvorený dvoma kovovými elektródami spojenými zvonka vodivým drôtom vyvinul John Frederic Daniell (1790-1845) v roku 1836.
Batéria sa skladá z dvoch elektród spojených vodivým drôtom a elektrolytu, kde sú ióny. Elektróda je pevný vodivý povrch, ktorý umožňuje výmenu elektrónov.
anóda: elektróda, na ktorej dochádza k oxidácii. Je to tiež záporný pól batérie.
Katóda: elektróda, pri ktorej dochádza k redukcii. Je to tiež kladný pól batérie.
Na obrázku vyššie je kovový zinok anódou a podlieha oxidácia. Kovová meď je katódou a podlieha redukcii. K migrácii elektrónov (e-) dochádza z anódy na katódu cez vodivý drôt.
Reakcie, ktoré sa vyskytujú v obrazovom systéme, sú:
- anóda (oxidácia): Zn(s) → Zn2(tu) + 2e-
- Katóda (zníženie): Cu2+(tu) + 2e- → zadok(s)
- všeobecná rovnica: Zn(s) + zadok2+(tu) → zadok(s) + Zn2+(tu)
Zinok je kov s väčšou tendenciou strácať elektróny, a preto sa v roztoku tvoria katióny. Zinková elektróda sa začína opotrebovávať a strácať hmotu, pretože zinok sa uvoľňuje do roztoku pri tvorbe katiónov Zn2+.
Elektróny z anódy prichádzajú na katódu a katióny kovov sa po ich prijatí premenia na kovovú meď, ktorá sa usadí na elektróde a zväčší jej hmotnosť.
Soľný mostík je iónový prúd zodpovedný za cirkuláciu iónov v systéme, aby bol elektricky neutrálny.
Prečítajte si tiež o oxidačné číslo (nox).
typy batérií
V bunke je tendencia chemických druhov prijímať alebo darovať elektróny určená redukčným potenciálom.
Zložka s najvyšším redukčným potenciálom má tendenciu podstupovať redukciu, teda získavať elektróny. Druhy s najnižším redukčným potenciálom a následne aj najvyšším oxidačným potenciálom majú tendenciu prenášať elektróny.
Napríklad pri redoxnej reakcii Zn0(s) + zadok2+(tu) → zadok0(s) + Zn2+(tu)
Zinok oxiduje a daruje elektróny, pretože má redukčný potenciál E0 = -0,76 V, menej ako redukčný potenciál medi E0 = +0,34 V, a preto prijíma elektróny a podlieha redukcii.
Ďalšie príklady stohov nájdete nižšie.
Zásobník zinku a vodíka
Oxidačná polovičná reakcia: Zn(s) → Zn2+ + 2e- (A0 = -0,76 V)
Redukčná polovičná reakcia: 2H+(tu) + 2e- → H2(g) (A0 = 0,00 V)
Globálna rovnica: Zn(s) + 2H+(tu) → Zn2+(tu) + H2(g)
Reprezentácia zásobníka:
Medený a vodíkový článok
Oxidačná polovičná reakcia: H2(g) → 2H+(tu) + 2e- (A0 = 0,00 V)
Redukčná polovičná reakcia: Cu2+(tu) + 2e- → zadok(s) (A0 = +0,34 V)
Globálna rovnica: Cu2+(tu) + H2(g) → 2H+(tu) + zadok(s)
Reprezentácia zásobníka:
Získajte viac vedomostí o téme s obsahom:
- elektrochémia
- Elektrolýza
Bibliografické odkazy
FONSECA, M. R. M. Chémia, 2. 1. vyd. São Paulo: Attika, 2013.
SANTOS, W.L.P; MOL, G.S. Občianska chémia, 3. 2. vyd. São Paulo: Editora AJS, 2013.
USBERCO, J. Pripojiť chémiu, 2: chémiu. - 2. vyd. São Paulo: Saraiva, 2014.