Množstvo kalórií závisí od zloženia potravy. Takže na experimentálne stanovenie množstva tepla uvoľneného potravinou, ktoré môže telo absorbovať, používame prístroj tzv kalorimeter.
Toto zariadenie meria teplo uvoľnené potravinami pri spálení. Existuje niekoľko typov kalorimetrov; prvá z nich bola vytvorená v roku 1780 Lavoisierom a Laplaceom a bola a ľadový kalorimeter.
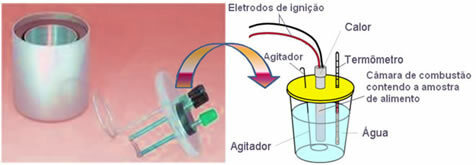
V dnešnej dobe je najpoužívanejšou a ktorá zohľadňuje vyššie vysvetlený kalorický koncept, vodný kalorimeter. Toto zariadenie je potiahnuté izolačným materiálom, aby sa zabránilo tepelným stratám z média; a jedlo, ktoré sa má analyzovať, sa umiestni do spaľovacia komora, ktorý obsahuje plynný kyslík a elektródy. Tieto elektródy prechádzajú elektrickým výbojom a spôsobujú ich vznietenie a spaľovanie potravín.
Známa masa vody obsiahnutá v kalorimetri absorbuje teplo uvoľnené spáleným jedlom a a teplomer meria zvýšenie teploty vody. Kalorimeter navyše obsahuje a miešadlo čo umožňuje, aby teplota vody zostala rovnomerná po celú dobu.
Takže ak použijeme napríklad hmotu 1 gramu cukru a kalorimeter má 1000 g vody, tak to nakoniec pozorujeme reakcie teplota vody klesla z 20 ° C na 24 ° C, to znamená, že sa zvýšila o 4 ° C, môžeme potom dosiahnuť energetickú hodnotu cukor. Páči sa mi to? Vzhľadom na pôvodný koncept kalórií máme:
| Zvyšujte z 1 ° C → 1 kal na gram vody |
| Zvyšujte od 4 ° C → 4 kalórie na gram vody |
Takže 1 g vody absorbuje 4 vápno. Použilo sa však 1 000 g vody a vzhľadom na to, že ním bolo absorbované všetko teplo uvoľnené pri spaľovaní, bola celková energia absorbovaná vodou 4 000 kal alebo 4 kcal. Preto vyvodzujeme, že:
Teraz neprestávajte... Po reklame je toho viac;)
| Energetická hodnota cukru = 4 000 kcal / g alebo 4 kcal / g. |
Transformácia na SI:
1 kcal 4,18 kJ
4 kcal / g x
x = 16,72 kJ / g
Ďalej môžeme použiť nasledujúcu rovnicu na výpočet množstva tepla odovzdaného alebo absorbovaného vodou:
| Q = m. ç. t |
Kde:
Q = teplo odovzdané alebo absorbované vodou;
m = hmotnosť vody;
c = merné teplo vody, ktoré sa rovná 1,0 kal / g. ° C alebo 4,18 J / g. ° C;
Δt = zmena teploty, ktorú voda trpí, ktorá je daná poklesom konečnej teploty o počiatočnú (tf - ti).
Pomocou tohto vzorca dostaneme rovnaký výsledok:
Q = m. ç. t
Q = 1 000 g. 1,0 kal / g. ° C. (24-20) ° C
Q = 4 000 kal
Q = 4,0 kcal
alebo
Q = m. ç. t
Q = 1 000 g. 4,18 kJ / g. ° C. (24-20) ° C
Q = 16,72 kJ
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Meranie kalórií v potravinách pomocou kalorimetra“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm. Sprístupnené 27. júna 2021.