Periodická tabuľka je spôsob organizovania všetkých chemických prvkov podľa ich vlastností a zobrazenia niektorých informácií o nich.
V každodennom živote je organizácia veľmi dôležitá pre uľahčenie nášho života. Predstavte si napríklad svoju skriňu chaotickú s ponožkami zmiešanými s košeľami a nohavicami. Bolo by to veľmi ťažké a hľadanie konkrétnej ponožky, ktorú by ste si chceli obliecť, by trvalo dlhšie, však?! Ak si ale usporiadate šatník a všetky ponožky dáte do jedného zásuvky, majte zásuvku. na tričká, iné na šortky a tak ďalej, bude oveľa jednoduchšie nájsť čo potreba. A čím viac oblečenia vlastníte, tým je potrebná väčšia organizácia.
Rovnako tak vedci v priebehu času objavili mnoho chemických prvkov. Pre predstavu, v roku 1850 bolo známych asi 60 prvkov, ale dnes vieme o existencii 118. Vznikla teda potreba usporiadať tieto chemické prvky spôsobom, ktorý by uľahčil pochopenie ich vlastností. Toto je úloha periodickej tabuľky chemických prvkov.
Periodická tabuľka, ktorú dnes používame, je usporiadaná do vodorovných čiar vo vzostupnom poradí podľa atómového čísla.
Mali by ste sa pozrieť do periodickej tabuľky, akoby ste čítali normálny text, to znamená, že vždy začína prvým radom a z ľavej strany na pravú a potom pokračuje dole do ďalšieho riadky.Chemické prvky boli umiestnené na Periodickej tabuľke na samostatných štvorcoch, kde je symbol prvku v polovica a hodnota atómového čísla je zvyčajne napísaná v hornej časti, ako je to znázornené na príklade vodíka nižšie:

Symbol vodíka a jeho atómové číslo uvedené v periodickej tabuľke
Atómové číslo je množstvo protónov alebo kladných nábojov, ktoré majú atómy prvku. Táto hodnota sa rovná počtu elektrónov, keď je atóm v základnom stave.Vodík je prvok, ktorý má iba 1 protón, to znamená, že jeho atómové číslo je 1. Preto je vodík prvým prvkom uvedeným v tabuľke. Ďalším prvkom, ktorý je na rovnakej línii ako vodík, je hélium, pretože má atómové číslo rovné 2.
Ak sa presunieme do spodného riadku, prvý je lítium s atómovým číslom rovným 3, vedľa je berýlium s atómovým číslom 4 a tak ďalej.Pozrite sa na prvé riadky periodickej tabuľky zobrazené nižšie a uvidíte, že poradie atómového čísla rastie tak akurát.
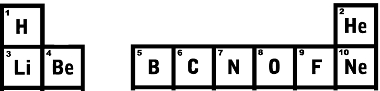
Prvé dva riadky periodickej tabuľky
V periodickej tabuľke je sedem riadkov a tieto riadky sa nazývajú obdobia. Pozri:

Periodické tabuľky
Existuje 18 stĺpcov, ktoré sú tzv rodiny alebo skupiny. Dôležitým aspektom je to prvky patriace do tej istej rodiny sú tie, ktoré majú podobné fyzikálne a chemické vlastnosti.

Rodiny alebo skupiny periodických tabuliek
Uvidíme, či to pochopíš? Povedzte mi, ktorý chemický prvok patrí do 4. obdobia a rodiny 16?
Ak ste povedali Se (selén), máte pravdu! Teraz mi povedzte, aké má atómové číslo. Máte pravdu, je to 34 rokov.
Na každom malom štvorci, ktorý prvok vidí, sú aj ďalšie dôležité informácie, napríklad atómová hmotnosť a elektróny ktoré sú v každej elektronickej vrstve atómov. Napríklad na nasledujúcom obrázku vidíte, že neón má Ne ako symbol, jeho atómové číslo je rovné 10, jeho atómová hmotnosť je 20,1797 u a jeho elektróny sú takto rozložené vo svojich vrstvách: 2 - 8, to znamená, že vo vrstve najbližšej k jadru sú dva elektróny a v najvzdialenejšej je osem elektróny.

Neónový symbol na periodickej tabuľke a jeho atóm
Teraz si všimnite dva zaujímavé aspekty: (1) iba neón má dve dráhy alebo vrstvy, kde sú vaše elektróny, preto obsadzuje 2. obdobie (2. riadok);a (2) má osem elektrónov na poslednej vrstve, preto on je rodina 18.
Toto nám ukazuje nasledujúce:
* Prvky, ktoré sú v rovnakom období periodickej tabuľky, majú rovnaké množstvo elektronických vrstiev a môžu mať najviac sedem;
* Chemické prvky, ktoré sú v rovnakej skupine periodickej tabuľky, majú rovnaký počet elektrónov v poslednej elektrónovej škrupine:
* Rodina 1: mať všetko 1 elektrón v poslednej elektronickej vrstve;
* Rodina 2: mať všetko 2 elektróny v poslednej elektronickej vrstve;
* Rodina 13: mať všetko 3 elektróny v poslednej elektronickej vrstve;
* Rodina 14: mať všetko 4 elektróny v poslednej elektronickej vrstve;
* Rodina 15: mať všetko 5 elektrónov v poslednej elektronickej vrstve;
* Rodina 16: mať všetko 6 elektrónov v poslednej elektronickej vrstve;
* Rodina 17: mať všetko 7 elektrónov v poslednej elektronickej vrstve;
* Rodina 18: mať všetko 8 elektrónov v poslednej elektronickej vrstve.
Niektorým skupinám alebo rodinám v periodickej tabuľke sú dané konkrétne mená, pozri niektoré:
Rodina 1: Alkalické kovy;
Rodina 2: Kovy alkalických zemín;
Rodina 16: Chalkogény;
Rodina 17: Halogény;
Rodina 18: Ušľachtilé plyny.

Organizácia rodín periodických tabuliek
Opäť si otestujme vaše vedomosti. Odpovedzte na nasledujúce otázky iba pomocou Periodickej tabuľky:
1 - Aký je názov rodiny chlórov?
2 - Aké je jeho atómové číslo a atómová hmotnosť?
3 - Koľko elektronických vrstiev má atóm chlóru?
4 - Koľko elektrónov má atóm chlóru vo svojom poslednom elektrónovom obale?
Odpovede:
1 - Halogény (rodina 17).
2- Atómové číslo chlóru je 17 a jeho atómová hmotnosť je rovná 35,45 u.
3 - Atóm chlóru má tri elektronické vrstvy, pretože patrí do 3. periódy tabuľky.
4 - Atóm chlóru má vo valenčnej škrupine sedem elektrónov, pretože patrí do rodiny 17.
Stále existujú ďalšie dôležité informácie, ktoré nám Periodická tabuľka poskytuje, a o ktorých si v ďalších textoch povieme lepšie. Ale tu diskutované sú tie hlavné, aby ste začali chápať, ako sú v nej usporiadané prvky. Pamätajte, že stôl nie je vyrobený na zdobenie, ale musíte ho dobre poznať, aby ste na neho mohli v prípade potreby odkazovať.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Využite príležitosť a pozrite si naše video kurzy týkajúce sa tejto témy:

