Det er fire hovedfaktorer som endrer reaksjonshastigheten, se hva de er:
1-KontaktflateO:Jo større kontaktflaten er, jo større reaksjonshastighet.
Dette er fordi reaksjoner finner sted mellom molekylene som sitter på overflatene til reaktantene. De utfører kollisjoner som, hvis de er effektive (med riktig retning og med mengden energi nødvendig), vil resultere i brudd på gamle bindinger og dannelse av nye, det vil si den kjemiske reaksjonen vil skje. Derfor, jo større kontaktflaten er, jo flere molekyler er i kontakt med hverandre, desto mer sannsynlig er det at effektive støt vil oppstå, og jo raskere blir reaksjonen.
Et eksempel som bekrefter dette er hvis du reagerer med samme mengde vann en hel brusetablett og en knust. Hvilket vil ende opp med å reagere raskere? Svaret er den knuste tabletten, siden kontaktflaten er mye større enn den for den kompakte tabletten.

Reaksjon mellom brusende syrenøytraliserende syre og vann i to forskjellige situasjoner: i det første glasset er syrenøytraliserende pulverisert; i det andre er det i nettbrett
2- Temperatur:Jo høyere temperatur, desto raskere blir reaksjonen.
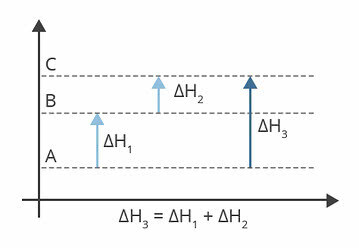
Dette skjer fordi, med økningen i temperatur, øker den kinetiske energien til molekylene til de reagerende stoffene, det vil si de beveger seg i høyere hastighet, noe som øker mengden effektive støt som resulterer i mer rask. Videre, når energien til molekylene øker, tillater dette dem å ha nok energi til å reagere, som kalles aktiveringsenergi.
For eksempel, når det oppstår en brann i en skog, som er et medium der varmetapet er lite, frigjør reaksjonen varme i mediet. Som et resultat øker temperaturen i miljøet, og dette gjør at forbrenningsreaksjonen finner sted enda raskere.

Økningen i temperatur øker hastigheten på skogbranner
Trykkokeren brukes også til dette formålet, da økningen i trykk øker temperaturen ved hvilken væsken koker og følgelig jo raskere tilberedningen av maten.

Trykkokeren er et eksempel på temperaturens innvirkning på reaksjonshastigheten
Ikke stopp nå... Det er mer etter annonseringen;)
På den annen side, hvis vi vil at en reaksjon skal gå saktere, kan vi senke temperaturen. Det er slik at vi for eksempel legger kjøtt i fryseren, da den lave temperaturen gjør at denne maten nedbrytes saktere.
3- Konsentrasjon:Jo større konsentrasjon av reaktanter, jo større reaksjonshastighet.
Når vi øker konsentrasjonen av reaktanter, øker vi antall reagerende molekyler eller partikler per enhet volum og følgelig antall kollisjoner mellom dem øker, noe som resulterer i raskere reaksjonshastighet.
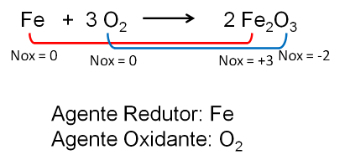
Et eksempel er forbrenning av kull. Hvis vi legger et stykke rødglødende kull i en kolbe med rent oksygen, vil reaksjonen finne sted mye raskere. Dette er fordi konsentrasjonen av en av forbrenningsreaktantene (oksygen) har økt. Før var oksygen til stede i luften, som er i en andel på omtrent 20%. Inne i flasken går denne andelen imidlertid til 100%.
4- Katalysatorer: De er stoffer som øker hastigheten på visse reaksjoner uten å delta i dem, det vil si uten å bli konsumert under reaksjonen.
For eksempel spaltes hydrogenperoksid over tid, men når det bringes i kontakt med blodet fra en skade, oppstår denne reaksjonen med en mye større hastighet, som ses gjennom dannelsen av bobler.
Dette skjer fordi blodet har et enzym kalt katalase som fungerer som en katalysator for nedbrytningsreaksjonen av hydrogenperoksid, det vil si at det øker hastigheten.
Katalysatorer er i stand til å øke reaksjonshastigheten fordi de virker ved å endre reaksjonsmekanismen ved å redusere reaksjons aktiveringsenergi. Med en mindre mengde aktiveringsenergi er det således lettere for de reagerende partiklene å nå denne energien og reagere.
Forstå bedre hvordan dette skjer ved å lese teksten Hvordan katalysatorstoffer fungerer.
Det er andre faktorer som kan forstyrre spesifikke reaksjoner. Noen eksempler er: lys,strøm, trykk (når det gjelder gassformede systemer) og reagensens natur (Jo større antall reagensbindinger som må brytes og jo sterkere de er, jo lenger tid tar reaksjonen).
Av Jennifer Fogaça
Uteksamen i kjemi