Det er flere måter å representere den samme kjemiske forbindelsen på, dette gjøres gjennom den kjemiske formelen, som kan gi oss litt informasjon om stoffet den representerer.
Vi vil nå kjenne 5 former for presentasjon av en forbindelse, og ta et eksempel på den organiske substansen Benzen.
flat strukturformel: Det er formelen som beskriver alle elementene som er tilstede i det sammensatte molekylet og arrangementet av atomene gjennom av en flat representasjon, er parene av elektroner som etablerer den kjemiske bindingen representert med bindestreker. (─). Strukturformelen ovenfor viser hvordan atomene som utgjør benzen er koblet sammen.

molekylær formel: I denne typen formler er elementet representert med symbolet etterfulgt av indeksen (abonnementsnummer) som indikerer antall atomer som er tilstede i hvert molekyl. Så vi har antall atomer som utgjør stoffet, som vi ser, er det 6 karbonatomer (C) og 6 hydrogener (H) i et benzenmolekyl.

empirisk formel: det er som en “oppsummert” måte å representere forbindelsene på. Den enkle strukturen lar oss bare forstå formen på benzenstrukturen og tilstedeværelsen av umettede (dobbeltbindinger).

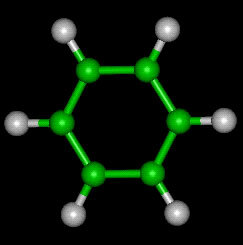
Ball Structure Formula: på denne måten identifiseres karbon og hydrogen etter farge og størrelse, hvor C er representert av den svarte fargen og H av den hvite fargen.


Formel i slag og ballstruktur
Denne siste representasjonen er den mest brukte for å sette inn emnet Organisk kjemi, det tillater det observere strukturens form og fremdeles visualisere typen binding som forbinder hydrogenene til kjeden hoved.
Det er faktisk deler på markedet for å montere strukturen til linjer og kuler, som om det var et puslespill, der læreren trinn for trinn kan demonstrere dannelsen av organiske forbindelser.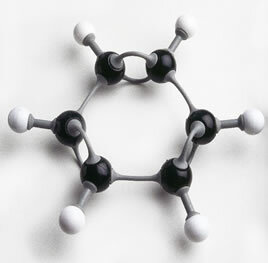
Foto av benzenring satt sammen med plastdeler: et utmerket undervisningsmateriale som skal jobbes med i klasserommet.
Av Líria Alves
Uteksamen i kjemi
Brasil skolelag
Se mer!
Strukturelle formler av karbon
kjemiske formler
Generell kjemi - Kjemi - Brasilskolen
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/classificacao-das-formulas.htm
