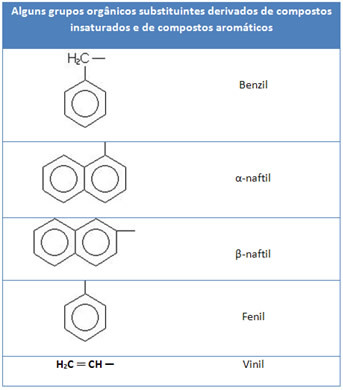
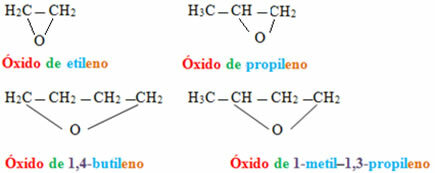
Det er tre typer alkadiene eller diener, som er:
1-akkumulert: Dobbeltbindinger er plassert på samme karbon og vises suksessivt:
─C ═ Ç ═ C ─
│ │
2- Isolert: Dobbeltbindingen er på forskjellige karbonatomer og er atskilt med minst to påfølgende enkeltbindinger:
│
─C ═ C C ─ C ═ C ─
│ │ │ │ │
3- Konjugater: Dobbeltbindinger vises vekselvis, og er atskilt med en enkelt enkeltbinding:
─C ═ C C ═ C ─
│ │ │ │
Et eksempel på en viktig konjugert dien er isopren, som er en basisk enhet av terpengruppen, en klasse organiske forbindelser. veldig viktig, noen eksempler på produkter dannet av isoprener er gummi, betakaroten (ansvarlig for den oransje fargen på gulrøtter), vitamin A og oljer som finnes i fruktskall, frø, blomster, blader, røtter, grønnsaker og tre, slik som limonen og myrcen.
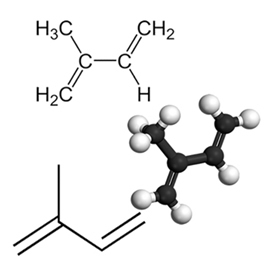
Til akkumulerte og isolerte diener, tilleggsreaksjoner oppstår akkurat som i tilfelle alkener, hva du kan forstå ved å lese teksten Tilleggsreaksjoner. Den eneste forskjellen er at diener gjennomgår denne typen dobbeltreaksjon, fordi de har to dobbeltbindinger, mens alkener bare har en dobbeltbinding.
Imidlertid, i tilfelle konjugerte diener, tilsetningsreaksjonen har en egenart, da disse forbindelsene kan gjennomgå resonans, slik at tilsetningen kan finne sted på to måter:
1- Tillegg 1.2:
Dette regnes som normal tilsetning, ettersom tilsetningen skjer på de to karbonatomer som lager samme dobbeltbinding, det vil si på karbon 1 og 2:
Ikke stopp nå... Det er mer etter annonseringen;)
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH─ CH ═ CH2
│ │
HBr
Se at denne typen reaksjoner følger Markovnikovs styre, binder hydrogenet til det mer hydrogenerte karbonet (med flere hydrogenatomer festet).
Tilsetning 1,2 behandles ved lave temperaturer (-60 ° C).
2- Tillegg 1.4:
I dette tilfellet fortsetter reaksjonen ved høye temperaturer. Det er viktig å påpeke at både produktet av tilsetning 1.2 og tilsetning av 1.4 alltid dannes, men temperaturen indikerer hvilken som vil bli dannet i større mengde.
Følgende er et eksempel på tillegg av type 1.4:
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH ═ CH─CH2
│ │
HBr
Merk at det følgende skjer, en av de delte elektronene i pi-båndet til hvert av de dobbelte karbonene deles med substituenten og de andre danner en ny dobbeltbinding mellom andre karbonatomer:
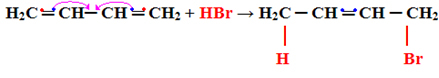
Av Jennifer Fogaça
Uteksamen i kjemi
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Tilleggsreaksjoner i Dienes"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/reacoes-adicao-dienos.htm. Tilgang 28. juni 2021.